-
干旱和遮荫是树木常受到的两类非生物胁迫形式,会影响到树木的存活、生长、代谢及多个生理过程。水分代谢和碳代谢是树木生长和存活的基础,在逆境下水分代谢和碳平衡的维持能力很大程度上决定了树木对逆境的适应能力。前人研究表明,“干旱导致树木水分长距离运输受阻”是“干旱导致树木死亡”的主要机制[1-2],同时干旱限制了植物的光合作用与碳素利用导致的碳饥饿也是干旱导致植物死亡的重要原因之一[3-5]。遮荫会导致植物碳摄取受阻,影响植物的碳素分配[6];也有研究表明,遮荫会在一定程度上缓解干旱对植物的影响[7],但遮荫与干旱的共同作用对植物的影响缺乏更深入的研究,这限制了人们对植物在干旱和遮荫交互逆境下水碳代谢和生长、存活关系的全面了解。黄酮类化合物是植物抵御逆境的重要次生代谢物质[8],一般在全光照条件下生长的植株,其黄酮的含量较高,而在遮荫条件下,黄酮类化合物的积累较少[9-10],干旱胁迫会促进植株黄酮类成分的合成积累,以抵御干旱胁迫对植株的影响[9, 11],但干旱和遮荫及其交互作用对黄酮类化合物含量有何影响,有待进一步深入研究。
沙棘广泛分布于我国的东北、西北、西南和黄土高原区,属于生态经济兼用树种,因其具有较好的生态适应性,在黄土高原被广泛种植。前期研究中显示,不同海拔、不同坡向及不同遮荫条件下沙棘的生长和存活情况存在较大的差别。不同水分和光照条件会对沙棘产生较大的影响[12],但目前尚不完全了解沙棘水碳代谢对不同水分和光照条件下的适应能力,也不了解干旱和遮荫两种胁迫对沙棘影响的交互作用方式。此外,沙棘黄酮类化合物含量与沙棘对环境条件的响应密切相关。因此,确定沙棘黄酮类化合物对干旱和遮荫的响应,将有利于全面了解沙棘环境适应性,也有助于了解沙棘黄酮类化合物含量对环境条件的响应。
本研究以中国沙棘(Hippophae rhamnoides L. subsp. sinensis Rousi
)为研究对象,通过比较干旱和遮荫对沙棘水分状况、光合作用、生长和生物量分配、碳平衡、黄酮类化合物含量的影响,旨在研究干旱和遮荫两种非生物胁迫形式下沙棘的水碳代谢与生长的关系,揭示干旱和遮荫对沙棘不同部位黄酮类化合物含量的影响,以期全面了解中国沙棘对水分和光照条件的适应能力,同时可以揭示干旱和遮荫对沙棘黄酮类化合物含量的影响。 -
试验于山西省晋中市太谷区山西农业大学林业站(112°35′06″ E,37°25′47″ N)遮雨棚内进行,该地区位于黄土高原东部,属温带大陆性季风气候。年均气温11 ℃,1月份平均气温−4.4 ℃,最低气温−11 ℃;年平均降水量437 mm,年平均日照时数2 500~2 600 h,无霜期150~190 d。
-
试验材料为3年生中国沙棘扦插苗,扦插材料取自同一沙棘雌株。于2021年4月初定植于高25 cm,直径20 cm的塑料盆中,培养基质采用沙壤土与细沙3:1混合,盆底放置塑料托盘与地面土壤隔离。2021年6月初选取生长基本一致的沙棘48株,随机分为4组,每组12株,分别进行正常浇水(正常供水土壤含水量为饱和含水量的70%、无遮荫)、干旱(土壤含水量为饱和含水量的40%、无遮荫)、遮荫浇水(土壤含水量为饱和含水量的70%、遮光50%)、遮荫干旱(土壤含水量为饱和含水量的40%、遮光50%)处理。遮荫处理采用遮荫网在盆栽植株南部和上部遮荫处理,干旱通过称量质量法控制土壤水分。每个处理随机分为2组,其中,1组(6株)用于测定水力学指标、光合指标;另一组(6株)用于测定生物量、非结构性碳水化合物(NSC)含量、黄酮类化合物含量。在处理2个月后(8月初)测定水势、导水损失率、光合作用等指标,在处理3个月后(9月初)测定生物量,并采集样品测定根、茎、叶非结构性碳水化合物含量。
-
在2021年8月上旬选择连续晴天,测定枝条的水势、导水损失率(Percentage loss of conductivity, PLC)。水势的测定时间为12:00—14:00,用Model 600水势仪(PMS,Albany,USA)测定,每个处理随机选取5~6个枝条进行测定。
正午PLC测量时间与正午水势相同,测定方法如下:为保证剪口浸没在水下,剪取20~30 cm长度枝条,带回实验室后用锋利的刀片在水中截取3~4 cm长的枝段,用低压液流法[13]获得PLC。测定溶液为0.025 mol·L−1 KCl溶液(0.22 µm微孔滤膜抽滤)。首先,以4 kPa的压差将KCl溶液通过枝段,收集流出的液体并通过万分之一天平称量质量,连接到天平的计算机通过LPFM软件计算流量,记录初始流量Ki(kg·m−1·s−1·MPa−1)。通过用相同的KCl溶液在0.175 MPa下高压冲洗约5 min,然后以与Ki相同的方式获得最大流速Kmax。PLC计算公式为: PLC = (1 − Ki/Kmax) × 100%
-
于2021年8月上旬选择连续晴天的上午9:00—11:00用Li-6400光合测定系统(LI-COR,Lincoln,USA)进行测定,分别测定其净光合速率、蒸腾速率、气孔导度,每个处理至少6次重复。
-
在2021年9月初,将每个处理的沙棘植株叶、茎、根分开,放置105 ℃烘箱杀青15 min,75 ℃烘干,称质量,计算植株生物量占比。 生物量占比=叶(茎、根)生物量/总生物量。
-
将烘干的叶、茎、根样品粉碎过100目筛用于测定可溶性糖、淀粉含量。可溶性糖、淀粉含量采用硫酸蒽酮法[14]测定,非结构性碳水化合物(NSC)含量 = 可溶性糖含量 + 淀粉含量。
-
黄酮含量采用亚硝酸钠-硝酸铝-氢氧化钠比色法测定[15]。
-
采用SPSS 26.0 软件对数据进行统计分析,采用One-way ANOVA进行方差分析,并用最小显著性差异数法(LSD)进行多重比较,以P < 0.05作为显著性的标准,并用Sigmaplot 13.0作图。
-
干旱处理的沙棘枝条水势显著低于正常浇水处理(P < 0.05),遮荫浇水处理中国沙棘枝条的水势略高于正常浇水处理,但未达到显著性差异水平,遮荫干旱处理中国沙棘的枝条水势略低于正常浇水处理,但没有显著性差异(图1A)。干旱处理的枝条PLC显著高于正常浇水处理(P < 0.05),比正常浇水处理高32.8%,遮荫浇水处理的枝条PLC与正常浇水处理没有显著性差异,遮荫干旱处理的枝条PLC显著高于其它3种处理(P < 0.05)(图1B)。干旱处理显著降低了枝条的水势,显著增加了枝条的PLC(表1);遮荫处理显著增加了枝条的水势,也显著增加了枝条的PLC;干旱和遮荫的共同作用没有对沙棘水势造成显著影响,但显著增加了枝条的PLC。
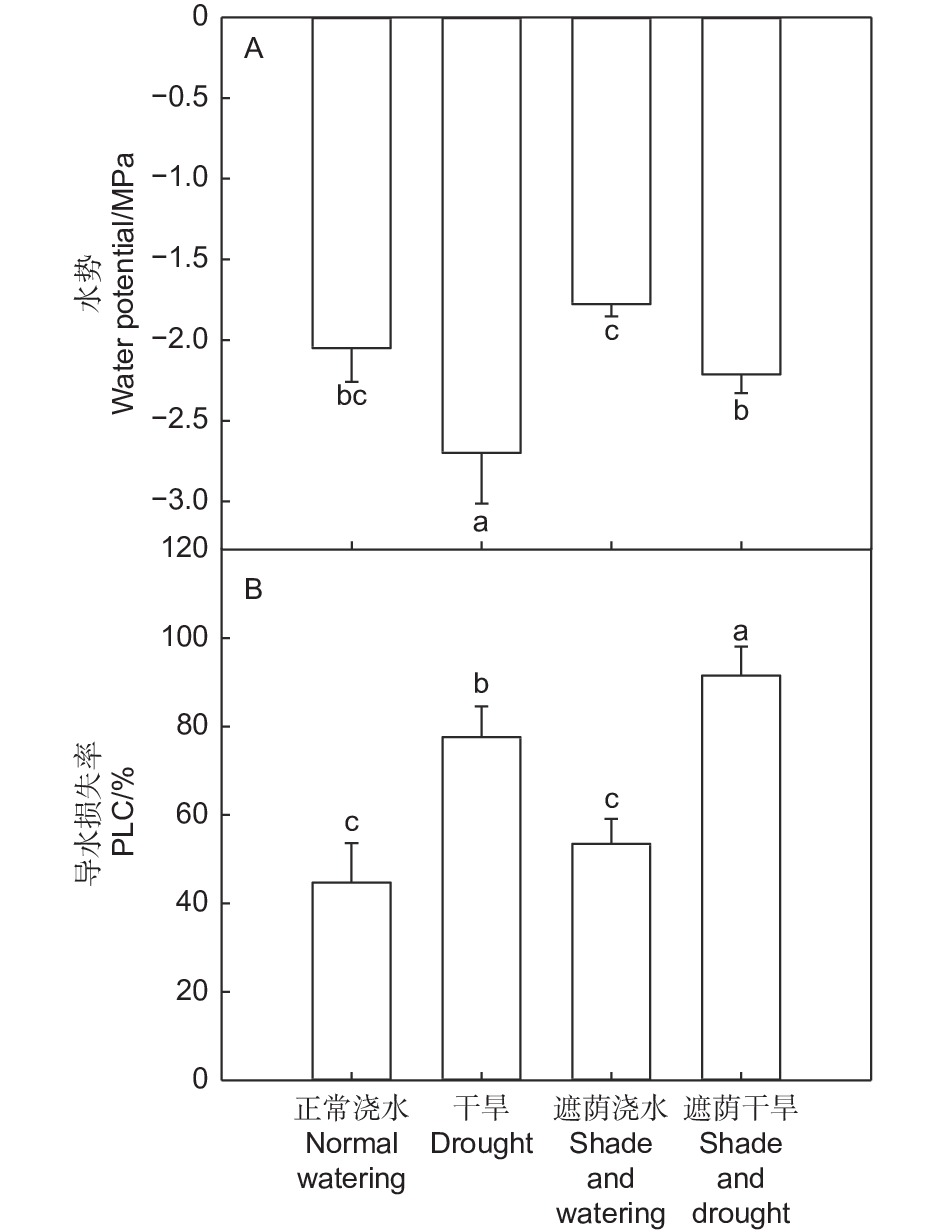
图 1 干旱和遮荫处理对中国沙棘水势和导水损失率的影响
Figure 1. Effect of drought and shading on water potential and hydraulic conductivity loss rate of H. rhamnoides
表 1 遮荫和干旱及交互对各指标的影响
Table 1. Effects of shading, drought and interaction on each index of H. rhamnoides
指标 Index 遮荫 shade 干旱 Drought 遮荫 × 干旱 Shade × Drought F P F P F P 水势 Water potential 10.752 < 0.05 21.981 < 0.01 0.847 0.384 导水损失率 PLC 10.766 < 0.01 105.322 < 0.01 0.550 0.474 净光合速率 Net photosynthetic rate 99.571 < 0.01 137.627 < 0.01 32.269 < 0.01 气孔导度 Stomatal conductance 42.430 < 0.01 132.111 < 0.01 10.603 < 0.01 蒸腾速率 Transpiration rate 41.480 < 0.01 151.147 < 0.01 8.347 < 0.05 叶生物量 Leaf biomass 54.508 < 0.01 23.186 < 0.01 13.924 < 0.01 茎生物量 Stem biomass 2.772 0.115 5.352 < 0.05 2.694 0.120 根生物量 Root biomass 54.638 < 0.01 3.029 0.102 22.020 < 0.01 叶可溶性糖含量 Leaf soluble sugar content 59.410 < 0.01 5.074 < 0.05 1.841 0.200 叶NSC含量 Leaf NSC content 78.204 < 0.01 5.695 < 0.05 0.005 0.946 茎NSC含量 Stem NSC content 74.445 < 0.01 40.000 < 0.01 31.156 < 0.01 根NSC含量 Root NSC content 0.298 0.595 100.793 < 0.01 70.814 < 0.01 叶黄酮含量 Lesf flavonoid content 12.540 < 0.01 17.082 < 0.01 2.619 0.144 茎黄酮含量 Stem flavonoid content 0.953 0.367 36.220 < 0.01 0.539 0.491 根黄酮含量 Root flavonoid content 16.938 < 0.05 54.978 < 0.01 6.240 0.067 -
干旱处理下,中国沙棘叶片的净光合速率、气孔导度和蒸腾速率均显著低于正常浇水处理(P < 0.05),分别比正常浇水处理低54.6%、66.3%、64.3%,遮荫浇水处理的净光合速率、气孔导度、蒸腾速率也显著低于正常浇水处理(P < 0.05),分别比正常浇水处理低49.1%、43.9%、39.6%。遮荫干旱处理的净光合速率、气孔导度、蒸腾速率均显著低于其它3种处理(P < 0.05)(图2)。干旱和遮荫的交互作用显著降低了中国沙棘的光合作用、气孔导度和蒸腾速率(表1)。这表明干旱和遮荫处理及二者的共同作用均显著降低了中国沙棘的光合能力。
-
干旱和遮荫浇水处理的叶生物量均显著低于正常浇水处理(P < 0.05),比正常浇水处理分别降低55.2%、71.8%,遮荫干旱处理的叶生物量显著低于正常浇水处理(P < 0.05),但与遮荫浇水处理差异不显著(图3A)。干旱处理和遮荫浇水处理的茎生物量与正常浇水处理差异不显著,遮荫干旱处理的茎生物量显著低于正常浇水处理、干旱处理和遮荫浇水处理(P < 0.05)(图3B)。干旱处理的根生物量显著大于正常浇水处理(P < 0.05),遮荫干旱处理的根生物量显著低于正常浇水处理(P < 0.05),也略低于遮荫浇水处理(图3C)。
以上表明干旱处理显著降低了中国沙棘的叶生物量,增加了中国沙棘的根生物量,遮荫干旱显著降低了中国沙棘的叶、根生物量,干旱和遮荫的共同作用显著影响了叶、根生物量(表1)。
-
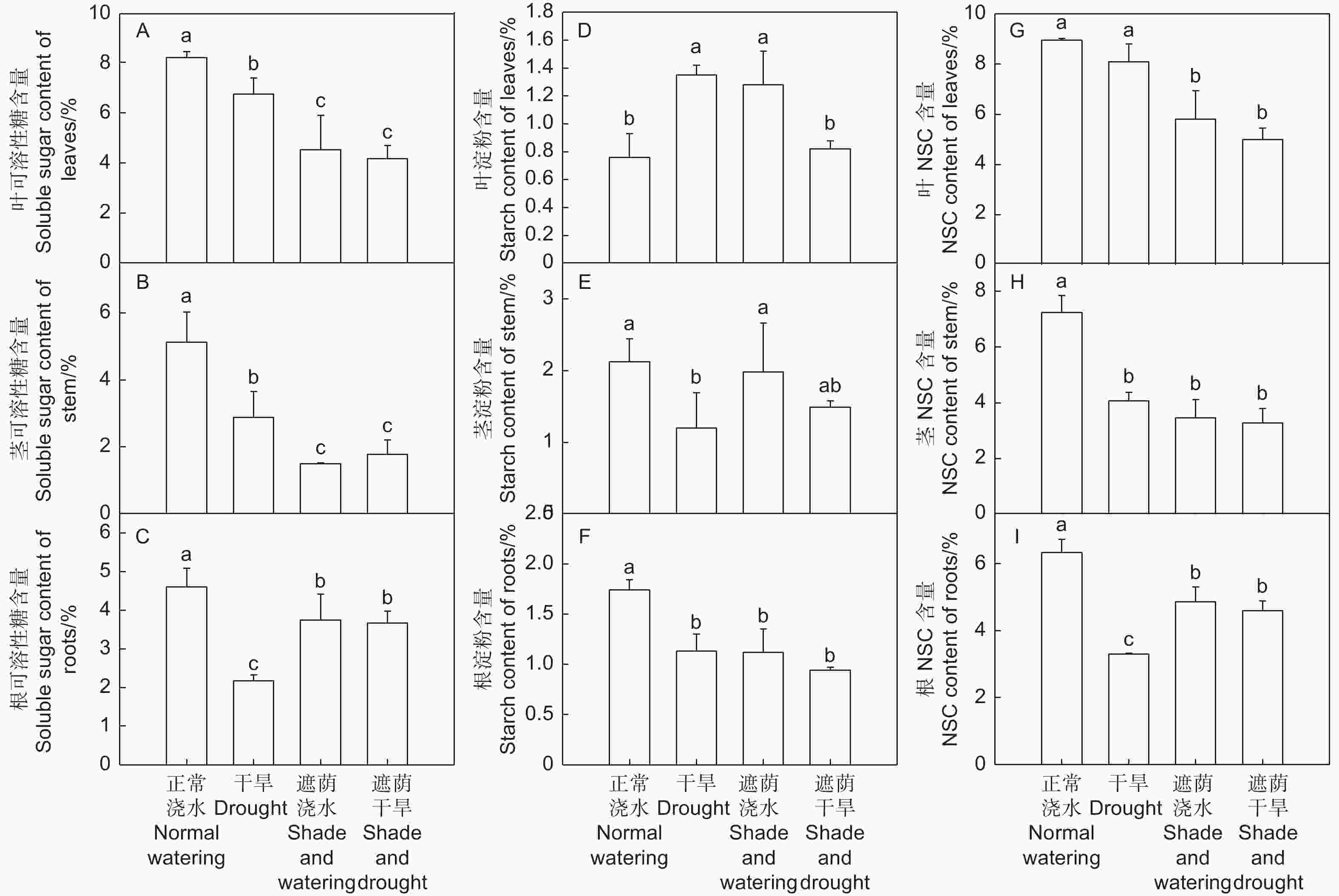
干旱处理和遮荫浇水处理、遮荫干旱处理的叶、茎、根可溶性糖含量均显著低于正常浇水处理(P < 0.05)。遮荫干旱处理的叶、茎可溶性糖含量显著低于干旱处理(P < 0.05),遮荫干旱处理的根可溶性糖含量显著高于干旱处理(P < 0.05),与遮荫浇水处理没有显著性差异(图4A、B、C)。
干旱处理的沙棘叶淀粉含量显著高于正常浇水处理(P < 0.05),但干旱处理的茎、根淀粉含量均显著低于正常浇水处理(P < 0.05)。遮荫浇水处理的叶淀粉含量显著高于正常浇水处理(P < 0.05),根淀粉含量显著低于正常浇水处理(P < 0.05)。遮荫干旱处理的叶淀粉含量与正常浇水处理没有显著性差异,根淀粉含量显著低于正常浇水处理(P < 0.05)(图4D、E、F)。
干旱处理的叶NSC含量与正常浇水处理没有显著性差异,茎和根NSC含量显著低于正常浇水处理(P < 0.05),遮荫浇水处理的叶、茎、根NSC含量均显著低于正常浇水处理(P < 0.05),遮荫干旱处理的叶、茎、根NSC含量均显著低于正常浇水处理(P < 0.05),与遮荫浇水处理没有显著性差异(图4G、H、I)。
以上表明干旱显著降低了沙棘茎和根NSC含量,遮荫显著降低了各个部位的NSC含量,干旱和遮荫的共同作用显著降低了沙棘茎和根的NSC含量。
-
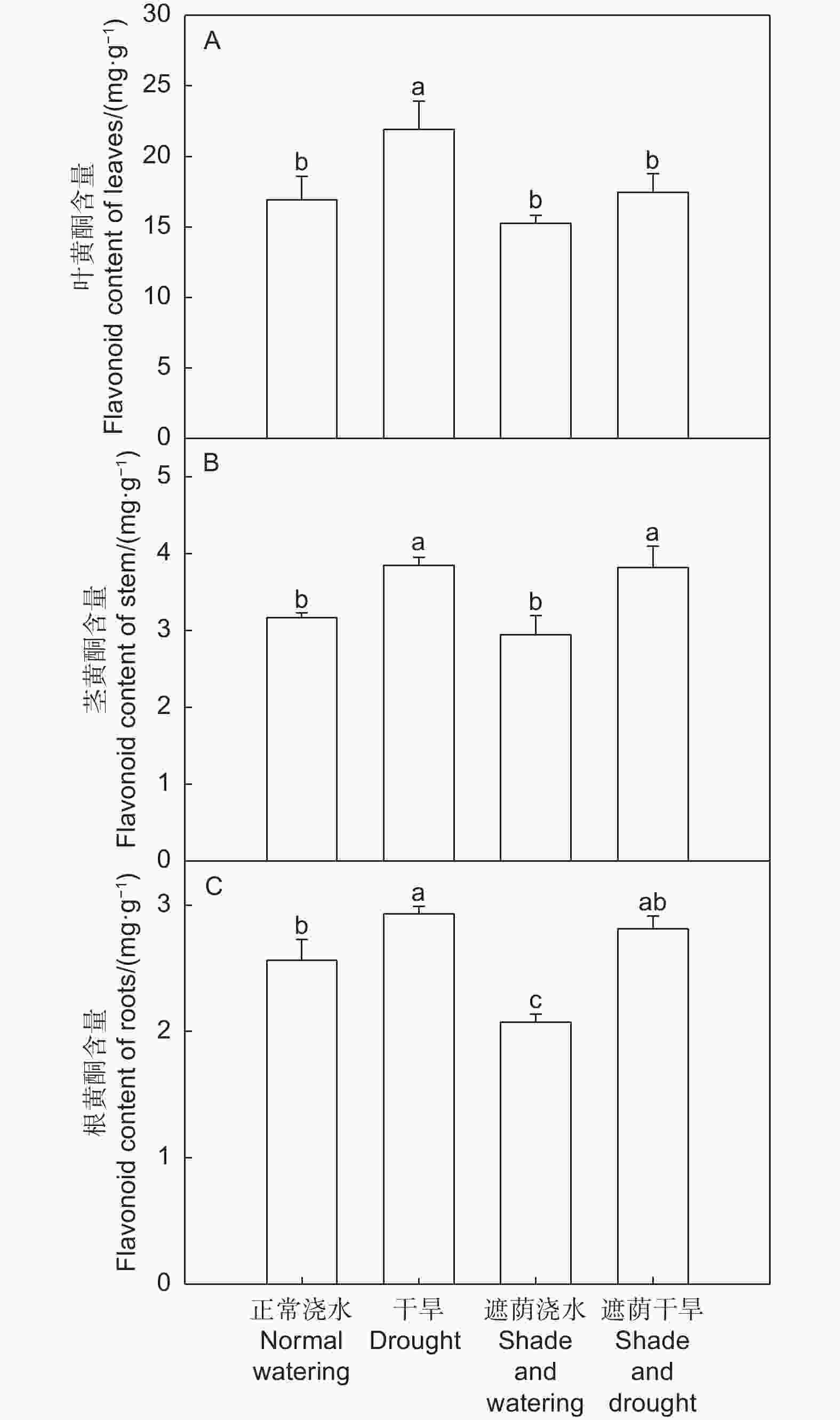
沙棘叶的黄酮含量在15~25 mg·g−1之间,茎黄酮含量在3~5 mg·g−1之间,根黄酮含量在2~3 mg·g−1之间。干旱处理的叶、茎、根黄酮含量均显著高于光照浇水处理(P < 0.05),遮荫浇水处理的根黄酮含量显著低于正常浇水处理(P < 0.05),遮荫浇水处理的叶和茎黄酮含量略低于正常浇水处理,但没有显著性差异,遮荫干旱处理的叶黄酮含量显著低于干旱处理(P < 0.05),与正常浇水处理和遮荫浇水处理没有显著性差异,茎黄酮含量显著高于正常浇水处理和遮荫浇水处理(P < 0.05),与干旱处理没有显著性差异,根黄酮含量与正常浇水处理和干旱处理没有显著性差异,显著高于遮荫浇水处理(P < 0.05)(图5)。这表明沙棘叶有较高的黄酮物质含量,干旱促进了各个部位黄酮物质的积累,遮荫显著降低了根黄酮的积累,干旱和遮阴的共同作用显著增加了茎黄酮含量,但对叶和根黄酮含量没有显著性影响。
-
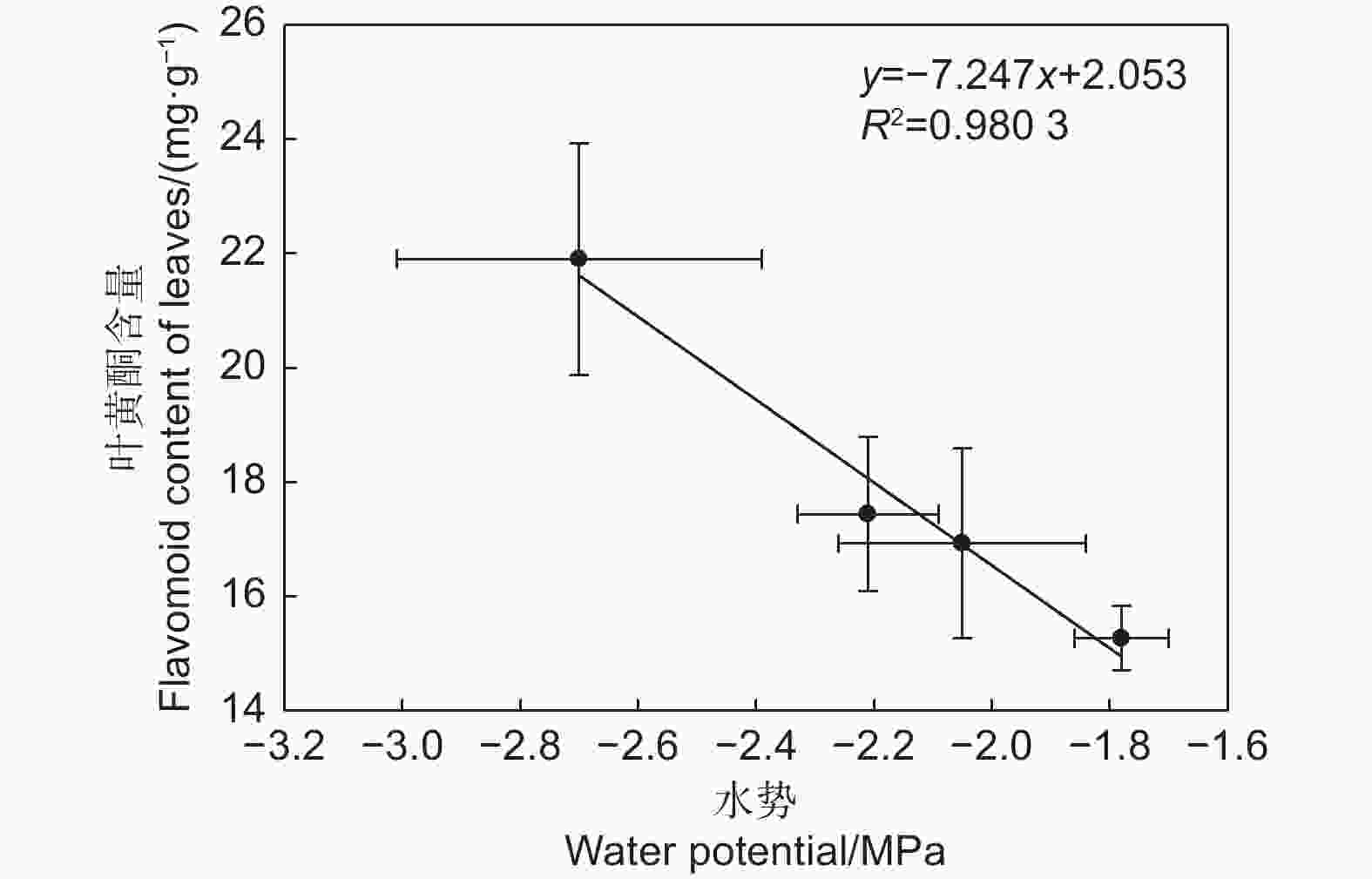
本研究分析了不同部位黄酮含量与其他指标间的相关性,结果表明:叶黄酮含量与植物的水势有显著性的负相关关系(图6)。
-
干旱是沙棘经常受到的非生物胁迫形式,沙棘资源丰富的华北、西北地区,每年受到较大程度的干旱或季节性干旱的影响[16],虽然之前的研究和生产经验认为沙棘有较好的耐旱性,但近年来越来越多的试验证据表明沙棘易受到干旱胁迫的影响[12,17]。本研究中,无论是正常光照处理还是遮荫处理下,干旱处理均显著降低了沙棘的水势,显著提高了沙棘的枝条PLC,这表明本研究的干旱对沙棘水分状况有较大程度的影响,进而会影响到沙棘的光合作用。因此,干旱处理的净光合速率显著低于正常浇水处理。遮荫是沙棘经常受到的另外一种非生物胁迫形式,沙棘属于灌木树种,树木较矮小,与其它树木混交情况下,会不同程度的受到遮荫的影响。前人研究表明,沙棘属于阳性树种,对遮荫的适应能力较差[16,18]。本研究中,遮荫对沙棘的水分状况没有显著影响,相反,在遮荫处理下,环境温度降低、蒸腾潜能减少,因此,遮荫会在一定程度上减少干旱胁迫的影响程度[7],在本研究中具体表现为水势一定程度的升高、沙棘水分状况较正常浇水处理略好,这和前期的研究结果类似[16],但遮荫处理受光照不足的影响,较大程度的限制了沙棘的光合作用[16]。
对枝条PLC的研究结果没有表现出与水势的一致响应,具体表现为遮荫干旱处理的水势虽然高于光照干旱处理,但枝条PLC也显著高于光照干旱处理,这可能是由于在遮荫处理下沙棘枝条的抗气穴栓塞能力或栓塞修复能力降低引起的,前人的研究中也有报道遮荫降低枝条的抗气穴栓塞能力[19];同时本研究的NSC含量结果也表明,遮荫处理显著降低枝条的可溶性糖和NSC含量,进而会影响气穴栓塞的修复能力[20],虽然本研究不能准确证明这种枝条PLC增加的原因是由抗栓塞能力下降还是修复能力下降引起,但导致的结果是水分输导能力下降。对植物在干旱条件下维持水分平衡不利,受干旱导致水分状况变差和遮荫导致光合速率降低两方面的影响,遮荫干旱处理的光合速率在4个处理中最低,进而导致碳摄取不足,并可能会影响生长和光合产物的储藏利用。
-
植物通过光合产物摄取的碳,通常分为两类用途,一部分用于植物的生长,转化为结构性碳,另外一部分用于呼吸代谢、储藏或发挥其渗透调节等生理功能[21],这一部分通常以NSC形式存在。在结构性碳方面,干旱处理下碳摄取受限,导致叶生物量显著降低,这种反应在正常光照处理下表现的更明显,另外干旱也会影响植物体不同部位的生物量分配[22],在光照处理下,干旱显著增加沙棘的根生物量,这有利于沙棘的水分吸收功能,应对干旱胁迫[23]。遮荫处理下的中国沙棘由于光照不足,限制了光合速率,导致叶生物量较正常光照处理显著降低,但对茎、根的生物量影响不显著;同时本研究也发现,在遮荫和干旱共同作用下,显著降低了根、茎、叶的生物量,这表明遮荫和干旱的共同作用对沙棘的生长更不利[7,16,24]。
干旱对植物NSC含量的影响没有一致性结论,有研究认为,干旱限制植物的光合作用,会导致植物出现NSC含量不足,甚至近年来的一些研究认为,干旱导致的NSC含量不足出现碳饥饿是导致植物死亡的重要原因[4];也有研究认为,干旱虽然限制植物的光合作用,但受植物本身生长减少的影响,干旱并不会导致NSC含量降低,甚至会出现NSC含量增加的情况,这可能与不同树种的调节策略有关[24]。本研究中,干旱处理并没有使中国沙棘的根、茎、叶NSC含量增加,相反茎和根均有较大程度的降低,这种降低对沙棘应对干旱不利,茎和根的NSC含量降低的主要原因是光合产物不足时,会优先就近供应距离光合部位较近的叶片,而距离光合部位较远的根和茎,一定程度的受到碳胁迫的影响。遮荫处理显著降低了不同部位的NSC含量,一方面是因为遮荫导致碳摄取能力降低,另一方面是遮荫一定程度上缓解了植物的水分状况,不需要那么多的可溶性糖用于渗透调节[25]。通常的研究认为,干旱会促进淀粉向糖的转化[26],但本研究中没有体现出这一规律,可能与干旱影响了淀粉向糖转化的能力有关,具体生理机制有待进一步研究。
-
黄酮类化合物是植物应对逆境的重要物质,在植物遭受干旱等非生物胁迫时,通过合成黄酮类化合物来消耗过剩的能量和活性氧,以减轻非生物胁迫所造成的细胞氧化损伤和膜质结构破坏[27-28]。本研究中,干旱处理显著增加了沙棘不同部位黄酮类化合物含量,这与前人的大部分研究结果一致[29-31];本研究结果也发现,叶黄酮含量与植物的水势有显著性的负相关关系,这表明随着水分状况的变差,黄酮类化合物含量有增加趋势,干旱处理能促进沙棘的黄酮类化合物合成。前人的大部分研究结果认为,遮荫会降低黄酮类化合物含量[32-33] 。本研究中,遮荫处理在一定程度上降低了黄酮类化合物含量[7]。同时黄酮类化合物也是重要的生物活性物质,本研究发现,沙棘叶片黄酮类化合物含量显著高于茎,是可用于黄酮类化合物提取利用的主要部位。
-
本研究比较了干旱和遮荫对沙棘水分状况、光合作用、生长、碳平衡、黄酮类化合物含量的影响,结果表明,干旱处理会影响中国沙棘的水分状况、碳摄取,降低茎和根的NSC储藏,增加黄酮类化合物含量;遮荫处理会影响中国沙棘的光合速率、根茎叶的NSC储藏,降低黄酮类化合物含量;干旱和遮荫的共同作用进一步加剧了中国沙棘水分长距离运输、光合作用、生物量积累和NSC储藏的不利影响。以上结果表明,干旱和遮荫均对中国沙棘光合作用、生长、NSC含量产生不利影响,干旱和遮荫的共同作用进一步降低了中国沙棘的水分输导能力、光合作用、生物量积累和NSC储藏,遮荫降低了中国沙棘对干旱胁迫的适应能力,适度干旱有利于黄酮类化合物的积累。
干旱和遮荫对中国沙棘水碳平衡和黄酮化合物含量的影响
Effects of Drought and Shading on Water Carbon Balance and Flavonoids Contents of Hippophae rhamnoides subsp. sinensis Rousi
-
摘要:
目的 研究干旱和遮荫对中国沙棘生长、水碳代谢和黄酮类化合物含量的影响有助于全面了解沙棘的生态适应性,同时有利于了解干旱和遮荫对沙棘黄酮类化合物含量的影响。 方法 本研究以中国沙棘为研究对象,比较了干旱(40%土壤水分饱和含水量)、遮荫(遮光50%)及二者交互处理下的水势、枝条导水损失率(PLC)、光合作用、生物量、非结构性碳水化合物(NSC)含量和黄酮类化合物含量的变化。 结果 干旱处理显著降低了中国沙棘的枝条水势、净光合速率、叶生物量、根和茎的NSC含量,显著增加了枝条PLC、根生物量;遮荫显著降低了净光合速率、叶生物量、根茎叶的NSC含量和黄酮含量,干旱和遮荫的共同作用显著增加了枝条PLC,降低了叶净光合速率、根茎叶生物量和NSC含量;且叶黄酮类化合物含量与枝条水势呈显著负相关。 结论 干旱会影响中国沙棘的水分状况、碳摄取,降低茎和根的NSC储藏,增加黄酮类化合物含量,遮荫会影响中国沙棘的光合速率、根茎叶的NSC储藏,干旱和遮荫的共同作用进一步降低了中国沙棘的水分输导能力、光合作用、生物量积累和NSC储藏,遮荫降低了中国沙棘对干旱胁迫的适应能力,适度干旱有利于沙棘黄酮类化合物的合成。 Abstract:Objective To study the effects of drought and shade on growth, water and carbon metabolism, and the flavonoid content of Hippophae rhamnoides subsp. sinensis Rousi for comprehensively understanding the ecological adaptability of sea-buckthorn and the response of flavonoid content to drought and shade. Methods The changes of water potential, branch hydraulic conductivity loss (PLC), photosynthesis, biomass, non structural carbohydrate (NSC) content and flavonoid content of Hippophae rhamnoides in drought (40% saturated soil water content), shading (50% shading) and their interaction were compared. Results Drought treatment significantly reduced branch water potential, net photosynthetic rate, leaf biomass, and NSC content in root and stem of Hippophae rhamnoides, and significantly increased the branch PLC and root biomass. Shading treatment significantly decreased the net photosynthetic rate, leaf biomass, NSC content of each part, and flavonoid content. The interaction of drought and shading significantly increased branch PLC, but decreased the leaf net photosynthetic rate, the biomass and NSC content of roots, stems and leaves. Moreover, there was a significant negative correlation between leaf flavonoids content and branch water potential. Conclusion Drought will affect water status and carbon uptake, reduce NSC storage in stems and roots, and increase flavonoids content in Hippophae rhamnoides. Shading will affect photosynthetic rate, and NSC storage of roots, stems and leaves, And the combination of drought and shade will further reduce the water transport capacity, photosynthesis, biomass accumulation and NSC storage of Hippophae rhamnoides. Shading will reduce the adaptability of Hippophae rhamnoides. to drought stress, and moderate drought is beneficial to the synthesis of flavonoids. -
Key words:
- Hippophae rhamnoides subsp. sinensis Rousi
- / shade
- / drought
- / water use
- / carbon balance
- / flavonoid
-
表 1 遮荫和干旱及交互对各指标的影响
Table 1. Effects of shading, drought and interaction on each index of H. rhamnoides
指标 Index 遮荫 shade 干旱 Drought 遮荫 × 干旱 Shade × Drought F P F P F P 水势 Water potential 10.752 < 0.05 21.981 < 0.01 0.847 0.384 导水损失率 PLC 10.766 < 0.01 105.322 < 0.01 0.550 0.474 净光合速率 Net photosynthetic rate 99.571 < 0.01 137.627 < 0.01 32.269 < 0.01 气孔导度 Stomatal conductance 42.430 < 0.01 132.111 < 0.01 10.603 < 0.01 蒸腾速率 Transpiration rate 41.480 < 0.01 151.147 < 0.01 8.347 < 0.05 叶生物量 Leaf biomass 54.508 < 0.01 23.186 < 0.01 13.924 < 0.01 茎生物量 Stem biomass 2.772 0.115 5.352 < 0.05 2.694 0.120 根生物量 Root biomass 54.638 < 0.01 3.029 0.102 22.020 < 0.01 叶可溶性糖含量 Leaf soluble sugar content 59.410 < 0.01 5.074 < 0.05 1.841 0.200 叶NSC含量 Leaf NSC content 78.204 < 0.01 5.695 < 0.05 0.005 0.946 茎NSC含量 Stem NSC content 74.445 < 0.01 40.000 < 0.01 31.156 < 0.01 根NSC含量 Root NSC content 0.298 0.595 100.793 < 0.01 70.814 < 0.01 叶黄酮含量 Lesf flavonoid content 12.540 < 0.01 17.082 < 0.01 2.619 0.144 茎黄酮含量 Stem flavonoid content 0.953 0.367 36.220 < 0.01 0.539 0.491 根黄酮含量 Root flavonoid content 16.938 < 0.05 54.978 < 0.01 6.240 0.067 -
[1] ROMY R, ANGELICA C, MARCUS Z, et al. Drought-induced xylem embolism limits the recovery of leaf gas exchange in Scots pine[J]. Plant physiology, 2020, 184(2): 852-864. doi: 10.1104/pp.20.00407 [2] LI Q, ZHAO M, WANG N, et al. Water use strategies and drought intensity define the relative contributions of hydraulic failure and carbohydrate depletion during seedling mortality[J]. Plant Physiology and Biochemistry, 2020, 153: 106-118. doi: 10.1016/j.plaphy.2020.05.023 [3] HARTMANN H. Carbon starvation during drought-induced tree mortality–are we chasing a myth?[J]. Journal of Plant Hydraulics, 2015, 2: 1-5. [4] ADAMS H D, ZEPPEL M J B, ANDEREGG W R L, et al. A multi-species synthesis of physiological mechanisms in drought-induced tree mortality[J]. Nature ecology & evolution, 2017, 1(9): 1285-1291. [5] MCDOWELL N G. Mechanisms linking drought, hydraulics, carbon metabolism, and vegetation mortality[J]. Plant physiology, 2011, 155(3): 1051-1059. doi: 10.1104/pp.110.170704 [6] 邓秀秀. 马尾松光合产物的分配特征及其受干旱和遮荫的影响[D]. 北京: 中国林业科学研究院, 2020. [7] 王 林, 代永欣, 张劲松, 等. 水分和光照条件对核桃-黄豆农林复合系统中黄豆光合作用和生长的影响[J]. 林业科学, 2020, 56(4):188-196. doi: 10.11707/j.1001-7488.20200421 [8] AHMED U, RAO M J, QI C, et al. Expression profiling of flavonoid biosynthesis genes and secondary metabolites accumulation in populus under drought stress[J]. Molecules, 2021, 26(18): 5546. doi: 10.3390/molecules26185546 [9] SZYMBORSKA S I. Developmental and chemical characteristics of Melittis melissophyllum L. in limited access of sunlight[J]. Herba Polonica, 2020, 66(1): 1-8. doi: 10.2478/hepo-2020-0003 [10] 贺小妮, 郑鹏坤, 胡喜巧, 等. 光照对红豆杉幼苗生长及黄酮、多糖含量的影响[J]. 现代园艺, 2018(7):19-20. doi: 10.14051/j.cnki.xdyy.2018.07.007 [11] 管仁伟, 郭瑞齐, 林慧彬, 等. 基于植物代谢组学技术的干旱及盐胁迫对黄芩中黄酮类成分影响的研究[J]. 中草药, 2022, 53(5):1504-1511. [12] 陈汉鑫. 山西野生沙棘对吕梁山区海拔和坡位的生理生态响应[D]. 晋中: 山西农业大学, 2020. [13] DAI Y X, WANG L, WAN X C. Relative contributions of hydraulic dysfunction and carbohydrate depletion during tree mortality caused by drought[J]. AoB Plants, 2018, 10(1): plx069. [14] MITCHELL P J, O'GRADY A P, TISSUE D T, et al. Drought response strategies define the relative contributions of hydraulic dysfunction and carbohydrate depletion during tree mortality[J]. The New phytologist, 2013, 197(3): 862-872. doi: 10.1111/nph.12064 [15] 任园宇, 魏东伟, 王中伟, 等. 亚硝酸钠-硝酸铝比色法测定干旱胁迫前后玉米幼苗的总黄酮含量[J]. 农学学报, 2020, 10(5):15-20. doi: 10.11923/j.issn.2095-4050.cjas20190800161 [16] 李海波, 薛 浩, 薛静茹, 等. 中国沙棘树冠上中下部枝条的水碳代谢与生长结实性状研究[J]. 林业科学研究, 2022, 35(5):188-195. doi: 10.13275/j.cnki.lykxyj.2022.005.021 [17] 吴 旭, 牛耀彬, 荀梦瑶, 等. 黄土丘陵区优势造林树种水分来源对季节性干旱的响应[J]. 生态学报, 2022, 42(10):4101-4112. [18] 黄 铨, 于倬德. 沙棘研究[M]. 北京: 科学出版社, 2006. [19] SCHOONMAKER A L, HACKE U G, LANDHÄUSSER S M, et al. Hydraulic acclimation to shading in boreal conifers of varying shade tolerance[J]. Plant, cell & environment, 2010, 33(3): 382-393. [20] TOMASELLA M, CASOLO V, NATALE S, et al. Shade-induced reduction of stem nonstructural carbohydrates increases xylem vulnerability to embolism and impedes hydraulic recovery in Populus nigra[J]. New phytologist, 2021, 231(1): 108-121. doi: 10.1111/nph.17384 [21] SCHOONMAKER A S, HILLABRAND R, LIEFFERS V J, et al. Seasonal dynamics of non-structural carbon pools and their relationship to growth in two boreal conifer tree species[J]. Tree Physiology, 2021, 41(9): 1563-1582. doi: 10.1093/treephys/tpab013 [22] JENSEN A M, ECKERT D, CARTER K R, et al. Springtime drought shifts carbon partitioning of recent photosynthates in 10-year old Picea mariana trees, causing restricted canopy development[J]. Frontiers in Forests and Global Change, 2021, 3: 601046. doi: 10.3389/ffgc.2020.601046 [23] ZHOU G, ZHOU X, NIE Y, et al. Drought‐induced changes in root biomass largely result from altered root morphological traits: evidence from a synthesis of global field trials[J]. Plant Cell & Environment, 2018, 41(11): 2589-2599. [24] PIPER F I, REYES-DIAZ M, CORCUERA L J, et al. Carbohydrate storage, survival, and growth of two evergreen Nothofagus species in two contrasting light environments[J]. Ecological Research, 2009, 24(6): 1233-1241. doi: 10.1007/s11284-009-0606-5 [25] PIPER F I, PAULA S. The role of nonstructural carbohydrates storage in forest resilience under climate change[J]. Current Forestry Reports, 2020, 6(1): 1-13. doi: 10.1007/s40725-019-00109-z [26] OUYANG S, GESSLER A, SAURER M, et al. Root carbon and nutrient homeostasis determines downy oak sapling survival and recovery from drought[J]. Tree Physiology, 2021, 41(8): 1400-1412. doi: 10.1093/treephys/tpab019 [27] 李丹丹, 梁宗锁, 普布卓玛, 等. 干旱胁迫对紫花苜蓿黄酮类化合物含量及其合成途径关键酶活性的影响[J]. 西北植物学报, 2020, 40(8):1380-1388. doi: 10.7606/j.issn.1000-4025.2020.08.1380 [28] HAGAGGI N S A, ABDUL-RAOUF U M. Drought-tolerant Sphingobacterium changzhouense Alv associated with Aloe vera mediates drought tolerance in maize (Zea mays)[J]. World journal of microbiology & biotechnology, 2022, 38(12): 248. [29] YAO H, WANG F, BI Q, et al. Combined analysis of pharmaceutical active ingredients and transcriptomes of Glycyrrhiza uralensis under peg6000-induced drought stress revealed glycyrrhizic acid and flavonoids accumulation via ja-mediated signaling[J]. Frontiers in Plant Science, 2022, 13: 920172. doi: 10.3389/fpls.2022.920172 [30] ZHANG G H, YU Z M, YAO B, et al. SsMYB113, a Schima superba MYB transcription factor, regulates the accumulation of flavonoids and functions in drought stress tolerance by modulating ROS generation[J]. Plant and Soil, 2022, 478(1-2): 427-444. doi: 10.1007/s11104-022-05466-6 [31] JAN R, KHAN M A, ASAF S, et al. Drought and UV Radiation stress tolerance in rice is improved by overaccumulation of non-enzymatic antioxidant flavonoids[J]. Antioxidants, 2022, 11(5): 917. doi: 10.3390/antiox11050917 [32] 邱 璐, 于邦友, 刘可可, 等. 遮荫对青钱柳苗生长和黄酮类化合物积累的影响[J]. 安徽农业大学学报, 2022, 49(03):359-367. doi: 10.13610/j.cnki.1672-352x.20220705.023 [33] YE J H, LV Y Q, LIU S R, et al. Effects of light intensity and spectral composition on the transcriptome profiles of leaves in shade grown tea plants (Camellia sinensis L. ) and regulatory network of flavonoid biosynthesis[J]. Molecules, 2021, 26(19): 5836. doi: 10.3390/molecules26195836 -




 下载:
下载: