-
微管(Microtubule)是由α-微管蛋白(α-tubulin,TUA)和β-微管蛋白(β-tubulin,TUB)以异二聚体的形式聚合成的中空管状结构,它与微丝(Microfilament)和中间纤维(Intermediate filament)共同组成了细胞骨架。微管蛋白是高度保守的,植物、动物、原生生物和真菌中的TUA和TUB蛋白具有高达88%的序列相似性[1-2]。迄今为止,人们已在拟南芥中发现6个TUA蛋白和9个TUB蛋白[3];在水稻中发现4个TUA蛋白[4]和8个TUB蛋白[5];在毛果杨中有8个TUA蛋白和20个TUB蛋白[6]。
微管对植物生长发育有着重要作用,研究表明,微管影响细胞形态发生,并最终影响植物的形态。Abe等[7]发现,拟南芥中TUA6和TUA4突变体lefty1和lefty2出现左旋生长的现象,其中,包括lefty1和lefty2双突变体幼苗下胚轴螺旋生长,根伸长区的径向细胞扩增,周质微管排列比野生型更加片段化且不对齐。在双突变体植株中,花丝细胞的各向异性生长受到严重损害。微管和微丝骨架的动态变化还参与了细胞周期进程的调节[8]。在拟南芥中,短期的低温会影响有丝分裂末期的径向微管列阵的形成,从而导致二倍体和多倍体花粉的产生[9]。微管在植物抵御环境胁迫的过程中也发挥重要作用。Wang等[10]发现, 盐胁迫诱导下拟南芥周质微管发生解聚和重组,提出周质微管在植物对盐胁迫的耐受性中发挥重要作用。此外,微管在信息传递[11]、纤维素微纤维沉积和木材形成[6, 12],调节气孔运动[13]等方面具有重要功能。
目前,林木微管蛋白功能的研究鲜有报道,特别是微管调控林木形态与材性分子机制的研究尚属空白。研究微管功能首先要对活体材料进行微管的形态观察,而现在缺乏林木微管研究的转基因材料,因此,建立稳定遗传的林木微管标记的转基因株系是首要且重要的。为此,首先要构建植物微管荧光表达载体,且通过瞬时表达等方法加以验证。构建荧光表达载体时,目的基因连接在荧光标签的N’端还是C’端一直存在争议,在拟南芥中发现,微管蛋白连接在荧光蛋白C’端时会影响转基因植物荧光观察[14]。本研究以84K杨为材料,克隆获得84KTUA5和84KTUB16基因,并通过同源重组的方法分别将84KTUA5和84KTUB16基因连接至荧光标签mCherry的N’端和C’端,共构建了4种重组载体,并通过烟草叶片瞬时表达系统,验证了重组蛋白的表达及其产生的荧光信号,为进一步研究杨树微管功能奠定基础。
-
本氏烟草( Nicotiana benthamiana ) 组培苗由本实验室保存。
-
大肠杆菌(Escherichia coli)TOP10 感受态细胞购自天根生化科技(北京)有限公司;根癌农杆菌GV3101感受态细胞购自北京华越洋生物科技有限公司;植物表达载体pCAMBIA 1300-mCherry购自淼灵质粒平台;EASYspin 植物 RNA 快速提取试剂盒、cDNA反转录试剂盒、pTOPO-TA- simple克隆试剂盒、琼脂糖凝胶纯化回收试剂盒、质粒小提试剂盒购自北京艾德莱生物科技有限公司;重组酶试剂盒购自南京诺唯赞生物科技有限公司;DL2000 DNA Marker 购自宝生物工程(大连)有限公司;试验过程中所用的限制性内切酶均购自NEB公司;引物的合成和序列的测定均在北京擎科公司完成;卡那霉素、壮观霉素、庆大霉素、利福平购自北京coolaber科技有限公司。
-
本研究中用到的拟南芥基因组数据库为http://www.arabidopsis.org/;毛果杨基因组数据库为https://phytozome. jgi.doe.gov/pz/portal.html;核酸和氨基酸序列比对软件为BioEdit。
-
根据文献中提供的毛果杨TUA5和TUB16基因编号[6],搜索其基因组数据库,分别获得PtTUA5和PtTUB16基因序列。由于微管蛋白在各物种间的保守性很高,因此,本研究以毛果杨的TUA5和TUB16基因为模板,利用Primer软件设计同源引物,用于克隆84K杨的TUA5和TUB16基因。提取84K杨的RNA并反转录成cDNA,以此为模板进行同源克隆,PCR克隆反应所用引物84KTUA5-UTR和84KTUA16-UTR的序列信息见表1。
表 1 84KTUA5和84KTUB16的引物
Table 1. The primers of 84KTUA5 and 84KTUB16
引物名称 Primer name 引物序列 Primer sequences (5' to 3') 同源克隆引物 84KTUA5-UTR F: ATAAACGTCTTCGCTCCTATTCTCC
R: TATTAGGCTACACCCATTACGAAGG84KTUA16-UTR F: TAACGCGAAACAAAAAATGAGAGAA
R: TCAAACACGAACACCAATACAAAACCherry N’端同源重组引物 84KTUA5-Cherry F: gcttcgaattctgcagtcgacATGAGAGAGTGCATTTCGATCCAC
R: atcccgggcccgcggtaccgCATGTACTCGTCACCATCATCATCA84KTUB16-Cherry F: gcttcgaattctgcagtcgacATGAGAGAAATCCTTCACGTTCAGG
R: atcccgggcccgcggtaccgCATCCCGGCAGCATCTTCTT连接肽PCR扩增引物 Linker-84KTUA5 F: AGGGAGGTGGAAGTGGAGGTAGCGGTATGAGAGAGTGCATTTCGATCCAC
R: TCACATGTACTCGTCACCATCATCALinker-84KTUB16 F: GGGAGGTGGAAGTGGAGGTAGCGGTATGAGAGAAATCCTTCACGTTCAGG
R: TTACATCCCGGCAGCATCTTCTTCherry C’端同源重组引物 Cherry-84KTUA5 F: ggcggcatggacgagctgtacaAGGGAGGTGGAAGTGGAGGTAG
R: attctagcccctagatcacttgtacaTCACATGTACTCGTCACCATCATCATCherry-84KTUB16 F: ggcggcatggacgagctgtacaAGGGAGGTGGAAGTGGAGGTAG
R: gcattctagcccctagatcacttgtacaTTACATCCCGGCAGCATCTTCT鉴定引物 Gene-Cherry F: acgagctcaagcttcgaattctg
R: caccttgaagcgcatgaactccCherry-Gene F: gactacaccatcgtggaacagtac
R: acgttgtaaaacgacggccagt克隆得到的84KTUA5和84KTUB16基因分别与pTOPO-T simple载体连接,连接产物转化大肠杆菌TOP10感受态细胞,并涂布于含Amp(100 mg·L−1)的LB固体培养基上,37℃倒置培养12 h,挑取单菌落,进行菌落PCR鉴定并测序。测序结果利用BioEdit软件与毛果杨的TUA5和TUB16基因进行序列比对。
-
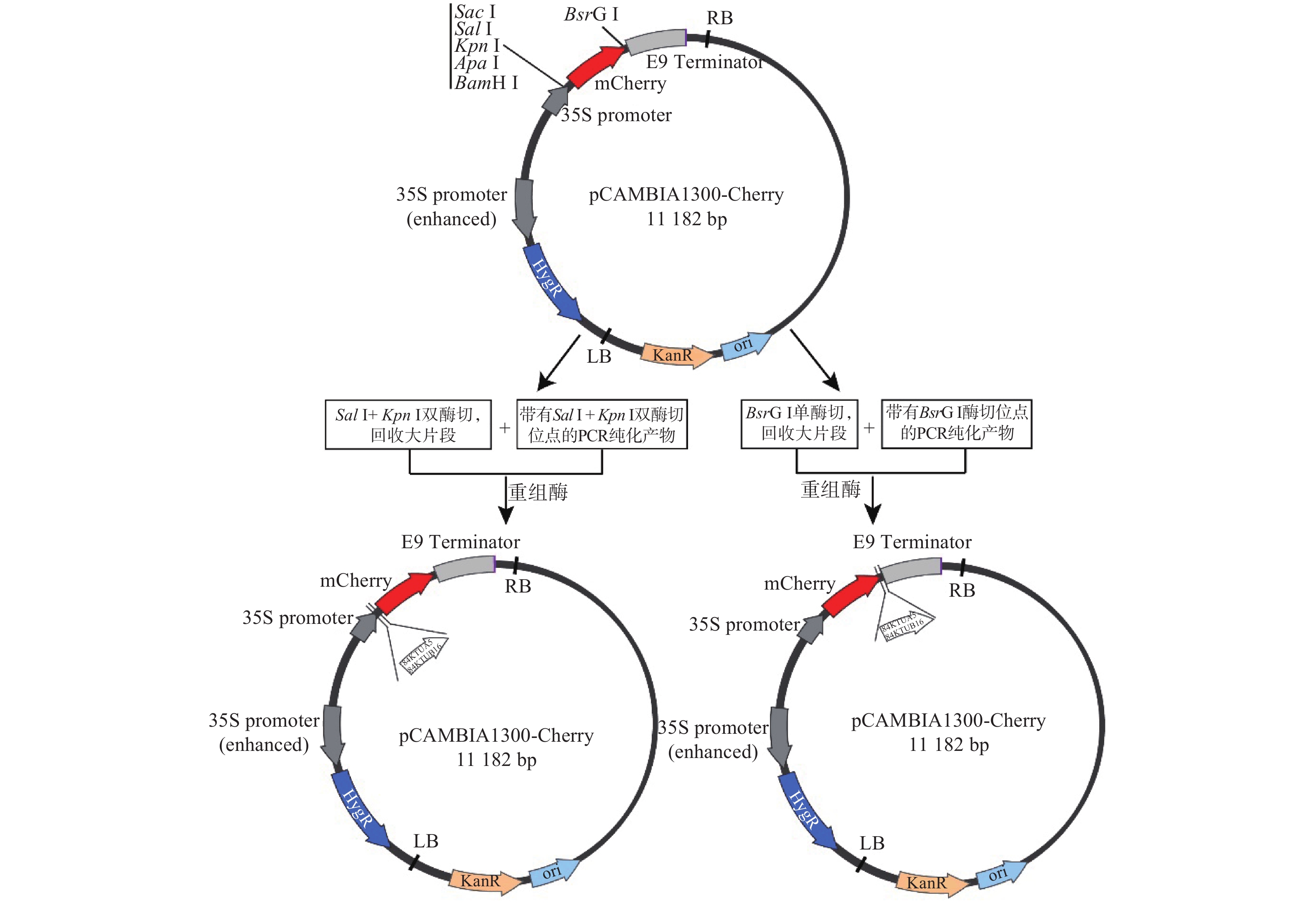
84KTUA5和84KTUB16与荧光蛋白基因mCheery N’端连接植物表达载体构建的具体步骤如下:双酶切(KpnⅠ和SalⅠ)pCAMBIA 1300载体,设计与载体一致的同源重组引物(表1),PCR扩增84KTUA5和84KTUB16基因,利用重组酶clonExperss Mix将扩增得到的目的基因连接在pCAMBIA 1300载体mCherry荧光标签的N’端,获得植物过表达载体pCAMBIA 1300-84KTUA5-mCherry和pCAMBIA 1300-84KTUB16-mCherry,转化大肠杆菌TOP10感受态细胞,涂布于含Kan(50 mg·L−1)的LB固体培养基上,37℃倒置培养12 h,挑取单菌落进行菌落PCR鉴定。鉴定采用的上下游引物序列分别来自于载体和插入基因(表1),筛选阳性克隆并测序。
84KTUA5和84KTUB16与荧光蛋白基因mCheery C’端连接植物表达载体构建的具体步骤如下:由于mCherry荧光标签的C’端存在终止密码子且无过度序列,为了同时保证插入蛋白和荧光蛋白形成正确的构象,84KTUA5和84KTUB16基因需借助连接肽连接在mCherry荧光标签的C’端。连接肽的序列为(5’-GGAGGTGGAAGTGGAGGTAGCGGT-3’),PCR扩增获得linker-84KTUA5和linker-84KTUB16序列,引物见表1。纯化回收后分别与pTOPO-T simple载体连接,转化大肠杆菌TOP10感受态细胞,涂布于含Amp(100 mg·L−1)的LB固体培养基上,37℃倒置培养12 h,挑取单菌落进行菌落PCR鉴定并测序。采用同源重组的方法将上述序列与pCAMBIA 1300载体连接(酶切位点为BsrG I-HF),获得植物过表达载体pCAMBIA 1300-mCherry-84KTUA5和pCAMBIA 1300-mCherry-84KTUB16,转化大肠杆菌TOP10感受态细胞,涂布于含Kan(50 mg·L−1)的LB固体培养基上,37℃倒置培养12 h,挑取单菌落进行菌落PCR鉴定,引物见表1,筛选阳性克隆并测序。载体构建过程见图1。
-
构建成功的重组质粒通过电击转化法转入农杆菌GV3101中,涂布在含有Rif(50 mg·L−1)、Kan(50 mg·L−1)和Gent(50 mg·L−1)的LB固体培养基上,28℃倒置培养24 h,挑取单菌落进行菌落PCR鉴定并测序。
-
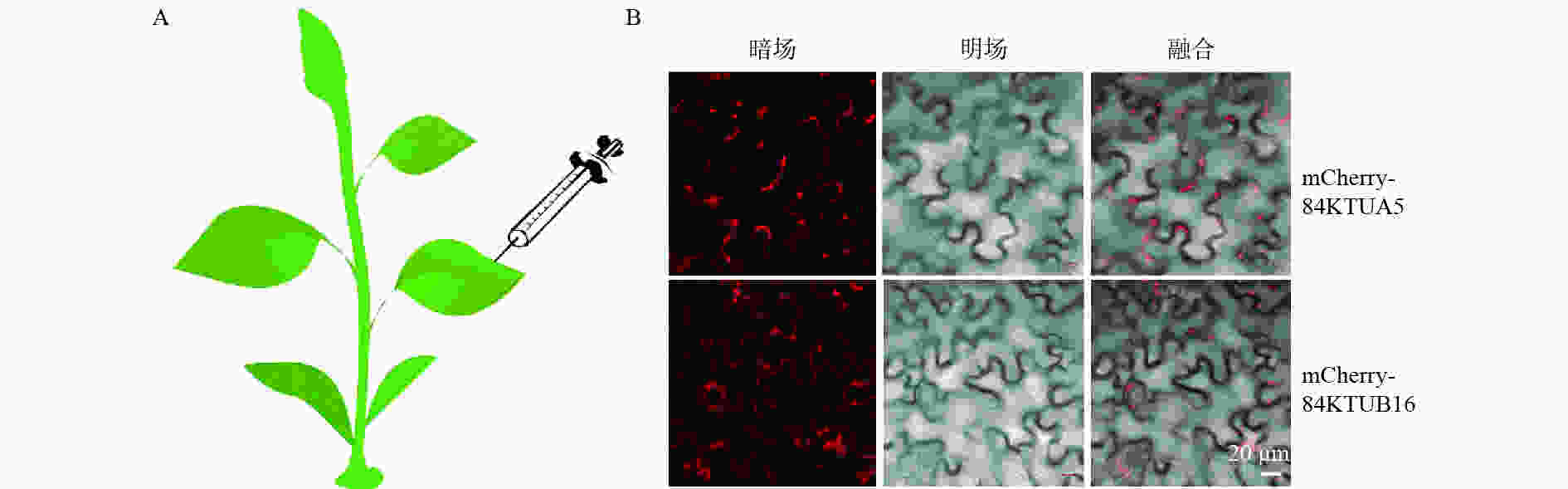
含有重组质粒的农杆菌菌液扩大培养至OD600=0.6~0.8,5 000 rpm离心10 min,收集菌体,配制烟草注射液(10 mmol·L−1 MgCl2,10 mmol·L−1 MES,pH 5.6),加入200 μmol·L−1 AS(乙酰丁香酮),悬浮菌体,使OD600约为1.0,室温放置2 h,选取3~4周长势较好的本氏烟草为植物材料,按照Imogen等[15]的瞬时表达方法,用注射器将注射液从叶片下表皮注射到烟草叶片内(图2A)。
农杆菌侵染48 h后的本氏烟草叶片置于滴有蒸馏水的载玻片上,做成临时封片,立即在激光共聚焦显微镜下观察叶片组织的上表皮细胞。本研究中所用的显微镜为Zeiss LSM510倒置激光扫描共聚焦显微镜。所用激光器为594 nm氦氖激光器(2 mW),激发光波长为594 nm,发射光接收范围为630~695 nm。用于图像采集的显微镜物镜为40×物镜,数值孔径为1.44,针孔大小为1 AiryUnit,扫描分辨率为1 024×1 024。采用Zen软件分析实验结果。
-
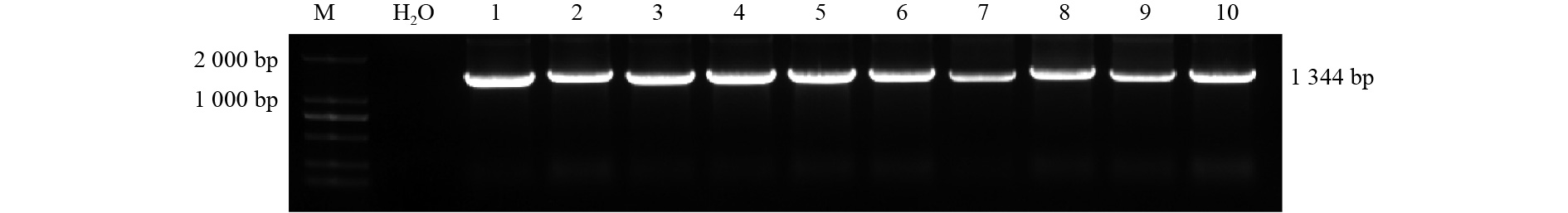
从克隆产物菌落PCR鉴定结果(图3)可以看出:在1 300 bp左右有明显条带,与预测的目的基因片段大小吻合,初步确定为目的基因片段。测序结果显示:84KTUA5基因CDS序列全长1 344 bp,编码448个氨基酸;84KTUB16基因CDS序列全长1 356 bp,编码452个氨基酸,利用BioEdit软件对84K杨与毛果杨中的TUA5和TUB16基因序列进行同源比对(表2),其同源性分别达98.80%和96.70%。
表 2 序列同源性比对
Table 2. Sequences homology alignment %
Sequences Pt-TUA5 84K-TUA5 Pt-TUB16 84K-TUB16 Pt-TUA5 ID 98.80 50.50 50.30 84K-TUA5 98.80 ID 50.50 50.30 Pt-TUB16 50.50 50.50 ID 96.70 84K-TUB16 50.30 50.30 96.70 ID -
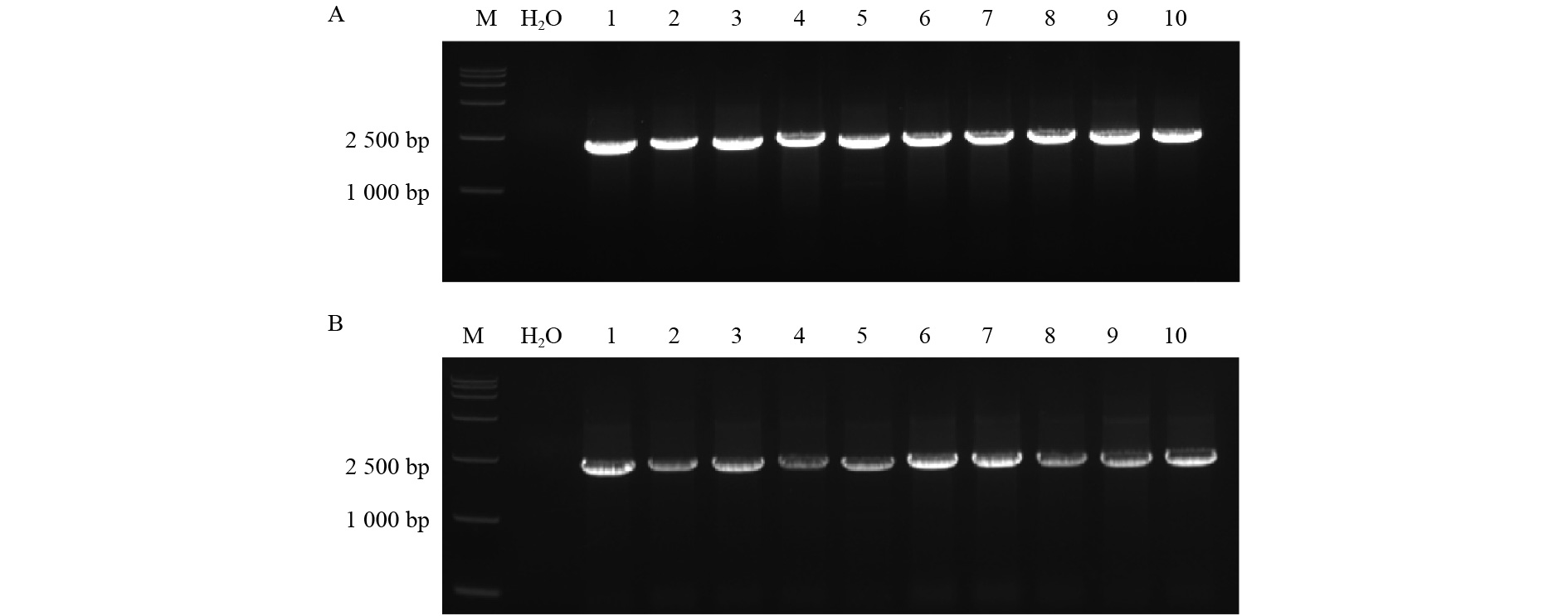
对4种重组表达载体pCAMBIA 1300-84KTUA5-mCherry、pCAMBIA 1300-84KTUB16-mCherry、pCAMBIA 1300-mCherry-84KTUA5、pCAMBIA 1300-mCherry-84KTUB16进行菌落PCR鉴定。由图4可以看出:2 200 bp左右有明显条带,与预测序列大小一致。经测序后,用BioEdit软件进行序列分析,结果表明,目的基因已成功插入pCAMBIA 1300-mCherry表达载体中。
-
激光共聚焦结果(图2B)显示:pCAMBIA 1300-mCherry-84KTUA5和pCAMBIA 1300-mCherry-84KTUB16重组质粒转化的烟草叶片上表皮细胞的细胞膜上有红色荧光分布,表明这两种融合蛋白能够正确表达,可以用于后续的遗传转化实验;而pCAMBIA 1300-84KTUA5-mCherry和pCAMBIA 1300-84KTUB16-mCherry重组质粒转化的烟草叶片上表皮细胞无法观察到红色荧光,说明这两种融合蛋白未能正确表达,无法用于后续实验。本实验观察的是叶片上表皮细胞,几乎不含叶绿体,因此,叶绿体自发荧光对观察结果的影响较小,且由于荧光标记的是周质微管,因而,只在细胞边缘发现红色荧光。
-
林木遗传改良的两个重要方向:林木材性的遗传改良和林木形态的遗传改良。现阶段,针对林木材性遗传改良的研究主要集中在木质素及纤维素合成与调控的分子机理上[16],直接研究木质素和纤维素合成与调控的相关通路及结构基因已成为当今的热点。微管作为纤维素合酶的轨道,指导了纤维素的合成与延伸[12, 17]。因此,研究林木微管的结构与功能,解析微管间接调控林木材性的分子机理对林木遗传改良同样具有十分重要的意义。林木形态的改良还主要集中在传统的选育水平,从分子水平解析林木形态决定的关键因子显得尤为重要。微管通过不同的排列方式决定了细胞的形态,最终导致了植株的形态差异,研究微管的结构与功能对林木的形态改良同样具有十分重要的意义。为了弥补研究林木微管功能所需活体材料的空缺,建立稳定遗传的林木微管标记的植物材料十分必要。本研究旨在构建林木微管功能研究植物表达载体,并让其在植物中表达,为建立微管功能研究林木转基因材料奠定基础。
高度保守的微管蛋白在物种间具有很高的序列相似性,毛果杨中有8个TUA蛋白和20个TUB蛋白,本研究选取了本底表达量较高的PtTUA5和PtTUB16基因作为模板设计引物,同源克隆得到84K杨的84KTUA5和84KTUB16基因,分析结果显示:84KTUA5和PtTUA5同源性为98.80%,84KTUB16 和PtTUB16同源性为96.70%,将二者分别与pCAMBIA 1300载体mCherry荧光标签的N’端和C’端进行同源重组,构建植物过表达载体。
pCAMBIA 1300系列载体为双元表达载体,是目前比较主流并得到广泛认可的植物表达载体。相比于卡那霉素或草铵膦等抗性基因,pCAMBIA 1300载体在植物中具有的潮霉素抗性更易筛选获得阳性植株。本研究中选用的mCherry为红色荧光蛋白,为将来以其他颜色荧光(如GFP/YFP荧光蛋白)研究微管功能提供背景材料。
构建的4种重组质粒中,目的基因连接在mCherry荧光标签N’端的融合蛋白未能在烟草中成功表达,推测原因是融合蛋白没有正确折叠形成有生物学功能的蛋白质。直接将两种蛋白融合时常会导致嵌合的蛋白形成空间位阻,影响蛋白活性,连接肽的引入对融合蛋白的表达、活性和稳定性有重要作用。连接肽有柔性和刚性之分,柔性连接肽主要由Gly和Ser组成,如Huston等[18]提出的(GGGGS)n(n≤6)序列,刚性连接肽是α螺旋结构的,一般使用的是(EAAAK)n(n≤6)。连接肽的长度影响融合蛋白的活性和稳定性。本研究中设计了8个氨基酸长度的柔性连接肽(GGGSGGSG),用于目的基因与mCherry基因的C’端连接,使融合蛋白成功表达。
-
本研究分别构建了84K杨TUA5和TUB16基因与pCAMBIA 1300-mCherry的4种融合表达载体,并通过农杆菌介导的烟草瞬时表达证实:目的基因通过连接肽连接在pCAMBIA1300载体mCherry荧光标签C’端的融合表达载体pCAMBIA 1300-mCherry-84KTUA5和pCAMBIA 1300-mCherry-84KTUB16能够在植株中正确表达,且能产生较强的红色荧光信号。杨树微管功能研究植物表达载体的构建及验证,为研究微管调控林木形态与材性奠定了基础。笔者将利用以上2种融合表达载体进行杨树的遗传转化,进一步研究杨树各个组织微管形态的差异。
杨树微管功能研究植物表达载体构建及验证
Construction and Verification of Plant Expression Vectors for Poplar Microtubule Function Research
-
摘要:
目的 分别构建84K杨的微管蛋白TUA5和TUB16与红色荧光蛋白mCherry融合的植物过表达载体,瞬时表达验证载体在植物体内表达后的荧光信号,为研究杨树微管功能奠定基础。 方法 以毛果杨微管蛋白TUA5和TUB16的基因序列为模板,设计84K杨的TUA5和TUB16基因的引物,提取野生型84K杨的RNA并反转录成cDNA,同源克隆得到84KTUA5和84KTUB16基因,分别连接在pCAMBIA 1300载体mCherry荧光标签的N’端和C’端,转化到大肠杆菌TOP10感受态细胞中,通过菌落PCR和测序鉴定获得阳性单克隆,并通过电击法将重组质粒转化到农杆菌GV3101中,瞬时转化烟草后进行荧光观察。 结果 克隆得到了84KTUA5和84KTUB16基因,成功与pCAMBIA 1300-mCherry载体连接,烟草瞬时表达荧光观察结果显示:仅目的基因与mCherry标签C’端相连的融合蛋白能够成功表达,且荧光明显。 结论 成功构建了84K杨TUA5和TUB16基因与pCAMBIA 1300-mCherry的融合表达载体,为进一步研究杨树微管功能提供了背景材料。 Abstract:Objective To lay the foundation for studying the microtubule function of poplar, plant overexpression vectors of 84K poplar by constructing the tubulin TUA5 and TUB16 fused with red fluorescent protein mCherry, and using transient expression to verify the fluorescent signal after vectors expressed in plant. Method Primers for TUA5 and TUB16 genes of 84K poplar were designed using TUA5 and TUB16 homologous gene sequences from Populus trichocarpa, RNA from wild type 84K poplar was extracted and reversely transcribed into cDNA, homologous cloning yield 84KTUA5 and 84KTUB16 genes, which were respectively linked to N’ and C’ terminal of the mCherry fluorescent tag from pCAMBIA 1300 vector, and then transformed into E.coli TOP10 competent cells.Positive monoclonal were conducted by means of colony PCR, and after sequencing identification, the recombinant plasmid was transformed into agrobacterium GV3101 by electrochemical reaction to transiently transformed into tobacco leaf, and then observed fluorescence excitated from mCherry. Result The 84KTUA5 and 84KTUB16 genes were cloned and successfully linked to pCAMBIA 1300-mCherry vector, fluorescence observation of tobacco transient expression showed that only the fusion protein of the target gene linked to the C' terminal can be successfully expressed, and the fluorescence was obvious. Conclusion The fusion expression vectors of TUA5 and TUB16 genes of 84K poplar and pCAMBIA 1300-mCherry were successfully constructed respectively, which provids background materials for further study of poplar microtubule function. -
Key words:
- tubulin
- / homologous recombination
- / vector construction
- / transient expression
-
表 1 84KTUA5和84KTUB16的引物
Table 1. The primers of 84KTUA5 and 84KTUB16
引物名称 Primer name 引物序列 Primer sequences (5' to 3') 同源克隆引物 84KTUA5-UTR F: ATAAACGTCTTCGCTCCTATTCTCC
R: TATTAGGCTACACCCATTACGAAGG84KTUA16-UTR F: TAACGCGAAACAAAAAATGAGAGAA
R: TCAAACACGAACACCAATACAAAACCherry N’端同源重组引物 84KTUA5-Cherry F: gcttcgaattctgcagtcgacATGAGAGAGTGCATTTCGATCCAC
R: atcccgggcccgcggtaccgCATGTACTCGTCACCATCATCATCA84KTUB16-Cherry F: gcttcgaattctgcagtcgacATGAGAGAAATCCTTCACGTTCAGG
R: atcccgggcccgcggtaccgCATCCCGGCAGCATCTTCTT连接肽PCR扩增引物 Linker-84KTUA5 F: AGGGAGGTGGAAGTGGAGGTAGCGGTATGAGAGAGTGCATTTCGATCCAC
R: TCACATGTACTCGTCACCATCATCALinker-84KTUB16 F: GGGAGGTGGAAGTGGAGGTAGCGGTATGAGAGAAATCCTTCACGTTCAGG
R: TTACATCCCGGCAGCATCTTCTTCherry C’端同源重组引物 Cherry-84KTUA5 F: ggcggcatggacgagctgtacaAGGGAGGTGGAAGTGGAGGTAG
R: attctagcccctagatcacttgtacaTCACATGTACTCGTCACCATCATCATCherry-84KTUB16 F: ggcggcatggacgagctgtacaAGGGAGGTGGAAGTGGAGGTAG
R: gcattctagcccctagatcacttgtacaTTACATCCCGGCAGCATCTTCT鉴定引物 Gene-Cherry F: acgagctcaagcttcgaattctg
R: caccttgaagcgcatgaactccCherry-Gene F: gactacaccatcgtggaacagtac
R: acgttgtaaaacgacggccagt表 2 序列同源性比对
Table 2. Sequences homology alignment %
Sequences Pt-TUA5 84K-TUA5 Pt-TUB16 84K-TUB16 Pt-TUA5 ID 98.80 50.50 50.30 84K-TUA5 98.80 ID 50.50 50.30 Pt-TUB16 50.50 50.50 ID 96.70 84K-TUB16 50.30 50.30 96.70 ID -
[1] Dutcher S K. The tubulin fraternity:alpha to eta[J]. Current Opinion in Cell Biology, 2001, 13(1): 49-54. doi: 10.1016/S0955-0674(00)00173-3 [2] Fosket D E, Morejohn L C. Structural and Functional Organization of Tubulin[J]. Annual Review of Plant Physiology & Plant Molecular Biology, 1992, 43(1): 201-240. [3] Snustad D P, Haas N A, Steven D.Kopczak, et al. The small genome of Arabidopsis contains at least nine expressed beta-tubulin genes[J]. Plant Cell, 1992, 4(5): 549-556. [4] Jeon J S, Lee S, Jung K H, et al. Tissue-preferential expression of a rice alpha-tubulin gene, OsTubA1, mediated by the first intron[J]. Plant Physiology, 2000, 123(3): 1005-1014. doi: 10.1104/pp.123.3.1005 [5] Yoshikawa M, Yang G, Kawaguchi K, et al. Expression Analyses of β-tubulin Isotype Genes in Rice[J]. Plant & Cell Physiology, 2003, 44(11): 1202-1207. [6] Oakley RV, Wang Y S, Ramakrishna W, et al. Differential expansion and expression of alpha- and beta-tubulin gene families in Populus[J]. Plant Physiology, 2007, 145(3): 961-973. doi: 10.1104/pp.107.107086 [7] Abe T, Thitamadee S, Hashimoto T. Microtubule defects and cell morphogenesis in the lefty1lefty2 tubulin mutant of Arabidopsis thaliana[J]. Plant & Cell Physiology, 2004, 45(2): 211-220. [8] 薛秀花, 任海云. 细胞骨架在植物细胞周期进程中的动态变化及其调控[J]. 北京师范大学学报:自然科学版, 2016, 52(6):687-695. [9] Storme N D, Copenhaver G P, Geelen D. Production of diploid male gametes in Arabidopsis by cold-induced destabilization of postmeiotic radial microtubule arrays[J]. Plant Physiology, 2012, 160(4): 1808-1826. doi: 10.1104/pp.112.208611 [10] Wang C, Li J, Yuan M. Salt tolerance requires cortical microtubule reorganization in Arabidopsis[J]. Plant & Cell Physiology, 2007, 48(11): 1534-1547. [11] Marcus A I, Moore R C, Cyr R J. The role of microtubules in guard cell function[J]. Plant Physiology, 2001, 125(1): 387-395. doi: 10.1104/pp.125.1.387 [12] Paredez A R, Somerville C R, Ehrhardt D W. Visualization of cellulose synthase demonstrates functional association with microtubules[J]. Science, 2006, 312(5779): 1491-1495. doi: 10.1126/science.1126551 [13] Eisinger W, Ehrhardt D, Briggs W. Microtubules are essential for guard-cell function in vicia and Arabidopsis[J]. Molecular Plant, 2012, 5(3): 601-610. doi: 10.1093/mp/sss002 [14] Abe T, Hashimoto T. Altered microtubule dynamics by expression of modified alpha-tubulin protein causes right-handed helical growth in transgenic Arabidopsis plants[J]. Plant Journal for Cell & Molecular Biology, 2005, 43(2): 191-204. [15] Sparkes IA, Runions J, Kearns A, et al. Rapid, transient expression of fluorescent fusion proteins in tobacco plants and generation of stably transformed plants[J]. Nature Protocols, 2006, 1(4): 2019-2025. doi: 10.1038/nprot.2006.286 [16] 周贤武, 高玉磊, 苏明垒, 等. 基因工程改良木材性质研究进展[J]. 林业科学, 2018, 54(3):152-160. [17] Gutierrez R, Lindeboom J J, Paredez A R, et al. Arabidopsis cortical microtubules position cellulose synthase delivery to the plasma membrane and interact with cellulose synthase trafficking compartments[J]. Nature Cell Biology, 2009, 11(7): 797-806. doi: 10.1038/ncb1886 [18] Huston J S, Levinson D, Mudgett-Hunter M, et al. Protein engineering of antibody binding sites:recovery of specific activity in an anti-digoxin single-chain Fv analogue produced in Escherichia coli[J]. Proceedings of the National Academy of Sciences of the United States of America, 1988, 85(16): 5879-5883. doi: 10.1073/pnas.85.16.5879 -





 下载:
下载: