-
油橄榄(Olea europaea L.)为木犀科(Oleaceae)木犀榄属(Olea L.)常绿乔木,是世界著名木本油料树种,主要分布于地中海地区,由其新鲜初熟或成熟果实冷榨而成的橄榄油,富含单不饱和脂肪酸和抗氧化物质,营养和保健功能越来越受到人们的认可[1-2]。
油橄榄为风䗋异花授粉,不同品种自交和杂交亲和性仍没有得到充分地研究和揭示,如对栽培品种“Moraiolo”和“Manzanillo”自交亲和性的研究,不同学者得出的结论完全相反[3]。Mekuria等[4]认为,实验条件不同甚至参试品种鉴定不准确或名称混淆,自交亲和性的研究都有可能出现截然不同的结果。人工套袋授粉,显微观察花粉管萌发、生长,统计坐果率,是油橄榄品种亲和性研究的常规方法[5-6],但这种方法很难避免外来花粉污染[7],袋内微环境的改变及果实自然脱落都会影响对套袋真实坐果率的判断[8]。采用分子标记方法进行亲和性分析准确性较高,其中,SSR标记具有共显性、高多态性的特点,在油橄榄遗传学研究中得到广泛应用[3,9-13]。
20世纪50年代以来,我国自国外引种油橄榄品种150多个,在甘肃、四川、重庆、云南等地推广种植,目前栽培面积近11万hm2,经济、生态和社会效益显著;然而,我国早期营建的很多油橄榄品种园缺乏明确的授粉品种配置技术,坐果率低、挂果少、产量低等现象较为普遍。甘肃武都油橄榄品种园是我国收集保存油橄榄种质资源较丰富的品种园,本研究以该品种园收集保存的114份油橄榄种质作为候选父本,选择园内4个主要栽培品种,利用SSR标记对品种子代的真实父本进行鉴定,分析品种亲和性,探索适宜的授粉品种,以期为油橄榄品种园中品种配置提供科学依据。
-
甘肃省陇南市武都地区自1978年开始引种油橄榄,1992年建立近7 hm2油橄榄丰产示范园[14]。目前,武都油橄榄品种园已收集、保存油橄榄种质114份(114份种质信息表略),包括油橄榄亚种尖叶木犀榄(O. europaea subsp. cuspidata (Wall. ex G. Don) Cif.)和变种金叶木犀榄(O. europaea subsp. cuspidata var. chrysophylla Lam.)。
品种园内不同种质材料混合种植,株行距约3 m×3 m,植株长势良好。选择“城固32”(“Chenggu 32”)、“豆果”(“Arbequina”)、“贺吉布兰克”(“Hojiblanca”)和“皮瓜尔”(“Picual”)4个主要栽培品种,于果实成熟期分别从不同品种植株中部的4个方位,随机采摘新鲜果实5颗以上,其中,“城固32”30颗,“豆果”25颗,“贺吉布兰克”20颗,“皮瓜尔”20颗。用自封袋将果实分装带回实验室,果肉自然软化后,去除果皮,剥出的种子保存在4℃冰箱中备用。
从每份种质的正常结实植株上采集新鲜叶片,立即装在样品袋中进行硅胶干燥,带回实验室于4℃冰箱中储藏备用。样品采集时,详细登记每份种质的原始名称、原产地和引种地等信息。原始记录名称缺失或不确定的27份种质,采用UC1、UC2、UC3、
$\cdots $ 、UC27进行编号。材料标本凭证保存于中国林业科学研究院林业研究所国家林业和草原局林木培育重点实验室。
-
叶片DNA提取:利用天根生化科技(北京)有限公司生产的植物基因组DNA提取试剂盒(DP305)提取油橄榄叶片全基因组DNA,操作参照说明书。
种胚DNA提取:使用同款DNA提取试剂盒,按照产品说明向GP1缓冲液中加入定量的β-巯基乙醇,65℃水浴备用。将油橄榄种子从硬质内果皮中剥离出,浸泡于65℃水中,去除种皮和胚乳,切取1/2种胚置于1.5 mL离心管中,加入约300 μL备用GP1缓冲液,利用TIANGEN-OSEY30高速组织研磨器研磨至样品完全粉碎,再向研磨样品加入备用GP1缓冲液约400 μL,轻摇混匀,置于65℃水浴锅中水浴40~60 min,期间每10 min取出重新混匀,后续操作参照说明书。
-
14对SSR引物根据文献[15-19]中记载的序列信息,由生工生物工程(上海)股份有限公司提供合成服务,其中,5′端分别用6-FAM、HEX、TMR和ROX荧光进行标记(表1)。
表 1 14对SSR引物序列信息
Table 1. Sequence information of the 14 SSR markers
位点Locus 引物序列Primer sequence (5′-3′) 重复单元Repeat motif 标记荧光Fluorescent ssrOeUA-DCA3 F:CCCAAGCGGAGGTGTATATTGTTAC (GT)19 6-FAM R:TGCTTTTGTCGTGTTTGAGATGTTG ssrOeUA-DCA9 F:AATCAAAGTCTTCCTTCTCATTTCG (GT)23 6-FAM R:GATCCTTCCAAAAGTATAACCTCTC ssrOeUA-DCA11 F:GATCAAACTACTGCACGAGAGAG (GA)26(GGGA)4 ROX R:TTGTCTCAGTGAACCCTTAAACC ssrOeUA-DCA15 F:GATCTTGTCTGTATATCCACAC (CA)3G(AC)14 6-FAM R:TATACCTTTTCCATCTTGACGC ssrOeUA-DCA16 F:TTAGGTGGGATTCTGTAGATGGTTG (GT)13(GA)29 HEX R:TTTTAGGTGAGTTCATAGAATTAGC DCA18 F:AAGAAAGAAAAAGGCAGAATTAAGC (CA)4(CT)1(CA)3(GA)19 TMR R:GTTTTCGTCTCTCTACATAAGTGAC UDO99-011 F:TGACTCCCTTTAAACTCATCAGG (CT)7(CA)10(CT)2(CA)2 2CT(CA)2CT(CA)9 6-FAM R:TGCGCATGTAGATGTGAATATG UDO99-019 F:TCCCTTGTAGCCTCGTCTTG (GT)20(AT)5 ROX R:GGCCTGATCATCGATACCTC UDO99-024 F:GGATTTATTAAAAGCAAAACATACAAA (CA)11(TA)2(CA)4 HEX R:CAATAACAAATGAGCATGATAAGACA UDO99-043 F:TCGGCTTTACAACCCATTTC (GT)12 TMR R:TGCCAATTATGGGGCTAACT GAPU59 F:CCCTGCTTTGGTCTTGCTAA (CT)9 ROX R:CAAAGGTGCACTTTCTCTCG GAPU71B F:GATCAAAGGAAGAAGGGGATAAA (AG)7(AAG)8 6-FAM R:ACAACAAATCCGTACGCTTG GAPU101 F:CATGAAAGGAGGGGGACATA (GA)8(GA)3(AG)3 HEX R:GGCACTTGTTGTGCAGATTG GAPU 103 F:TGAATTTAACTTTAAACCCACACA (TC)32 TMR R:GCATCGCTCGATTTTTATCC -
PCR扩增采用20 μL反应体系,包括7.9 μL ddH2O,10 μL PCR Mix(含DNA polymerase、dNTPs和Buffer),正反向引物(10 μmol·L−1)各0.8 μL,以及0.5 ng模板DNA。扩增程序:94℃预变性,4 min;94℃变性30 s,60℃左右退火30 s,72℃延伸2 min,10个循环;94℃变性30 s,55℃左右退火30 s,72℃延伸2 min,26个循环;72℃延伸10 min;10℃保存。退火温度因引物不同而异。使用ABI Veriti96 PCR仪进行PCR扩增,产物送北京擎科新业有限公司进行Sanger法测序。
-
采用GeneMapper 4.0软件(Applied Biosystems, Warrington, United Kingdom),按照使用说明书,设置参数,进行基因分型。分型的结果以Excel表格输出。
建立母本、候选父本(叶片)和子代(种胚)基因型数据库,使用Cervus 3.0软件计算等位基因频率、期望杂合度、观测杂合度、多态信息含量、哑等位基因以及非父排除概率等参数[20-21]。运行Simulation程序中的paternity子程序,输入等位基因频率分析文件,模拟10 000次亲子鉴定。运行Parentage Analysis程序中的paternity子程序,输入子代及候选父本基因型文件、等位基因频率分析和模拟分析文件,计算候选父本基因型似然对数比(LOD)值和不同置信水平(80%和95%)Delta值(最大和次大LOD值的差值),根据LOD值大小判定亲子关系。
-
4个油橄榄品种共采集果实95颗,种子败育现象在品种间普遍存在,“豆果”种子发育正常果实比例最高(96%),“贺吉布兰克”最低(70%)(表2)。
表 2 油橄榄不同品种果实种子发育情况
Table 2. Seed development of different olive cultivars
种质编号
Germplasm
number品种Cultivar 果实数量
Fruit
number/颗种子发育正常的果实数量
Number of fruits with
well-developed seeds/颗种子发育正常的果实比例
Proportion of fruits with
well-developed seeds/%具2粒发育正常种子
的果实数量
Number of bi-seeded
fruits/颗具2粒发育正常种子
的果实比例
Proportion of
bi-seeded fruits/%105 ‘豆果’‘Arbequina’ 25 24 96 0 0 108 ‘皮瓜尔’‘Picual’ 20 16 80 0 0 79 ‘城固32’‘Chenggu 32’ 30 26 87 3 10 106 ‘贺吉布兰克’‘Hojiblanca’ 20 14 70 5 25 油橄榄种子发育过程中,2个心皮内分别着生2个胚珠[22],后期通常只有1个胚珠发育成为种子[23]。通过对不同品种种子解剖发现,“城固32”和“贺吉布兰克”果实内具有2粒发育正常种子的现象(图1),其中,“贺吉布兰克”果实具2粒发育正常种子的比例达25%(表2)。
4个品种共获得88粒发育正常的种子,具2粒发育正常种子的仅取其中1粒,共剥离出80个种胚用于父本鉴定分析。
-
14个SSR位点的平均等位基因数16.1个(表3),其中,DCA9位点上的等位基因数目最多(29个),GAPU59位点上等位基因数目最少(8个),均满足利用SSR标记进行父本分析所需等位基因数要求[24]。UDO99-019位点132 bp的等位基因频率最高(0.645 9),而GAPU101位点194、216、245和247 bp的等位基因频率最低,均为0.002 6。
表 3 14个SSR位点等位基因及基因频率
Table 3. Number of alleles and allele frequencies of the 14 SSR loci
位点
Locus等位基因数
Number of alleles等位基因及其频率Allele and allele frequency DCA3 13 231(0.081 1);232(0.060 8);235(0.003 4);237(0.111 5);239(0.128 4);243(0.239 9);245(0.054 1);247(0.013 5);249(0.131 8);252(0.016 9);253(0.152 0);255(0.003 4);256(0.003 4) DCA9 29 123(0.002 8);144(0.002 8);157(0.002 8);158(0.002 8);159(0.005 5);162(0.287 3);163(0.002 8);165(0.024 9);169(0.002 8);172(0.124 3);175(0.013 8);177(0.002 8);179(0.002 8);181(0.049 7);182(0.002 8);183(0.138 1);185(0.019 3);187(0.002 8);191(0.035 9);193(0.071 8);195(0.005 5);201(0.011 0);203(0.030 4);205(0.127 1);207(0.016 6);209(0.002 8);211(0.002 8);217(0.002 8);221(0.002 8) DCA11 18 129(0.029 7);130(0.002 7);132(0.024 3);133(0.132 4);135(0.002 7);138(0.008 1);140(0.002 7);143(0.048 6);144(0.310 8);147(0.005 4);151(0.073 0);164(0.086 5);172(0.002 7);174(0.005 4);178(0.021 6);180(0.043 2);182(0.183 8);186(0.016 2) DCA15 13 238(0.002 8);243(0.002 8);244(0.041 4);245(0.447 5);246(0.002 8);247(0.013 8);250(0.002 8);255(0.013 8);262(0.016 6);263(0.008 3);264(0.433 7);266(0.002 8);267(0.011 0) DCA16 21 122(0.154 9);123(0.097 8);126(0.002 7);132(0.002 7);144(0.002 7);146(0.024 5);149(0.203 8);152(0.005 4);155(0.171 2);156(0.027 2);157(0.010 9);162(0.057 1);165(0.002 7);171(0.019 0);174(0.179 3);176(0.013 6);177(0.002 7);181(0.002 7);199(0.008 2);201(0.005 4);205(0.005 4); DCA18 15 162(0.023 9);163(0.005 3);165(0.013 3);166(0.005 3);169(0.087 8);170(0.143 6);172(0.122 3);174(0.016 0);176(0.255 3);178(0.199 5);180(0.087 8);184(0.018 6);186(0.002 7);187(0.013 3);197(0.005 3) UDO99-011 19 92(0.066 3);100(0.008 3);101(0.265 2);102(0.069 1);103(0.002 8);104(0.005 5);109(0.011 0);110(0.140 9);112(0.071 8);114(0.163 0);117(0.016 6);120(0.074 6);121(0.030 4);123(0.019 3);126(0.027 6);127(0.019 3);128(0.002 8);142(0.002 8);151(0.002 8) UDO99-019 11 98(0.013 5);101(0.008 1);102(0.140 5);132(0.645 9);133(0.027 0);146(0.002 7);147(0.002 7);155(0.002 7);158(0.054 1);164(0.002 7);170(0.100 0); UDO99-024 11 163(0.012 1);166(0.087 9);170(0.030 3);171(0.048 5);178(0.063 6);180(0.078 8);184(0.060 6);185(0.009 1);186(0.533 3);188(0.024 2);202(0.051 5) UDO99-043 21 135(0.332 4);145(0.002 7);146(0.324 3);153(0.002 7);160(0.013 5);161(0.118 9);162(0.086 5);175(0.008 1);176(0.032 4);179(0.016 2);182(0.002 7);183(0.005 4);185(0.002 7);186(0.008 1);206(0.005 4);210(0.002 7);212(0.010 8);214(0.008 1);216(0.002 7);219(0.010 8 );221(0.002 7); GAPU59 8 209(0.174 9);214(0.412 6);218(0.010 9);219(0.265 0);222(0.019 1);224(0.103 8);230(0.002 7);241(0.010 9); GAPU71B 10 114(0.010 9);116(0.002 7);117(0.144 8);120(0.316 9);122(0.106 6);123(0.038 3);126(0.109 3);129(0.002 7);134(0.002 7);140(0.26 5) GAPU101 13 184(0.128 9);190(0.034 2);192(0.157 9);194(0.002 6);196(0.007 9);198(0.181 6);200(0.250 0);204(0.005 3);206(0.118 4);216(0.002 6);218(0.105 3);245(0.002 6);247(0.002 6) GAPU103 23 120(0.009 2);122(0.006 1);137(0.082 8);140(0.009 2);152(0.064 4);159(0.003 1);161(0.070 6);162(0.009 2);164(0.042 9);166(0.003 1);170(0.006 1);174(0.033 7);176(0.138 0);178(0.033 7);184(0.061 3);188(0.024 5);190(0.012 3);192(0.095 1);198(0.122 7);199(0.036 8);206(0.052 1);212(0.064 4);245(0.018 4) -
14个SSR位点的观测杂合度(Ho)和期望杂合度(He)均值分别为0.788 0和0.786 3,变异范围分别为0.514 0~0.995 0和0.551 0~0.926 0(表4)。Ho和He均值相近,表明油橄榄品种受选择及近交等因素的影响较小;平均杂合度较高,表明油橄榄品种遗传变异大,环境适应能力强。
表 4 14个SSR位点在群体中的多态性检测
Table 4. Polymorphic information of the 14 SSR loci in the population
位点Locus 个体数Number of individuals 观测杂合度Observed heterozygosity (Ho) 期望杂合度Expected heterozygosity (He) 多态信息含量Polymorphism information content (PIC) 哑等位基因概率Null allele frequency DCA3 148 0.838 0 0.862 0 0.844 0 0.008 5 DCA9 181 0.901 0 0.858 0 0.842 0 −0.029 6 DCA11 185 0.816 0 0.835 0 0.816 0 0.009 8 DCA15 181 0.514 0 0.611 0 0.532 0 0.072 7 DCA16 184 0.734 0 0.860 0 0.842 0 0.078 2 DCA18 188 0.872 0 0.845 0 0.824 0 −0.015 8 UDO991-11 181 0.856 0 0.863 0 0.847 0 −0.002 0 UDO99-019 185 0.584 0 0.551 0 0.520 0 −0.034 1 UDO99-024 165 0.618 0 0.689 0 0.670 0 0.023 2 UDO99-043 185 0.995 0 0.763 0 0.727 0 −0.149 1 GAPU59 183 0.628 0 0.720 0 0.673 0 0.064 0 GAPU71B 183 0.891 0 0.786 0 0.752 0 −0.067 8 GAPU101 190 0.895 0 0.839 0 0.816 0 −0.032 9 GAPU103 163 0.890 0 0.926 0 0.918 0 0.017 2 均值Mean 179 0.788 0 0.786 3 0.758 8 - 注:“-”表示无数据。下同。
Note:No data are reported by “-”. The same below. -
通常认为,多态信息含量(PIC)>0.500 0时位点为高度多态,0.250 0<PIC<0.500 0时位点为中度多态,PIC<0.250 0时则为低度多态位点[25]。14个SSR位点的PIC值均大于0.500 0(表4),均为高度多态位点。平均多态信息含量为0.758 8,其中,UDO99-019位点最低(0.520 0),GAPU103位点最高(0.918 0)。14个SSR位点具有丰富的多态性,能够为研究提供足够的多态信息。
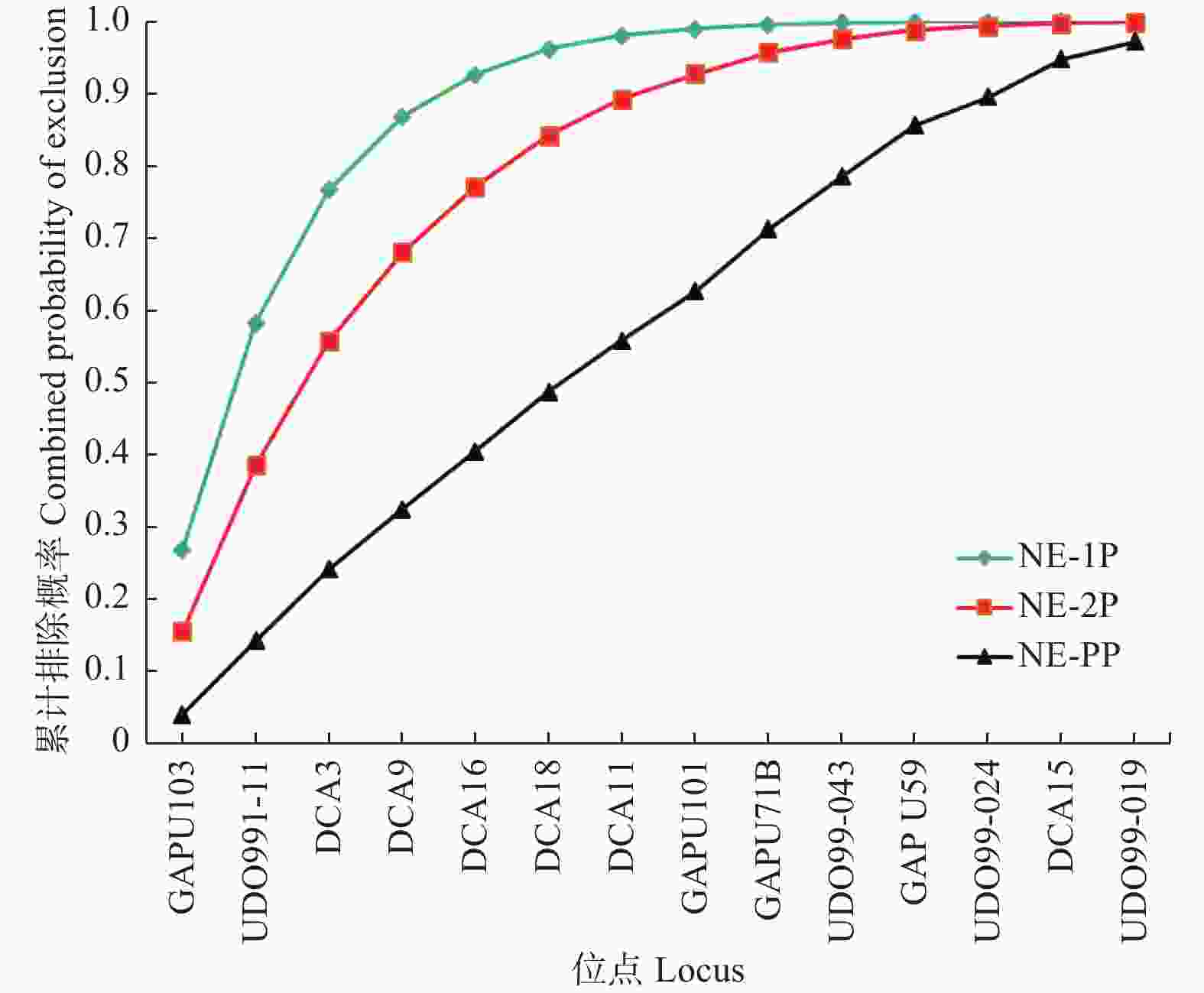
当双亲基因型皆未知时,单个SSR位点的非父排除概率(NE-1P)变化范围为0.268~0.827,均值0.550;当一个亲本基因型已知时,单个SSR位点的非父排除概率(NE-2P)变化范围为0.155~0.664,均值0.387;当双亲基因型已知时,单个SSR位点的非父排除概率(NE-PP)变化范围为0.040~0.504,均值0.212(表5)。
表 5 14个SSR位点的非父排除概率
Table 5. Non-exclusion probability of the 14 SSR loci
位点Locus 亲本基因型未知的非父排除概率Average non-exclusion probability for one candidate parent (NE-1P) 已知一个亲本基因型的非父排除概率Average non-exclusion probability for one candidate parent given the genotype of a known parent of the opposite sex (NE-2P) 双亲基因型已知的非父排除概率Average non-exclusion probability for a candidate parent pair (NE-PP) GAPU103 0.268 0.155 0.040 UDO991-11 0.429 0.272 0.106 DCA3 0.441 0.280 0.116 DCA9 0.437 0.278 0.109 DCA16 0.444 0.284 0.119 DCA18 0.477 0.311 0.139 DCA11 0.487 0.319 0.139 GAPU101 0.497 0.326 0.153 GAPU71B 0.595 0.417 0.231 UDO99-043 0.621 0.443 0.252 GAPU59 0.694 0.519 0.334 UDO99-024 0.684 0.491 0.269 DCA15 0.799 0.664 0.504 UDO99-019 0.827 0.653 0.460 均值Mean 0.550 0.387 0.212 依据PIC值由高至低依次累积计算14个SSR位点的排除概率,随着SSR位点数增加,累积排除概率增大(图2)。对于单亲已知类NE-2P,基于前9个SSR位点累积排除概率0.958,基于前12个SSR位点累积排除概率0.994,而基于全部14个SSR位点累积排除概率高达0.999。
-
哑等位基因影响遗传分析结果,数据处理时需要将哑等位基因频率偏高的位点删除[26]。对14个SSR位点哑等位基因的检测结果表明,各位点均存在一定的哑等位基因,但频率较低,均小于0.080 0(表4),可用于亲本鉴定分析[26]。
-
在置信度80%水平,4个品种共计29个子代鉴定出候选父本(表6),其中“城固32”13个(鉴定率50%),“豆果”7个(鉴定率29%),“贺吉布兰克”5个(鉴定率36%),“皮瓜尔”4个(鉴定率25%)。
表 6 油橄榄4个品种子代父本分析结果
Table 6. Paternity analysis result of the four olive cultivars progenies
子代编号
Progeny
number母本编号
Female parent
number母本名称
Female parent
name候选父本编号
Candidate paternal
parent number候选父本名称
Candidate paternal
parent nameLOD值
Trio LOD
scoreDelta值
Trio
Delta置信度
Trio
confidence79-1 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 5.79E+00 5.79E+00 * 79-2 79 ‘城固32’‘Chenggu 32’ 107 ‘科尼卡’‘Cornicabra’ 3.53E+00 3.53E+00 * 79-4 79 ‘城固32’‘Chenggu 32’ 100 ‘云台14’‘Yuntai 14’ 3.18E+00 3.16E+00 * 79-6 79 ‘城固32’‘Chenggu 32’ 16 ‘城固32’‘Chenggu 32’ 1.02E+00 7.32E-01 + 79-14 79 ‘城固32’‘Chenggu 32’ 106 ‘贺吉布兰克’‘Hojiblanca’ 3.71E+00 3.71E+00 * 79-15 79 ‘城固32’‘Chenggu 32’ UC5 - 1.65E+00 1.65E+00 * 79-18 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 3.41E+00 3.41E+00 * 79-21 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 1.60E+00 1.60E+00 * 79-24 79 ‘城固32’‘Chenggu 32’ UC17 - 4.09E+00 8.97E-01 + 79-26 79 ‘城固32’‘Chenggu 32’ 9 ‘莱星’‘Leccino’ 3.87E+00 6.74E-01 + 79-27 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 4.28E+00 4.28E+00 * 79-28 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 1.17E+00 1.17E+00 * 79-29 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 4.99E+00 4.99E+00 * 105-4 105 ‘豆果’‘Arbequina’ 109 ‘小苹果’‘Manzanilia’ 2.91E+00 2.79E+00 * 105-5 105 ‘豆果’‘Arbequina’ 53 ‘小苹果·塞维利亚’‘Manzanilia De Sevilla’ 1.34E+00 1.34E+00 * 105-10 105 ‘豆果’‘Arbequina’ 104 ‘小苹果’‘Manzanilia’ 3.81E+00 1.30E+00 * 105-14 105 ‘豆果’‘Arbequina’ 36 ‘配多灵’‘Pendolino’ 3.20E-01 3.20E-01 + 105-16 105 ‘豆果’‘Arbequina’ 5 ‘城固32’‘Chenggu 32’ 2.87E+00 2.87E+00 * 105-19 105 ‘豆果’‘Arbequina’ 104 ‘小苹果’‘Manzanilia’ 1.20E+00 1.20E+00 * 105-20 105 ‘豆果’‘Arbequina’ 104 ‘小苹果’‘Manzanilia’ 3.62E+00 3.62E+00 * 106-2 106 ‘贺吉布兰克’‘Hojiblanca’ 98 金叶木犀榄O. europaea subsp. cuspidata var. chrysophylla 2.12E-01 2.12E-01 + 106-4 106 ‘贺吉布兰克’‘Hojiblanca’ 104 ‘小苹果’‘Manzanilia’ 3.25E+00 3.39E-01 + 106-6 106 ‘贺吉布兰克’‘Hojiblanca’ 104 ‘小苹果’‘Manzanilia’ 1.48E+00 5.75E-01 + 106-7 106 ‘贺吉布兰克’‘Hojiblanca’ 101 ‘阿尔波萨纳’‘Arbosana’ 8.28E-01 8.28E-01 + 106-13 106 ‘贺吉布兰克’‘Hojiblanca’ 53 ‘小苹果·塞维利亚’‘Manzanilia De Sevilla’ 2.86E+00 2.86E+00 * 108-1 108 ‘皮瓜尔’‘Picual’ 105 ‘豆果’‘Arbequina’ 5.36E+00 5.36E+00 * 108-6 108 ‘皮瓜尔’‘Picual’ 105 ‘豆果’‘Arbequina’ 1.43E+00 1.43E+00 * 108-9 108 ‘皮瓜尔’‘Picual’ 106 ‘贺吉布兰克’‘Hojiblanca’ 3.86E+00 1.03E+00 + 108-13 108 ‘皮瓜尔’‘Picual’ 101 ‘阿尔波萨纳’‘Arbosana’ 1.10E+00 1.10E+00 + 注:*代表置信度为95%;+代表置信度为80%。
Notes: * represents a 95% confidence level; + represents a 80% confidence level.在置信度95%水平,“城固32”、“豆果”和“皮瓜尔”子代主要候选父本分别为“豆果”(占60%)、“小苹果”(占67%)以及“豆果”(占100%),而“贺吉布兰克”子代鉴定出的候选父本仅1个,为“小苹果·塞维利亚”。
-
多态信息含量(PIC)是衡量基因丰富度的重要指标,等位基因越多,多态性越丰富。本研究中,14个SSR位点PIC均值0.758 8,多态性高,哑等位基因频率检测结果也表明各SSR位点可用于油橄榄品种子代的父本分析。基于遗传排除法(Genetic exclusion)[27]和Cervus 3.0软件[28-30],利用这14个SSR标记对我国甘肃武都油橄榄品种园“城固32”、“豆果”、“贺吉布兰克”以及“皮瓜尔”4个主要栽培品种子代进行父本分析,检测各子代与候选父本之间的亲缘关系,在单亲基因型已知下,累积排除概率高达99%,可认为候选父本和子代间的亲子关系成立。通过比较子代、母本和候选父本的基因型,计算每个候选父本的LOD值,从候选父本中为部分子代鉴定出真实亲本。
对油橄榄4个品种80个子代父本分析结果表明,在80%置信水平可为29个子代确定候选父本,即花粉来源,鉴定率与其他学者对油松(Pinus tabulaeformis Carr.)[31]、马尾松(P. massoniana Lamb.)[32]、青冈(Cyclobalanopsis glauca (Thunb.) Oerst.)[33]等树种的研究结果相似。
4个油橄榄品种的子代检测出的候选父本相对集中,共14个品种,仅占全部候选父本的12%,表明品种园内仅有少数品种的花粉对子代的贡献较大。何田华等[34]认为,利用排除法进行亲本分析时,群体中候选亲本数量不宜大于100,否则很难为大多数子代确定亲本来源。本研究中,候选父本多达114个,这可能是只有少部分子代的父本被鉴定出的原因之一,而不同品种间的花期同步性、品种园内小区块的品种配置等因素可能也会影响对子代花粉来源的分析和鉴定,需要在今后研究中予以关注。
油橄榄多数品种存在自交不亲和现象[4],对品种自交亲和性和品种间杂交亲和性的研究结果受环境条件等因素的影响[35]。本研究中,4个油橄榄品种仅在“城固32”子代中检测到来自品种自身的花粉,表明“城固32”具有自交亲和性,王笑山等[36]对陕西城固油橄榄园主要品种自花授粉坐果率的研究也表明“城固32”具有一定的自交结实能力。“豆果”、“贺吉布兰克”和“皮瓜尔”子代没有检测到品种自身花粉,为自交不亲和品种。其它学者对我国四川凉山州[13]、意大利西西里岛[35,37]油橄榄品种亲和性的研究结果也表明“豆果”自交不亲和。
“城固32”子代候选父本60%为“豆果”(置信度95%),表明“豆果”是其主要的花粉贡献品种。同时,在“豆果”子代候选父本中检测出“城固32”(置信度95%),表明这2个品种可互相作为授粉品种,这与对四川凉山州油橄榄品种适配性的研究结果一致[13]。此外,在“豆果”和“贺吉布兰克”的子代候选父本中,“小苹果”的比例分别为57%和40%(置信度80%及95%),表明可以将“小苹果”作为“豆果”和“贺吉布兰克”建园的共同授粉品种。另外,“贺吉布兰克”子代候选父本中检测出油橄榄变种金叶木犀榄(置信度80%),表明以金叶木犀榄为父本,对“贺吉布兰克”实施杂交制种和遗传改良具有可行性。
研究发现“城固32”和“贺吉布兰克”果实内具有2粒发育正常的种子,且在后者果实中的比例达25%,而“豆果”和“皮瓜尔”果实内仅有1粒发育正常的种子。Cuevas等[23]研究表明,“贺吉布兰克”果实(14%)中同样具有2粒发育正常的种子,“皮瓜尔”中没有此现象,但在“豆果”中发现了少量果实(4%)具2粒发育正常的种子。Farinelli等[37]研究表明,在一些油橄榄品种中,具2粒发育正常种子的果实比仅2粒种子的果实大。因此,今后应加强对果实具2粒发育正常种子品种的研究,比较具2粒种子与1粒种子果实的表型差异,通过父本分析确定花粉来源,继而探索授粉品种对油橄榄果实种子发育的影响。
-
本研究将我国甘肃武都油橄榄品种园114份种质作为候选父本,利用14个SSR标记对园内4个主要栽培品种“城固32”、“豆果”、“贺吉布兰克”和“皮瓜尔”的子代进行父本分析,结果表明14个SSR位点均为高多态性位点,对于单亲已知类NE-2P,其累积排除概率高达0.999,这为油橄榄品种子代父本鉴定提供了重要的遗传标记选择。经检测,“城固32”和“皮瓜尔”子代的主要父本为“豆果”,而“豆果”和“贺吉布兰克”子代的主要父本为“小苹果”,同时,4个品种仅“城固32”具有一定的自交亲和性,这为今后油橄榄建园时的品种配置设计提供了基础依据。
基于SSR标记的油橄榄主要栽培品种子代父本分析
Paternity Analysis of Main Olive Cultivars Progenies Based on SSR Markers
-
摘要:
目的 对我国甘肃武都油橄榄品种园主要栽培品种子代进行父本分析,鉴定真实父本,探讨品种亲和性,为品种园授粉品种的选择提供科学依据。 方法 以武都油橄榄品种园114份种质为候选父本,基于14对SSR荧光标记,利用Cervus 3.0软件检测亲本分析相关参数,对‘城固32’、‘豆果’、‘贺吉布兰克’和‘皮瓜尔’4个主要栽培品种子代进行真实父本鉴定。 结果 14个SSR位点多态性高,累积排除概率随位点数增加而增大。对于单亲已知类非父排除概率(NE-2P),14个位点的累积排除概率高达0.999。通过比较子代、母本和候选父本的基因型,计算出每个候选父本的似然对数比,即LOD值,对油橄榄4个品种部分子代真实父本进行鉴定,其中‘城固32’和‘皮瓜尔’子代的主要父本为‘豆果’,‘豆果’和‘贺吉布兰克’子代的主要父本为‘小苹果’。 结论 所选高多态性和高累积排除概率的SSR位点适用于对油橄榄品种子代进行父本分析,为4个品种部分子代鉴定出真实父本,其中仅‘城固32’具有一定的自交亲和性,这为品种建园时授粉品种的选择和配置提供重要依据。 Abstract:Objective Paternity analysis of main olive cultivars progenies in Wudu Olive Orchard from Gansu province was carried out to identify the true paternal parent, explore the compatibility, and provide references for the selection of pollination cultivars in the orchard. Method 114 germplasm accessions from Wudu Olive Orchard were used as candidate paternal parents. Based on 14 pairs of fluorescence-labelled SSR markers, Cervus software was used to detect the parameters. True paternal parent identification of the four cultivars progenies (‘Chenggu 32’, ‘Arbequina’, ‘Hojiblanca’ and ‘Picual’) was performed. Result The 14 SSR loci were highly polymorphic and the cumulative exclusion probability increased with the number of loci. For the single parent known type NE-2P, the cumulative exclusion probability of the 14 loci was as high as 0.999. By comparing the genotypes of the progeny, the female parent and the candidate paternal parent, the LOD (log of likelihood ratio) values of each candidate paternal parent were calculated, and the identification of the true paternal parents of the partial progenies of the four cultivars was completed. The main paternal parent of the ‘Chenggu 32’ and ‘Picual’ progenies was ‘Arbequina’, while the main paternal parent of the ‘Arbequina’ and ‘Hojiblanca’ progenies was ‘Manzanilla’. Conclusion The SSR loci with characteristics of high polymorphism and high cumulative exclusion probability selected in the study are suitable for paternity analysis of olive cultivars progenies. The true paternal parents were identified for some of the four cultivars progenies and only ‘Chenggu 32’ among the four cultivars shows a certain self-compatibility, which provide important basis for the selection and configuration of pollination cultivars in the future orchard establishment. -
Key words:
- olive
- / cultivar
- / progeny
- / paternity analysis
- / SSR markers
-
表 1 14对SSR引物序列信息
Table 1. Sequence information of the 14 SSR markers
位点Locus 引物序列Primer sequence (5′-3′) 重复单元Repeat motif 标记荧光Fluorescent ssrOeUA-DCA3 F:CCCAAGCGGAGGTGTATATTGTTAC (GT)19 6-FAM R:TGCTTTTGTCGTGTTTGAGATGTTG ssrOeUA-DCA9 F:AATCAAAGTCTTCCTTCTCATTTCG (GT)23 6-FAM R:GATCCTTCCAAAAGTATAACCTCTC ssrOeUA-DCA11 F:GATCAAACTACTGCACGAGAGAG (GA)26(GGGA)4 ROX R:TTGTCTCAGTGAACCCTTAAACC ssrOeUA-DCA15 F:GATCTTGTCTGTATATCCACAC (CA)3G(AC)14 6-FAM R:TATACCTTTTCCATCTTGACGC ssrOeUA-DCA16 F:TTAGGTGGGATTCTGTAGATGGTTG (GT)13(GA)29 HEX R:TTTTAGGTGAGTTCATAGAATTAGC DCA18 F:AAGAAAGAAAAAGGCAGAATTAAGC (CA)4(CT)1(CA)3(GA)19 TMR R:GTTTTCGTCTCTCTACATAAGTGAC UDO99-011 F:TGACTCCCTTTAAACTCATCAGG (CT)7(CA)10(CT)2(CA)2 2CT(CA)2CT(CA)9 6-FAM R:TGCGCATGTAGATGTGAATATG UDO99-019 F:TCCCTTGTAGCCTCGTCTTG (GT)20(AT)5 ROX R:GGCCTGATCATCGATACCTC UDO99-024 F:GGATTTATTAAAAGCAAAACATACAAA (CA)11(TA)2(CA)4 HEX R:CAATAACAAATGAGCATGATAAGACA UDO99-043 F:TCGGCTTTACAACCCATTTC (GT)12 TMR R:TGCCAATTATGGGGCTAACT GAPU59 F:CCCTGCTTTGGTCTTGCTAA (CT)9 ROX R:CAAAGGTGCACTTTCTCTCG GAPU71B F:GATCAAAGGAAGAAGGGGATAAA (AG)7(AAG)8 6-FAM R:ACAACAAATCCGTACGCTTG GAPU101 F:CATGAAAGGAGGGGGACATA (GA)8(GA)3(AG)3 HEX R:GGCACTTGTTGTGCAGATTG GAPU 103 F:TGAATTTAACTTTAAACCCACACA (TC)32 TMR R:GCATCGCTCGATTTTTATCC 表 2 油橄榄不同品种果实种子发育情况
Table 2. Seed development of different olive cultivars
种质编号
Germplasm
number品种Cultivar 果实数量
Fruit
number/颗种子发育正常的果实数量
Number of fruits with
well-developed seeds/颗种子发育正常的果实比例
Proportion of fruits with
well-developed seeds/%具2粒发育正常种子
的果实数量
Number of bi-seeded
fruits/颗具2粒发育正常种子
的果实比例
Proportion of
bi-seeded fruits/%105 ‘豆果’‘Arbequina’ 25 24 96 0 0 108 ‘皮瓜尔’‘Picual’ 20 16 80 0 0 79 ‘城固32’‘Chenggu 32’ 30 26 87 3 10 106 ‘贺吉布兰克’‘Hojiblanca’ 20 14 70 5 25 表 3 14个SSR位点等位基因及基因频率
Table 3. Number of alleles and allele frequencies of the 14 SSR loci
位点
Locus等位基因数
Number of alleles等位基因及其频率Allele and allele frequency DCA3 13 231(0.081 1);232(0.060 8);235(0.003 4);237(0.111 5);239(0.128 4);243(0.239 9);245(0.054 1);247(0.013 5);249(0.131 8);252(0.016 9);253(0.152 0);255(0.003 4);256(0.003 4) DCA9 29 123(0.002 8);144(0.002 8);157(0.002 8);158(0.002 8);159(0.005 5);162(0.287 3);163(0.002 8);165(0.024 9);169(0.002 8);172(0.124 3);175(0.013 8);177(0.002 8);179(0.002 8);181(0.049 7);182(0.002 8);183(0.138 1);185(0.019 3);187(0.002 8);191(0.035 9);193(0.071 8);195(0.005 5);201(0.011 0);203(0.030 4);205(0.127 1);207(0.016 6);209(0.002 8);211(0.002 8);217(0.002 8);221(0.002 8) DCA11 18 129(0.029 7);130(0.002 7);132(0.024 3);133(0.132 4);135(0.002 7);138(0.008 1);140(0.002 7);143(0.048 6);144(0.310 8);147(0.005 4);151(0.073 0);164(0.086 5);172(0.002 7);174(0.005 4);178(0.021 6);180(0.043 2);182(0.183 8);186(0.016 2) DCA15 13 238(0.002 8);243(0.002 8);244(0.041 4);245(0.447 5);246(0.002 8);247(0.013 8);250(0.002 8);255(0.013 8);262(0.016 6);263(0.008 3);264(0.433 7);266(0.002 8);267(0.011 0) DCA16 21 122(0.154 9);123(0.097 8);126(0.002 7);132(0.002 7);144(0.002 7);146(0.024 5);149(0.203 8);152(0.005 4);155(0.171 2);156(0.027 2);157(0.010 9);162(0.057 1);165(0.002 7);171(0.019 0);174(0.179 3);176(0.013 6);177(0.002 7);181(0.002 7);199(0.008 2);201(0.005 4);205(0.005 4); DCA18 15 162(0.023 9);163(0.005 3);165(0.013 3);166(0.005 3);169(0.087 8);170(0.143 6);172(0.122 3);174(0.016 0);176(0.255 3);178(0.199 5);180(0.087 8);184(0.018 6);186(0.002 7);187(0.013 3);197(0.005 3) UDO99-011 19 92(0.066 3);100(0.008 3);101(0.265 2);102(0.069 1);103(0.002 8);104(0.005 5);109(0.011 0);110(0.140 9);112(0.071 8);114(0.163 0);117(0.016 6);120(0.074 6);121(0.030 4);123(0.019 3);126(0.027 6);127(0.019 3);128(0.002 8);142(0.002 8);151(0.002 8) UDO99-019 11 98(0.013 5);101(0.008 1);102(0.140 5);132(0.645 9);133(0.027 0);146(0.002 7);147(0.002 7);155(0.002 7);158(0.054 1);164(0.002 7);170(0.100 0); UDO99-024 11 163(0.012 1);166(0.087 9);170(0.030 3);171(0.048 5);178(0.063 6);180(0.078 8);184(0.060 6);185(0.009 1);186(0.533 3);188(0.024 2);202(0.051 5) UDO99-043 21 135(0.332 4);145(0.002 7);146(0.324 3);153(0.002 7);160(0.013 5);161(0.118 9);162(0.086 5);175(0.008 1);176(0.032 4);179(0.016 2);182(0.002 7);183(0.005 4);185(0.002 7);186(0.008 1);206(0.005 4);210(0.002 7);212(0.010 8);214(0.008 1);216(0.002 7);219(0.010 8 );221(0.002 7); GAPU59 8 209(0.174 9);214(0.412 6);218(0.010 9);219(0.265 0);222(0.019 1);224(0.103 8);230(0.002 7);241(0.010 9); GAPU71B 10 114(0.010 9);116(0.002 7);117(0.144 8);120(0.316 9);122(0.106 6);123(0.038 3);126(0.109 3);129(0.002 7);134(0.002 7);140(0.26 5) GAPU101 13 184(0.128 9);190(0.034 2);192(0.157 9);194(0.002 6);196(0.007 9);198(0.181 6);200(0.250 0);204(0.005 3);206(0.118 4);216(0.002 6);218(0.105 3);245(0.002 6);247(0.002 6) GAPU103 23 120(0.009 2);122(0.006 1);137(0.082 8);140(0.009 2);152(0.064 4);159(0.003 1);161(0.070 6);162(0.009 2);164(0.042 9);166(0.003 1);170(0.006 1);174(0.033 7);176(0.138 0);178(0.033 7);184(0.061 3);188(0.024 5);190(0.012 3);192(0.095 1);198(0.122 7);199(0.036 8);206(0.052 1);212(0.064 4);245(0.018 4) 表 4 14个SSR位点在群体中的多态性检测
Table 4. Polymorphic information of the 14 SSR loci in the population
位点Locus 个体数Number of individuals 观测杂合度Observed heterozygosity (Ho) 期望杂合度Expected heterozygosity (He) 多态信息含量Polymorphism information content (PIC) 哑等位基因概率Null allele frequency DCA3 148 0.838 0 0.862 0 0.844 0 0.008 5 DCA9 181 0.901 0 0.858 0 0.842 0 −0.029 6 DCA11 185 0.816 0 0.835 0 0.816 0 0.009 8 DCA15 181 0.514 0 0.611 0 0.532 0 0.072 7 DCA16 184 0.734 0 0.860 0 0.842 0 0.078 2 DCA18 188 0.872 0 0.845 0 0.824 0 −0.015 8 UDO991-11 181 0.856 0 0.863 0 0.847 0 −0.002 0 UDO99-019 185 0.584 0 0.551 0 0.520 0 −0.034 1 UDO99-024 165 0.618 0 0.689 0 0.670 0 0.023 2 UDO99-043 185 0.995 0 0.763 0 0.727 0 −0.149 1 GAPU59 183 0.628 0 0.720 0 0.673 0 0.064 0 GAPU71B 183 0.891 0 0.786 0 0.752 0 −0.067 8 GAPU101 190 0.895 0 0.839 0 0.816 0 −0.032 9 GAPU103 163 0.890 0 0.926 0 0.918 0 0.017 2 均值Mean 179 0.788 0 0.786 3 0.758 8 - 注:“-”表示无数据。下同。
Note:No data are reported by “-”. The same below.表 5 14个SSR位点的非父排除概率
Table 5. Non-exclusion probability of the 14 SSR loci
位点Locus 亲本基因型未知的非父排除概率Average non-exclusion probability for one candidate parent (NE-1P) 已知一个亲本基因型的非父排除概率Average non-exclusion probability for one candidate parent given the genotype of a known parent of the opposite sex (NE-2P) 双亲基因型已知的非父排除概率Average non-exclusion probability for a candidate parent pair (NE-PP) GAPU103 0.268 0.155 0.040 UDO991-11 0.429 0.272 0.106 DCA3 0.441 0.280 0.116 DCA9 0.437 0.278 0.109 DCA16 0.444 0.284 0.119 DCA18 0.477 0.311 0.139 DCA11 0.487 0.319 0.139 GAPU101 0.497 0.326 0.153 GAPU71B 0.595 0.417 0.231 UDO99-043 0.621 0.443 0.252 GAPU59 0.694 0.519 0.334 UDO99-024 0.684 0.491 0.269 DCA15 0.799 0.664 0.504 UDO99-019 0.827 0.653 0.460 均值Mean 0.550 0.387 0.212 表 6 油橄榄4个品种子代父本分析结果
Table 6. Paternity analysis result of the four olive cultivars progenies
子代编号
Progeny
number母本编号
Female parent
number母本名称
Female parent
name候选父本编号
Candidate paternal
parent number候选父本名称
Candidate paternal
parent nameLOD值
Trio LOD
scoreDelta值
Trio
Delta置信度
Trio
confidence79-1 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 5.79E+00 5.79E+00 * 79-2 79 ‘城固32’‘Chenggu 32’ 107 ‘科尼卡’‘Cornicabra’ 3.53E+00 3.53E+00 * 79-4 79 ‘城固32’‘Chenggu 32’ 100 ‘云台14’‘Yuntai 14’ 3.18E+00 3.16E+00 * 79-6 79 ‘城固32’‘Chenggu 32’ 16 ‘城固32’‘Chenggu 32’ 1.02E+00 7.32E-01 + 79-14 79 ‘城固32’‘Chenggu 32’ 106 ‘贺吉布兰克’‘Hojiblanca’ 3.71E+00 3.71E+00 * 79-15 79 ‘城固32’‘Chenggu 32’ UC5 - 1.65E+00 1.65E+00 * 79-18 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 3.41E+00 3.41E+00 * 79-21 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 1.60E+00 1.60E+00 * 79-24 79 ‘城固32’‘Chenggu 32’ UC17 - 4.09E+00 8.97E-01 + 79-26 79 ‘城固32’‘Chenggu 32’ 9 ‘莱星’‘Leccino’ 3.87E+00 6.74E-01 + 79-27 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 4.28E+00 4.28E+00 * 79-28 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 1.17E+00 1.17E+00 * 79-29 79 ‘城固32’‘Chenggu 32’ 105 ‘豆果’‘Arbequina’ 4.99E+00 4.99E+00 * 105-4 105 ‘豆果’‘Arbequina’ 109 ‘小苹果’‘Manzanilia’ 2.91E+00 2.79E+00 * 105-5 105 ‘豆果’‘Arbequina’ 53 ‘小苹果·塞维利亚’‘Manzanilia De Sevilla’ 1.34E+00 1.34E+00 * 105-10 105 ‘豆果’‘Arbequina’ 104 ‘小苹果’‘Manzanilia’ 3.81E+00 1.30E+00 * 105-14 105 ‘豆果’‘Arbequina’ 36 ‘配多灵’‘Pendolino’ 3.20E-01 3.20E-01 + 105-16 105 ‘豆果’‘Arbequina’ 5 ‘城固32’‘Chenggu 32’ 2.87E+00 2.87E+00 * 105-19 105 ‘豆果’‘Arbequina’ 104 ‘小苹果’‘Manzanilia’ 1.20E+00 1.20E+00 * 105-20 105 ‘豆果’‘Arbequina’ 104 ‘小苹果’‘Manzanilia’ 3.62E+00 3.62E+00 * 106-2 106 ‘贺吉布兰克’‘Hojiblanca’ 98 金叶木犀榄O. europaea subsp. cuspidata var. chrysophylla 2.12E-01 2.12E-01 + 106-4 106 ‘贺吉布兰克’‘Hojiblanca’ 104 ‘小苹果’‘Manzanilia’ 3.25E+00 3.39E-01 + 106-6 106 ‘贺吉布兰克’‘Hojiblanca’ 104 ‘小苹果’‘Manzanilia’ 1.48E+00 5.75E-01 + 106-7 106 ‘贺吉布兰克’‘Hojiblanca’ 101 ‘阿尔波萨纳’‘Arbosana’ 8.28E-01 8.28E-01 + 106-13 106 ‘贺吉布兰克’‘Hojiblanca’ 53 ‘小苹果·塞维利亚’‘Manzanilia De Sevilla’ 2.86E+00 2.86E+00 * 108-1 108 ‘皮瓜尔’‘Picual’ 105 ‘豆果’‘Arbequina’ 5.36E+00 5.36E+00 * 108-6 108 ‘皮瓜尔’‘Picual’ 105 ‘豆果’‘Arbequina’ 1.43E+00 1.43E+00 * 108-9 108 ‘皮瓜尔’‘Picual’ 106 ‘贺吉布兰克’‘Hojiblanca’ 3.86E+00 1.03E+00 + 108-13 108 ‘皮瓜尔’‘Picual’ 101 ‘阿尔波萨纳’‘Arbosana’ 1.10E+00 1.10E+00 + 注:*代表置信度为95%;+代表置信度为80%。
Notes: * represents a 95% confidence level; + represents a 80% confidence level. -
[1] Estruch R, Ros E, Salas-Salvadó J, et al. Primary prevention of cardiovascular disease with a Mediterranean diet supplemented with extra-virgin olive oil or nuts[J]. New England Journal of Medicine, 2018, 378(14): e34. doi: 10.1056/NEJMoa1800389 [2] Tarchoune I, Sgherri C, Eddouzi J, et al. Olive leaf addition increases olive oil nutraceutical properties[J]. Molecules, 2019, 24(3): 545. doi: 10.3390/molecules24030545 [3] Mookerjee S, Guerin J, Collins G, et al. Paternity analysis using microsatellite markers to identify pollen donors in an olive grove[J]. Theoretical and Applied Genetics, 2005, 111(6): 1174-1182. doi: 10.1007/s00122-005-0049-5 [4] Mekuria G T, Collins G G, Sedgley M. Genetic variability between different accessions of some common commercial olive cultivars[J]. The Journal of Horticultural Science and Biotechnology, 1999, 74(3): 309-314. doi: 10.1080/14620316.1999.11511114 [5] Díaz A, Martín A, Rallo P, et al. Cross-compatibility of the parents as the main factor for successful olive breeding crosses[J]. Journal of the American Society for Horticultural Science, 2007, 132(6): 830-835. doi: 10.21273/JASHS.132.6.830 [6] Wu S B, Collins G, Sedgley M. Sexual compatibility within and between olive cultivars[J]. The Journal of Horticultural Science and Biotechnology, 2002, 77(6): 665-673. doi: 10.1080/14620316.2002.11511554 [7] De la Rosa R, James C M, Tobutt K R. Using microsatellites for paternity testing in olive progenies[J]. HortScience, 2004, 39(2): 351-354. doi: 10.21273/HORTSCI.39.2.351 [8] Rallo L, Cuevas J, Rapoport H F. Fruit set pattern in self-and open-pollinated olive cultivars[C]//Rallo L, Caballero J M, Fernández-Escobar R. International symposium on olive growing. Cordoba: ISHS Acta Horticulturae, 1990: 219-222. [9] Díaz A, Martín A, Rallo P, et al. Self-incompatibility of ‘Arbequina’ and ‘Picual’ olive assessed by SSR markers[J]. Journal of the American Society for Horticultural Science, 2006, 131(2): 250-255. doi: 10.21273/JASHS.131.2.250 [10] Shemer A, Biton I, Many Y, et al. The olive cultivar ‘Picual’ is an optimal pollen donor for ‘Barnea’[J]. Scientia Horticulturae, 2014, 172(1057): 278-284. doi: 10.1016/j.scienta.2014.04.017 [11] Cáceres M E, Ceccarelli M, Pupilli F, et al. Obtainment of inter-subspecific hybrids in olive (Olea europaea L.)[J]. Euphytica, 2015, 201(2): 307-319. doi: 10.1007/s10681-014-1224-z [12] 秦 倩. 武都地区油橄榄品种适配性研究[D]. 北京: 中国林业科学研究院, 2015. [13] 王楠楠. 凉山州油橄榄品种适配性研究[D]. 北京: 中国林业科学研究院, 2016. [14] 徐纬英. 中国油橄榄种质资源与利用[M]. 长春: 长春出版社, 2001. [15] Sefc K M, Lopes M S, Mendonça D, et al. Identification of microsatellite loci in olive (Olea europaea) and their characterization in Italian and Iberian olive trees[J]. Molecular Ecology, 2000, 9(8): 1171-1173. doi: 10.1046/j.1365-294x.2000.00954.x [16] Carriero F, Fontanazza G, Cellini F, et al. Identification of simple sequence repeats (SSRs) in olive (Olea europaea L.)[J]. Theoretical & Applied Genetics, 2002, 104(2-3): 301-307. [17] Cipriani G, Marrazzo M T, Marconi R, et al. Microsatellite markers isolated in olive (Olea europaea L.) are suitable for individual fingerprinting and reveal polymorphism within ancient cultivars[J]. Theoretical & Applied Genetics, 2002, 104(2-3): 223-228. [18] Pasqualone A, Montemurro C, Caponio F, et al. Multiplex amplification of DNA microsatellite markers to fingerprint olive oils from single cultivars[J]. Polish Journal of Food and Nutrition Sciences, 2003, 12(Suppl. 2): 96-99. [19] Muzzalupo I, Stefanizzi F, Perri E. Evaluation of olives cultivated in Southern Italy by simple sequence repeat markers[J]. Hortscience, 2009, 44(3): 582-588. doi: 10.21273/HORTSCI.44.3.582 [20] Marshall T, Slate J, Kruuk L, et al. Statistical confidence for likelihood-based paternity inference in natural populations[J]. Molecular Ecology, 1998, 7(5): 639-655. doi: 10.1046/j.1365-294x.1998.00374.x [21] Slate J, Marshall T, Pemberton J. A retrospective assessment of the accuracy of the paternity inference program CERVUS[J]. Molecular Ecology, 2000, 9(6): 801-808. doi: 10.1046/j.1365-294x.2000.00930.x [22] Rosati A, Caporali S, Hammami S B M, et al. Tissue size and cell number in the olive (Olea europaea) ovary determine tissue growth and partitioning in the fruit[J]. Functional Plant Biology, 2012, 39(7): 580-587. doi: 10.1071/FP12114 [23] Cuevas J, Oller R. Olive seed set and its impact on seed and fruit weight[C]//Vitagliano C, Martelli G P. IV International symposium on olive growing. Valenzano: ISHS Acta Horticulturae, 2002: 485-488. [24] Barker J S F. A global protocol for determining genetic distances among domestic livestock breeds[C]//Smith C. Proceedings of the 5th world congress on genetics applied to livestock production. Guelph: Department of Animal & Poultry Science, University of Guelph, 1994: 501-508. [25] Botstein D, White RL, Skolnick M, et al. Construction of a genetic linkage map in man using restriction fragment length polymorphisms[J]. American Journal of Human Genetics, 1980, 32(3): 314. [26] 文亚峰, 韩文军, 谢伟东, 等. 微卫星标记中的无效等位基因[J]. 生物多样性, 2013, 21(1):117-126. [27] Jones A G, Ardren W R. Methods of parentage analysis in natural populations[J]. Molecular Ecology, 2003, 12(10): 2511-2523. doi: 10.1046/j.1365-294X.2003.01928.x [28] 孙 楠, 李 琪, 于 红, 等. 利用微卫星标记的魁蚶混交家系鉴定[J]. 中国海洋大学学报, 2015, 45(9):42-48. [29] 陈 亮, 汪登强, 何勇凤, 等. 基于微卫星多重PCR技术的长鳍吻亲子鉴定[J]. 农业生物技术学报, 2017, 25(9):1526-1537. [30] 殷 彬, 岳书俭, 俞 英, 等. 奶牛分子系谱构建或亲权鉴定的微卫星标记筛选[J]. 畜牧兽医学报, 2017, 48(4):595-604. doi: 10.11843/j.issn.0366-6964.2017.04.002 [31] 张冬梅, 孙佩光, 沈熙环, 等. 油松种子园自由授粉与控制授粉种子父本分析[J]. 植物生态学报, 2009, 33(2):302-310. doi: 10.3773/j.issn.1005-264x.2009.02.007 [32] 艾 畅, 徐立安, 赖焕林, 等. 马尾松种子园的遗传多样性与父本分析[J]. 林业科学, 2006, 42(11):146-150. doi: 10.3321/j.issn:1001-7488.2006.11.026 [33] 陈小勇, 宋永昌. 自然定居青冈幼苗的亲本分析[J]. 植物科学学报, 2000, 18(3):174-180. doi: 10.3969/j.issn.2095-0837.2000.03.002 [34] 何田华, 葛 颂. 植物种群交配系统、亲本分析以及基因流动研究[J]. 植物生态学报, 2001, 25(2):144-154. doi: 10.3321/j.issn:1005-264X.2001.02.003 [35] Marchese A, Marra F P, Costa F, et al. An investigation of the self-and inter-incompatibility of the olive cultivars ‘Arbequina’ and ‘Koroneiki’ in the Mediterranean climate of Sicily[J]. Australian Journal of Crop Science, 2016, 10(1): 88-93. [36] 王笑山, 淡克德. 城固油橄榄中试园主栽和授粉品种花期、花型及可配性测定结果[J]. 林业科技通讯, 1985(12):1-4. [37] Farinelli D, Tombesi A, Hassani D. Paternal and maternal effects on seed characteristics of olive cultivars[C]//Özkaya M T, Lavee S, Ferguson L. V International symposium on olive growing. Izmir: ISHS Acta Horticulturae, 2008: 121-125. -





 下载:
下载: