-
植物种群间或种群内的基因流是植物进化的主要动力,也是植物保持遗传连续性的重要因素。种子散布作为植物种群更新和基因交流的主要方式,它的散布模式不但影响种群的大小和遗传结构,也会影响种群的更新模式和可持续性[1-3]。种子离开母树后往往会受到各种限制而无法萌发或萌发后无法顺利成长为幼树,这种限制主要包括种源限制、传播限制和建成限制等[4-5]。种子产量不足和林内凋落物覆盖分别限制了红火烧兰(Cephalanthera rubra (L.) Rich.)和青杨(Populus cathayana Rehder)的自然更新能力[1, 6],而自然林内光照不足和凋落物覆盖则是银杏(Ginkgo biloba L.)进行有性更新的主要限制因子[7]。研究表明,海南岛木麻黄(Casuarina)防护林种子的室内平均萌发率仅为11.3%,种子质量总体不佳,但少数单株种子的萌发率可达22.3%~30.0%,且木麻黄单株的产种量巨大,可以弥补因种子萌发率低可能导致的更新限制。因此,种子的产量与质量并不是制约木麻黄人工林天然更新的限制因子,其天然更新难以成功的原因是林地内凋落物、光照、水分等环境因子影响了木麻黄种子萌发和幼苗生长[8-9]。
短枝木麻黄(Casuarina equisetifolia L.)是木麻黄属的常绿乔木,天然分布在亚热带至热带的沿海地区,因其抗旱、耐盐碱、生长迅速、耐贫瘠等特性,已成为华南沿海地区重要的生态防护林、用材林和多用途林树种[10-13]。目前,我国沿海木麻黄防护林以短枝木麻黄无性系造林为主,林分结构简单,品种单一,且品种间亲缘关系近[14],天然更新困难,即使存在少量的天然更新,其子代的遗传多样性也较低,近交衰退现象严重,生长差异较大,不利于木麻黄防护林的可持续经营。由于木麻黄无性系林分具有浅根性、抗逆性弱等缺点,遭遇台风时往往被连根拔起,因此,一些地区的林业管理部门要求沿海前沿100 m内的基干林带使用实生苗造林[10]。木麻黄实生人工林不仅遗传多样性高,抵御外界风险能力强,还具有寿命长、抗性高等优点。笔者观察发现,当木麻黄实生人工林地表土被人为扰动后,如合理间伐、带状翻土等,林分可以通过自由落种进行天然更新。这种通过实生人工林的种子自由散布而形成的木麻黄天然更新群体的遗传多样性如何?木麻黄林的种子散布模式是什么?散布距离有多远?能否通过这种人为干扰的方法促进木麻黄实生人工林的天然更新,减少因传统皆伐全垦的人工更新方式对沿海地区造成的水土流失、地力损耗、生物群落破坏等不利后果的影响?这些问题的解答将对指导木麻黄人工林的经营及人工促进木麻黄实生人工林的天然更新等具有较大的理论意义和实践价值。
SSR分子标记技术由于准确性高、变异位点丰富、多态性高、重复性好和共显性等优点,已被广泛应用于植物的遗传多样性和子代的亲本确定[1-2, 15-21]。本文利用前期开发的11对木麻黄EST–SSR引物,以8~10年生短枝木麻黄天然更新群体、周边的候选母本群体和30年生实生人工林群体为研究对象,利用SSR亲本分析技术确定天然更新群体中个体的亲本来源,研究短枝木麻黄的种子散布距离和特征,并通过与候选母本群体、实生人工林的比较,分析天然更新群体的遗传多样性,以期为人工促进木麻黄实生人工林的天然更新提供理论基础。
HTML
-
短枝木麻黄自然落种天然更新林和30年生实生人工林均位于福建省惠安县赤湖国有防护林场(118°54′48″ E,24°56′16″ N),属南亚热带海洋性季风气候,冬季盛行东北风,夏季盛行西南风。天然更新林为长约60 m、宽约40 m的矩形,形成时间约在2011年,是原短枝木麻黄实生人工林砍伐后,表土被人为扰动,由周边20~25年生的实生林(总长 × 总宽约为300 m × 260 m)母株自然落种后萌发长成,株高5~6 m,平均胸径9.1 cm。30年生短枝木麻黄实生人工林样地面积约25 hm2,距离天然更新林直线距离约3 km,是20世纪90年代初使用国外引进的短枝木麻黄不同种源种子营造而成,株高为25~30 m,平均胸径为33 cm。
采样时将短枝木麻黄天然更新林分为4个象限,每个象限均匀采集子代植株嫩枝,同时采集天然更新林周围150 m内所有已结果的母株(候选母本)嫩枝,最终获得子代205株,候选母本162株的样品。利用GPS(BHCnav K20s)对采样的子代和母本个体进行定位,精度为 ± 3 m,并挂牌作标记。对30年生短枝木麻黄实生人工林群体的个体嫩枝进行随机采样,采样间距为50 m,共采得98株植株的样品。所有采到的嫩枝样品用硅胶干燥保存。
-
采用改良的CTAB法[22]提取木麻黄天然更新林群体、候选母本群体和实生人工林群体个体样品的基因组DNA,并利用Nanodrop2000(Thermo)和1.2%的琼脂糖凝胶电泳检测DNA含量和纯度,然后将符合的样品稀释至20 ng·μL−1,放置在−20℃冰箱保存。
引物为前期筛选的基于表达序列标签(EST)开发的11对SSR引物,由英潍捷基(上海)贸易有限公司合成荧光引物,具体信息见表1。SSR–PCR反应体系为优化后的10 μL体系[23],包含1 × PCR buffer、0.2 mmol·L−1 dNTP、0.5 μmol·L−1引物、1.25 U Taq酶、2 ng模板DNA、1.75 mmol·L−1 Mg2+。扩增程序为:95℃预变性5 min,94℃变性1 min,最佳退火温度45 s,72℃延伸1 min,循环35次,72℃延伸10 min,4℃保存。在朗基A600 PCR仪(杭州朗基科学仪器有限公司)上进行PCR扩增,扩增完成后用ddH2O将PCR产物稀释10倍,再取1 μL加入0.16 μL LIZ500和9.34 μL Hi–Di混匀后95℃变性5 min,而后放入冰箱降温,降温后利用ABI3730X DNA分析仪进行基因分型。
引物名称
Primer序列(5′-3′)
Primer Sequence (5′-3′)5′修饰
5′ Modification纯化方式
Purification重复片段
Repeat motif退火温度
Tm/℃EST-C01(F) TGCAGCATCATCACTACT ROX HPL (AGA)6 54 EST-C01(R) ACTCCAACCAACTCTATTC PAG EST-C02(F) TTTGTCTTCCCTACTCCG TAM HPL (CTTCT)5 52 EST-C02(R) AACCCTTTTCCACTTTCTTA PAG EST-C03(F) TTCAAAACCCTAGCATCT TAM HPL (CTT)6 52 EST-C03(R) CATACCATTAACCAAAGC PAG EST-C04(F) GCTGGAGGTGGTGGTGTT FAM HPL (CT)14 56 EST-C04(R) TATGGAATAGACGAGAAGTGAG PAG EST-C08(F) GCTTTGTCCTACCGTTTC ROX HPL (GAC)12 52 EST-C08(R) ATCACCACCATCCTCGTC PAG EST-C10(F) AAAGAGAGGCTCAGAAAGA HEX HPL (GTT)9 56 EST-C10(R) GCACGAAGCAAGAGATAGA PAG EST-C13(F) ATGGGACATTTTGGTGAT HEX HPL (CATCTT)3 54 EST-C13(R) CTTTGCTTTAGGCGTTTT PAG EST-C15(F) CTTCGCCGTTTCCTCAGA ROX HPL (AG)13 56 EST-C15(R) ATATTTGCTTCGCAGGTCA PAG EST-C16(F) ATGATGAAGACGAGGATC FAM HPL (GAA)5 54 EST-C16(R) CTTCTTCTTCTTCCACCAC PAG EST-C18(F) AAAGGCACAAGTTAGGAGAG HEX HPL (CT)12 56 EST-C18(R) GCTGGTGCTGTTGAAATG PAG EST-C19(F) CGACCCAACCAAAATCTC TAM HPL (CT)7 56 EST-C19(R) AAGCGACAATCTGAAAGAAG PAG Table 1. Sequences of 11 SSR fluorescent primers
-
利用Gene Marker V2.2.0软件读取基因分型数据,采用软件Cervus 3.0中常用的80%和95% 2种可信度检验对205个种子散布子代单株和162株候选母本进行母本分析,根据最大似然法估算每个候选母本的似然性值比率(LOD),LOD取正值。软件参数设置如下:循环数为100 000,候选亲本的取样比为0.85,匹配基因位点为0.99,不匹配基因位点为0.01。计算天然更新林和实生人工林的等位基因数(Na)、有效等位基因数(Ne)、观测杂合度(Ho)、期望杂合度(He)和多态性信息量(PIC),利用POPGEN Version 1.32计算不同群体位点的Shannon's指数(I)和Nei's遗传多样性指数(h)。
1.1. 试验地概况及样品采集
1.2. DNA提取和SSR–PCR扩增
1.3. 数据统计和分析
-
利用前期筛选的11对EST-SSR多态性引物对短枝木麻黄种子散布子代和母本共计367个个体进行遗传分型,检测结果(表2)表明:11个SSR位点共检测出137个等位基因,平均等位基因数为12.45,平均有效等位基因数为4.95,其中,位点C18等位基因数最多(24个),位点C13的等位基因数最少(6个)。11个位点的平均观测杂合度和期望杂合度分别为0.77和0.75,其中,位点C02、C04、C15、C18的观测杂合度小于期望杂合度,表明这些位点杂合子缺失。该试验群体11个SSR位点平均多态性信息量为0.72,除位点C13多态性信息量属于中度多态性位点外,其余10个位点多态性信息量均大于0.50,属于高度多态性位点,Shannon's指数平均为1.74,表明本研究所采用的11对SSR引物能够检测出较多的等位位点,可以很好地反映该试验群体的遗传多样性。
位点 Locus 等位基因数 Na 有效等位基因数 Ne 观测杂合度 Ho 期望杂合度 He 多态性信息量 PIC Shannon’s信息指数 I C01 9 3.89 0.83 0.74 0.72 1.69 C02 11 5.54 0.76 0.82 0.80 1.84 C03 12 3.24 0.83 0.69 0.67 1.61 C04 8 2.88 0.60 0.65 0.59 1.26 C08 15 6.78 0.85 0.85 0.84 2.14 C10 9 3.69 0.79 0.73 0.69 1.47 C13 6 1.83 0.55 0.45 0.41 0.84 C15 17 8.70 0.78 0.89 0.88 2.38 C16 14 3.48 0.83 0.71 0.68 1.67 C18 24 10.03 0.80 0.90 0.89 2.52 C19 12 4.36 0.87 0.77 0.74 1.70 平均 Mean 12.45 4.95 0.77 0.75 0.72 1.74 Table 2. SSR polymorphism analyses of progeny and maternity populations of C.equisetifolia seedling plantation
-
对短枝木麻黄205个种子散布子代单株进行母本分析,结果(表3)表明:在95%置信区间下能确定母本的子代有19株,占子代试验群体的9.27%;在80%的置信区间下可为148株种子散布子代确定母本,占取样子代的72.20%,其余子代的LOD值为负值,表明子代与候选母本无亲缘关系。在已确定子代的84株母本中有7株母本鉴定出了4株子代,子代与母本的距离为17~108 m;可以鉴定出3株子代的母本有9株,子代与母本的距离为33~112 m,其他确定的候选母本鉴定子代个数为2株或1株。
母本
Maternal
tree子代株数
Numbers of
Progeny/株距离
Distance/
m母本
Maternal tree子代株数
Numbers of
progeny/株距离
Distance/
m母本
Maternal
tree子代株数
Numbers of
progeny/株距离
Distance/
m母本
Maternal
tree子代株数
Numbers of
progeny/株距离
Distance/
mM5 4(1) 25~62 M68 2 65~95 M10 1 54 M69 1 110 M9 4 60~76 M76 2 66~92 M16 1 38 M73 1 66 M109 4 35~62 M78 2 76~99 M21 1 55 M77 1 112 M111 4(1) 53~65 M83 2 110~114 M23 1 44 M86 1(1) 112 M115 4(1) 17~59 M97 2 94~96 M24 1 58 M89 1 92 M124 4(1) 57~74 M108 2(1) 55~57 M25 1(1) 66 M90 1 105 M132 4(1) 94~108 M110 2 25~62 M26 1 77 M94 1 122 M39 3 33~87 M117 2 17~37 M34 1 79 M96 1 130 M48 3 57~79 M118 2 27~28 M38 1 79 M107 1 42 M70 3 99~112 M119 2 22~39 M43 1(1) 97 M112 1 32 M74 3 72~80 M12 2(2) 42~67 M44 1 85 M113 1 53 M125 3(3) 53~70 M122 2 23~33 M46 1 98 M134 1 82 M129 3 45~60 M123 2 47~58 M51 1 63 M138 1 68 M137 3 72~95 M126 2 51~56 M53 1(1) 67 M139 1 101 M140 3(1) 87~95 M128 2(1) 39~54 M56 1 67 M143 1 119 M154 3(1) 90~103 M130 2 60~61 M59 1 65 M144 1 123 M1 2 30~35 M133 2 71~98 M60 1 78 M147 1 105 M6 2 65~66 M135 2 100~103 M61 1 46 M153 1 74 M58 2 59~94 M141 2 73~88 M64 1 46 M155 1 102 M62 2 68~83 M160 2 86~87 M66 1 76 M158 1(1) 79 M65 2 80~110 M2 1 49 M67 1 93 M161 1 113 注:括号内外的数字分别表示95%和80%置信区间下的子代数;黑色加粗字体表示位于样地东部和东北部的母本。
Notes: Numbers inside and outside of parenthesis indicate the number of progenies at 95% and 80% confidence intervals, respectively. The bold black font represents the maternity located in the east and northeast of the sample site.Table 3. Maternity analyses of seed-dispersed progenies from C.equisetifolia seedling plantations
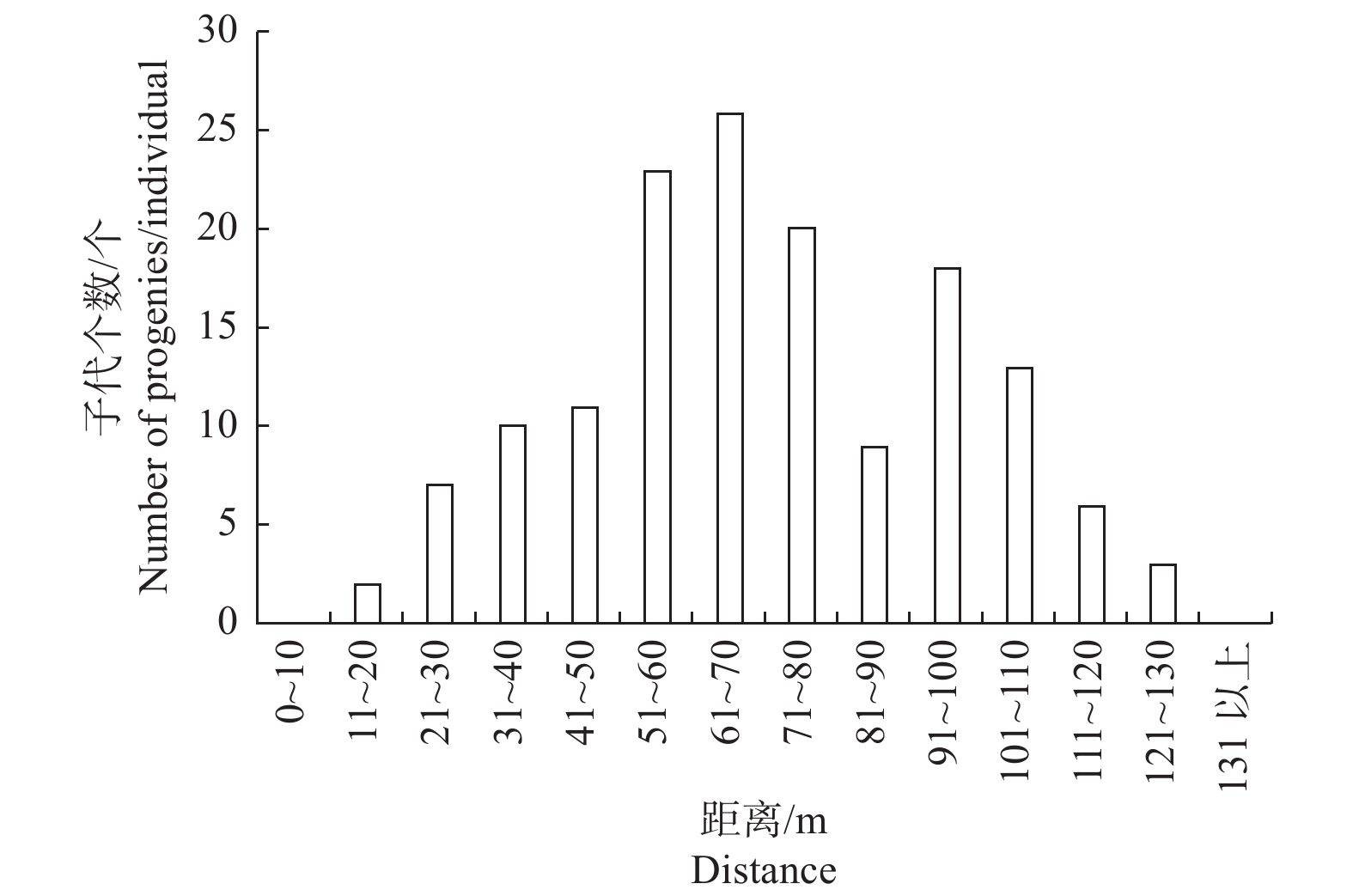
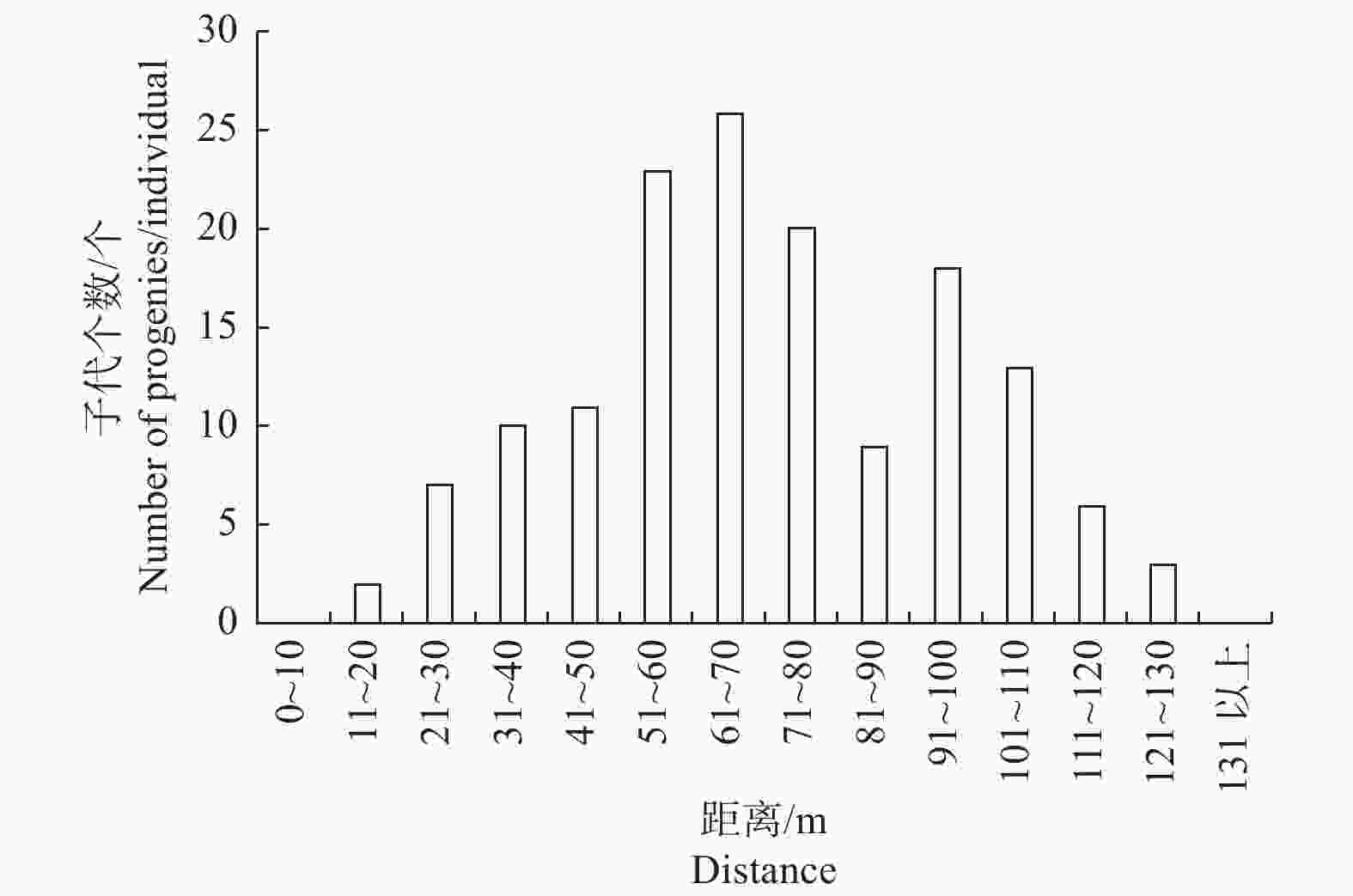
对已确定母本的子代和其相对应的母本进行了定位,分析了短枝木麻黄种子散布的有效距离,结果(图1)表明:短枝木麻黄种子散布的范围较宽,有效散布距离为10~130 m,平均散布距离为71 m。随着散布距离的增加,确定子代的个数出现了2个峰值,分别集中在50~80 m和90~110 m两个区间,各确定了69株和31株子代;散布距离在20~120 m范围内,共有143株子代可以确定母本,占已确定母本子代群体的96.62%。散布距离超过120 m,确定母本的子代数量明显减少,在120~130 m内仅发现了3株子代,超过130 m后没有可以确定母本的子代。已确定子代的母本中有71.43%位于样地东北和东部,共鉴定出111株子代,母本贡献率为75.00%。天然更新群体样本中不能确定母本的子代占27.80%,推测种子可能由更远的木麻黄林通过风或野生动物散布过来(图1、表3)。
-
从母本群体中选取已确定子代的84株母本,并从天然更新子代群体中选取与母本对应的84株子代以及从实生人工林群体中随机选取84株个体,形成母本、天然更新子代和实生人工林3个样本数相同的群体,然后利用11个SSR位点开展遗传多样性比较。结果(表4)显示:天然更新子代群体的平均等位基因数、有效等位基因数、观测杂合度、期望杂合度、多态性信息量、Shannon’s信息指数和Nei’s遗传多样性指数均略低于母本群体和实生人工林群体,而母本群体的遗传多样性参数除等位基因数外也均稍低于实生人工林群体。短枝木麻黄天然更新群体的遗传多样性与母本群体、实生人工林群体相比虽然略有降低,但其观测杂合度和期望杂合度仍远高于0.50,仍保持了较高的遗传多样性水平。
遗传多样性参数
Genetic diversity parameters天然更新群体
Natural regeneration population母本群体
Maternal population实生人工林群体
Seedling plantation population等位基因数 Na 9.00 10.00 9.55 有效等位基因数 Ne 4.65 4.83 5.15 观测杂合度 Ho 0.73 0.82 0.84 期望杂合度 He 0.72 0.76 0.77 多态性信息量 PIC 0.69 0.72 0.73 Shannon’s信息指数 I 1.62 1.72 1.74 遗传多样性指数 h 0.72 0.75 0.76 Table 4. Genetic diversity analyses of different populations of C.equisetifolia
2.1. SSR多态性分析
2.2. 种子散布子代母本分析及种子有效散布距离
2.3. 不同群体遗传多样性分析
-
研究表明,利用SSR分子标记对以异交为主的植物开展亲本分析时,应选择较多的遗传位点,10~20个多态性高的共显性分子标记可以取得较好的亲本分析结果,而自交为主的植物应多增加子代的取样数量[24-25]。风媒植物短枝木麻黄大多数为雌雄异株,交配模式以异交为主,在开展亲本分析时应采用较多的SSR位点。本研究利用11个SSR位点对木麻黄367个个本进行扩增,平均每个位点12.45个等位基因,平均观测杂合度和期望杂合度分别为0.77和0.75,平均多态性信息量和Shannon’s信息指数分别为0.72和1.74,表明这些标记具有相对较高的多态性,可用于木麻黄亲本分析、种质资源鉴定和遗传图谱构建等研究。
本研究利用软件Cervus3.0对短枝木麻黄实生人工林的种子散布子代进行母本分析,结果表明,在95%置信区间下只能为天然更新林19株子代确定母本,而在80%的置信区间下可为148株子代确定母本,占子代群体的72.20%,仍有27.80%的子代未能确定其母本,这可能是因为试验地点位于风速较大的沿海地区,轻且带翅的木麻黄种子在强风下能进行较长距离的散播,所以,部分未确定母本的子代很可能来自较远的母树;另外的原因可能是个别位点的扩增成功率相对较低,造成一些DNA遗传分型的数据缺失,导致短枝木麻黄亲本分析效率降低,使部分子代的母本未能被成功鉴别出来,下一步可通过增加新的标记位点来提高亲本的分析效率。
遗传多样性的高低代表着物种进化潜力的高低,遗传多样性越高则物种适应不良环境的能力就越强。目前,我国沿海木麻黄防护林多为短枝木麻黄无性系造林,遗传多样性水平低。余微等[14]利用12对EST-SSR引物对广东、福建、海南三省109个主栽短枝木麻黄无性系进行遗传多样性分析发现,华南三省109个短枝木麻黄无性系平均Shannon’s信息指数为1.10;许秀玉等[26]利用22条ISSR引物对来自广东、福建和海南等地的51个木麻黄无性系进行遗传多样性分析也发现了相同结论,51个无性系的平均Shannon’s信息指数仅为0.43。本研究利用11对EST-SSR引物对短枝木麻黄天然更新群体中的84个个体进行遗传多样性评价,平均等位基因数和有效等位基因数以及Shannon’s信息指数和遗传多样性指数分别为9.00、4.65和1.62、0.72,远高于华南地区的无性系群体,也高于其他一些同样依靠风力散播种子的植物群体,如密叶杨(Populus talassica Kom.)(I =1.379,h = 0.71)[27]、杉木(Cunninghamia lanceolate (Lamb.) Hook.)(I = 0.832,h = 0.476)[28]、青钱柳(Cyclocarya paliurus (Batal.) Iljinsk.)(I = 0.686,h = 0.404)[29]。这说明依靠风力进行种子散播的短枝木麻黄实生林,其天然更新群体具有较高的遗传多样性水平(I = 1.62,h = 0.72),但与其母本群体和实生人工林群体相比,短枝木麻黄天然更新群体表现了相对较低的遗传多样性,主要原因可能是天然更新子代很多都来源于相同母本,也很可能具有相同的父本。已有研究表明,林分中母株附近的高大雄株对子代的花粉贡献率具有明显的优势[30-31],因此,包含了一些半同胞甚至是全同胞子代的天然更新群体的遗传多样性略低于母本群体和实生人工林群体。
种子的传播和幼苗的定居是植物种群生态和进化遗传学研究的重要组成部分,国内外研究学者已经广泛应用分子标记来研究植物种子的散布格局及其对种群的影响。研究表明,种子通过重力或者风力传播的树种,其幼苗多聚集在母树周围,具有较强的空间遗传结构;而通过动物进行种子传播的树种,因种子传播者的生活习性如觅食、储存等行为,幼苗往往定居在远离母树的地方,种群的空间遗传结构较简单,但群体间拥有较高遗传异质性的可能性较大[3, 32-33]。本研究利用11对SSR引物对短枝木麻黄实生人工林天然更新群体进行母本分析,探究短枝木麻黄种子的散布规律。结果表明,短枝木麻黄种子有效散布距离为10~130 m,平均散布距离为71 m,与异木麻黄属轮生木麻黄(Allocasuarina verticillata (Lam.) L.A.S. Johnson)(约100 m)的散布距离相近[34],远低于种子长距离散播(不少于树高100倍的距离)的标准[35],属于短距离传播。种子靠风力散播的植物中,其种子散布能力受生境和空气动力学参数的影响较大[36],种子的散布效率与种子沉降速度、林分下层植被密度及母树周围植被高度成反比[37]。本研究中,在已确定子代的母本中,位于样地东北和东部的母本对天然更新子代的贡献率为75.00%,散布距离在50~80 m内的子代个数最多,这是因为木麻黄种子成熟旺期主要集中在10-11月,而该段时间内样地盛行东北风,因而,东北方向的母株贡献了天然更新林群体的多数子代。
-
短枝木麻黄作为华南沿海防护林重要树种,主要生长在沿海沙地,由于木麻黄防护林内枯枝落叶层厚,种子难以接触到土壤,再加上原生环境荫蔽、干旱等不利条件导致种子萌发和幼苗生长均受到限制。本研究利用11对SSR引物对木麻黄实生人工林种子散布子代进行遗传多样性和母本分析,结果表明,木麻黄种子有效散布距离为10~130 m,主要集中在20~120 m,属于短距离传播,子代群体平均Shannon’s信息指数和Nei’s遗传多样性指数分别为1.62和0.72,略低于母本群体和30年生实生林群体,但仍处于较高水平,说明通过对木麻黄实生人工林进行人为干扰和管理,如采取合理间伐、带状翻土、人工增施氮钾肥、补植优质的实生苗等措施,优化短枝木麻黄种子萌发与幼苗定居的生长环境,有望实现短枝木麻黄实生林的天然更新,且子代能保持相对较高的遗传多样性,此研究可为木麻黄人工林的经营及人工促进木麻黄实生林更新等奠定相应的理论基础。




 DownLoad:
DownLoad: