-
油橄榄(Olea europaea L.)是木樨榄属(Olea)常绿乔木,世界四大木本油料作物之一,野生油橄榄起源于小亚细亚,主产区在地中海区域[1],但南、北半球的40多个亚热带国家都有引种栽培,植物油产量居世界第六位[2]。油橄榄与其他亚热带常绿经济林树种一样,冷胁迫一方面影响其地理分布,另一方面造成产量的巨大损失[3],希腊和意大利就曾在2004年和2008年遭遇寒冷天气,导致油橄榄园受灾,鲜果减产[4]。我国西秦岭南坡的油橄榄主产区,位于北亚热带北缘,低温是限制该区域油橄榄地理分布和鲜果减产的重要因素[5],而引种和筛选耐低温品种能一定程度上解决低温对油橄榄栽培带来的不利影响[6]。
植物可以通过在低温条件下激活抗氧化酶系统抵御超氧自由基的毒害[7];通过调节组织中可溶性蛋白、非结构性碳水化合物以及游离脯氨酸含量来提高细胞液渗透势,提高对寒冷的忍耐力[8];低温下植物净光合速率、气孔导度、蒸腾速率和胞间CO2浓度等指标的变化能够反映植物光合器官受损程度,也与耐寒能力间有一定关系[9]。因此耐寒生理指标、植物光系统在低温下的破坏程度都可以作为耐寒性评价的方法,但由于各生理指标对低温敏感性差、实验数据可重复性低等因素,使植物耐寒能力定量化评价变得尤为复杂。在油橄榄适应性育种工作中,有许多科研人员致力于研发可靠的油橄榄耐寒性评价技术,用于筛选耐低温品种。地中海油橄榄主产区,M.Gómez等人通过对10个油橄榄品种越冬(−10.5 ~ −6.5 ℃)表现进行观测,发现油橄榄嫩枝抗冻性与发芽能力呈线性相关[10],品种间抗冻性存在显著差异,品种‘Cornicabra’和‘Arbequina’低温后嫩枝损伤率低,再生能力强,而‘Empeltre’、‘Frantoio’和‘Hojiblanca’耐寒性差。Cansev等人研究了9个油橄榄品种抗氧化酶的变化规律与耐寒性的关系,发现品种‘Domat’、‘Lecquest’、‘Ascolona’、‘Hojoblanca’和‘Gemlik’的组织通过增加过氧化氢酶(CAT)、抗坏血酸过氧化物酶(APX)和还原型辅酶II(NADPH)等酶的活性来激活抗氧化系统和脱氢酶的表达,增强了低温下细胞膜结构的稳定性,具有较强的耐寒能力[11]。在我国油橄榄作为引进树种,许多研究人员期望通过耐寒性评价来获得适合北亚热带高纬度、高海拔区域发展的品种,来扩大适生区。80年代,在油橄榄适应性研究过程中,就发现叶片节间短、叶片厚而浓绿、叶缘反卷等叶片形态与耐寒性呈正相关[12]。近几年,令凡等人也通过低温胁迫试验,对6个油橄榄品种1年生扦插苗耐寒能力的大小进行了评价,由强到弱依次为:‘Picholine’>‘Pendolino’>‘Leccino’>‘Ascolana’>‘Ez-8’>‘Frantoio’,但是采用油橄榄离体植物叶片进行低温胁迫试验所评价耐寒能力大小与活体样本有所偏差[5]。此外,低温胁迫对光系统破坏与植物耐寒性的关系在甘蔗、油菜等植物中已有研究报道[13-14],低温不耐寒品种的光系统损伤较大,叶绿素荧光参数、叶绿素含量均明显较耐寒品种低,但利用叶绿素荧光参数和气体交换参数结合评价油橄榄耐寒性的研究方法比较少见。试验以活体植株进行冷胁迫,以期揭示不同品种油橄榄幼苗膜系统、渗透调节物质、抗氧化酶系统、光系统对低温胁迫的响应,评价不同油橄榄品种幼苗耐寒性,为筛选耐寒品种提供方法和依据。
-
植物材料为2年生油橄榄无性系扦插苗,由油橄榄国家林木种质资源库提供,地点位于甘肃省陇南市武都区两水镇段河坝村,地理坐标(104°47′59″~104°49′02″ E,33°23′45″~33°24′57″ N),属于北亚热带半湿润气候,年平均气温14.9 ℃,绝对最高温40 ℃,极端低温−8.6 ℃,年日照1 911.7 h,无霜期150~270 d,年降水量474~900 mm,年平均湿度61%~71%,供试品种见表1(木质化程度基本一致)。
表 1 供试油橄榄材料基本情况
Table 1. Information of the test materials of olive seedlings
品种
Cultivar中文译名
Chinese叶长
Leaf length/mm叶宽
Leaf width/mm叶间距
Blade spacing/mm叶厚度
Leaf thickness/mm株高
Plant height/cm茎粗
Stemdia meter/mmArbequina 豆果 51.077 ± 2.729 bc 11.783 ± 1.021 ab 23.553 ± 2.362 ab 0.470 ± 0.036 a 27.367 ± 1.198 a 3.413 ± 0.263 a EZ-8 鄂植8号 50.920 ± 1.506 bc 11.043 ± 0.582 a 25.813 ± 4.445 ab 0.483 ± 0.035 a 30.767 ± 1.453 ab 3.577 ± 0.212 a Frantoio 佛奥 44.043 ± 1.975 a 10.840 ± 0.135 a 28.757 ± 5.191 b 0.467 ± 0.012 a 30.167 ± 4.253 ab 3.730 ± 0.433 a Leccino 莱星 47.233 ± 0.994 ab 11.057 ± 0.734 a 26.393 ± 2.620 ab 0.483 ± 0.032 a 35.233 ± 2.904 b 3.443 ± 0.437 a Koroneiki 柯基 53.810 ± 3.337 c 13.100 ± 0.894 b 22.613 ± 2.121 a 0.567 ± 0.021 b 33.700 ± 1.955 ab 3.500 ± 0.360 a Picual 皮瓜尔 52.523 ± 3.496 bc 11.933 ± 1.708 ab 27.270 ± 1.259 ab 0.563 ± 0.047 b 31.933 ± 0.689 ab 3.743 ± 0.064 a Coratina 科拉蒂 52.507 ± 2.381 bc 10.563 ± 0.108 a 25.207 ± 0.454 ab 0.577 ± 0.031 b 33.700 ± 1.457 ab 3.650 ± 0.437 a Arbosana 阿尔波萨纳 51.250 ± 4.280 bc 10.917 ± 1.042 a 26.097 ± 1.931 ab 0.617 ± 0.021 b 33.200 ± 1.305 ab 3.893 ± 0.072 a 注:表中数值为平均值 ± 标准误(n=3),不同小写字母表示同一品种不同处理间在0.05水平上差异显著(P<0.05)
Notes: The values in the table are the mean ± standard error (n=3), and the different lowercase letters indicate the significant differences in the 0.05 level between the different treatments of the same variety (P <0.05) -
2021年3月,每个供试品种挑选健壮且长势基本一致的30株2年生无性系扦插苗,盆栽于3 L容器中(肥水条件一致),至11月中旬大田温度降至20 ℃左右时,参照Ben-Ari[15]、Davide Guerra[16]等人冷胁迫方法,每个品种挑选21株置于人工气候室中,在22 ℃/18 ℃条件下适应14 d(光照时间为8:00—18:00,光照强度800 μmol·m−2·s−1、湿度50%~60%,温度控制误差为 ± 0.5 ℃),3株作为对照(CK),其余18株保持与之前相同的光强和光周期,以1 ℃·h−1降温速度进行低温处理,分别在达到16、12、8、4、0、−4 ℃时维持24 h,在各温度胁迫结束前3 h进行采样和测试。
-
胁迫结束前3 h每个品种随机选取3株,每株选取枝条顶端至基部方向第2~4对叶片中叶形、大小较为一致的3片叶,进行光合和荧光参数测定。随机摘取枝条顶端至基部方向第2~4对叶片中5~6片,根据李玲等[13]人的方法进行叶绿素含量(Chl)、可溶性糖(SS)、可溶性蛋白(SP)、脯氨酸(Pro)、丙二醛(MDA)、超氧化物歧化酶(SOD)、过氧化物酶(POD)、过氧化氢酶(CAT)等指标参数测定。
光合参数测定利用LI-6400便携式光合作用分析系统;叶绿素荧光参数测定采用CF-imager叶绿素荧光图像分析仪进行离体测定;电导率用DDS-11A 型电导率仪测定。
-
采用Excel 2010整理数据和SPSS 23.0进行数据处理,用Duncan多重比较检验不同处理间的差异显著性(ɑ=0.05),用origin2019作图。
-
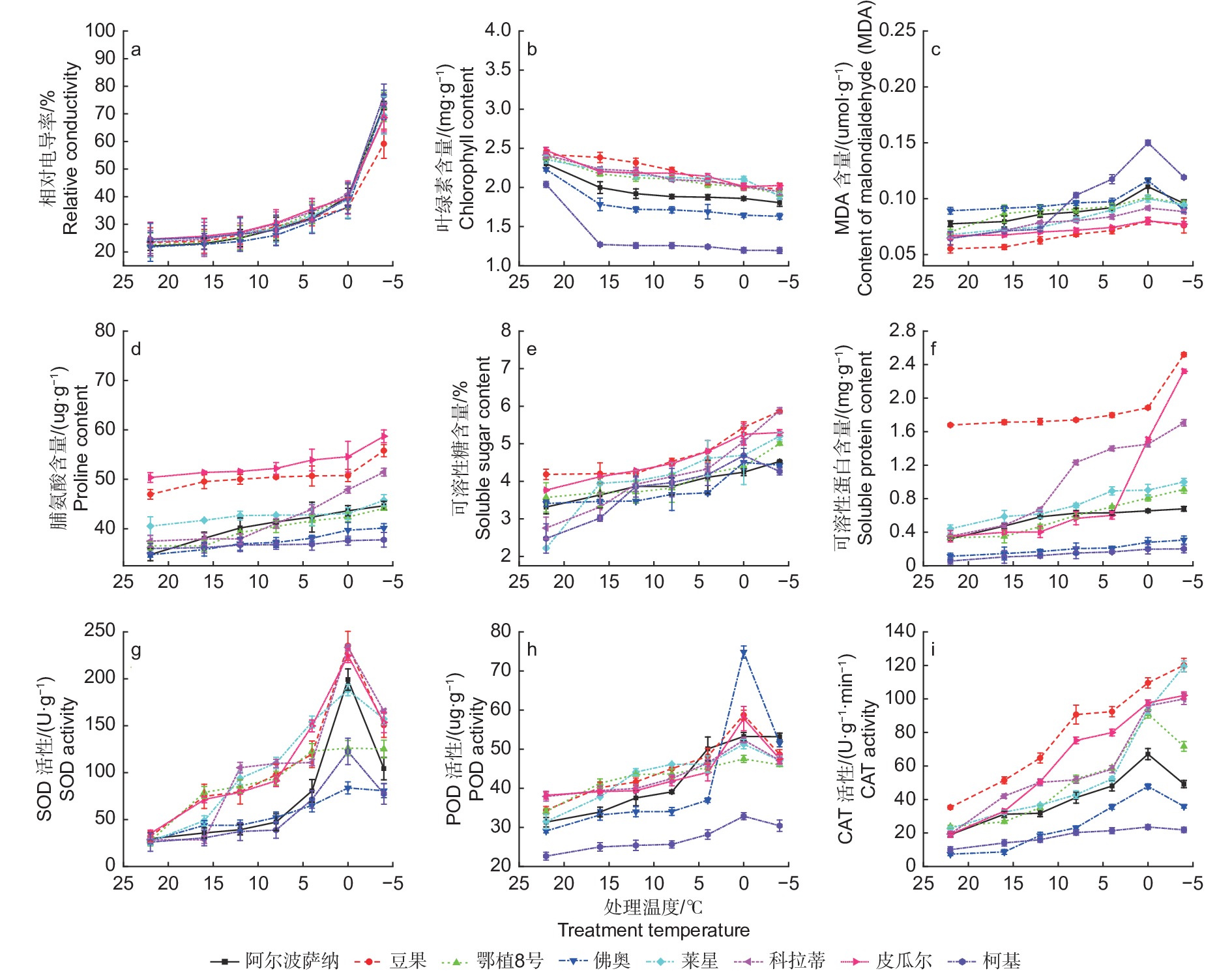
如图1a所示,温度从22 ℃降到0 ℃时,所有供试品种相对电导率逐渐增高,说明细胞膜透性缓慢增加,电解质在缓慢渗出。当温度降低至−4 ℃时,‘柯基’、‘佛奥’、‘阿尔波萨纳’和‘鄂植8号’叶片相对电导率分别升高至76.63%、72.50%、73.27%和73.00%,说明其叶片细胞膜受损严重,而‘豆果’、‘皮瓜尔’、‘科拉蒂’和‘莱星’相对电导率均小于70%,细胞膜受到伤害较小。通过Logistic方程对各品种不同处理温度和叶片相对电导率进行拟合,确定了LT50。发现8个油橄榄品种叶片相对电导率与半致死温度间呈较强正相关,供试品种的LT50介于−16.359~−9.715 ℃之间表2,耐寒性排序如下:‘豆果’>‘皮瓜尔’>‘科拉蒂’>‘莱星’>‘佛奥’>‘鄂植8号’>‘阿尔波萨纳’>‘柯基’。
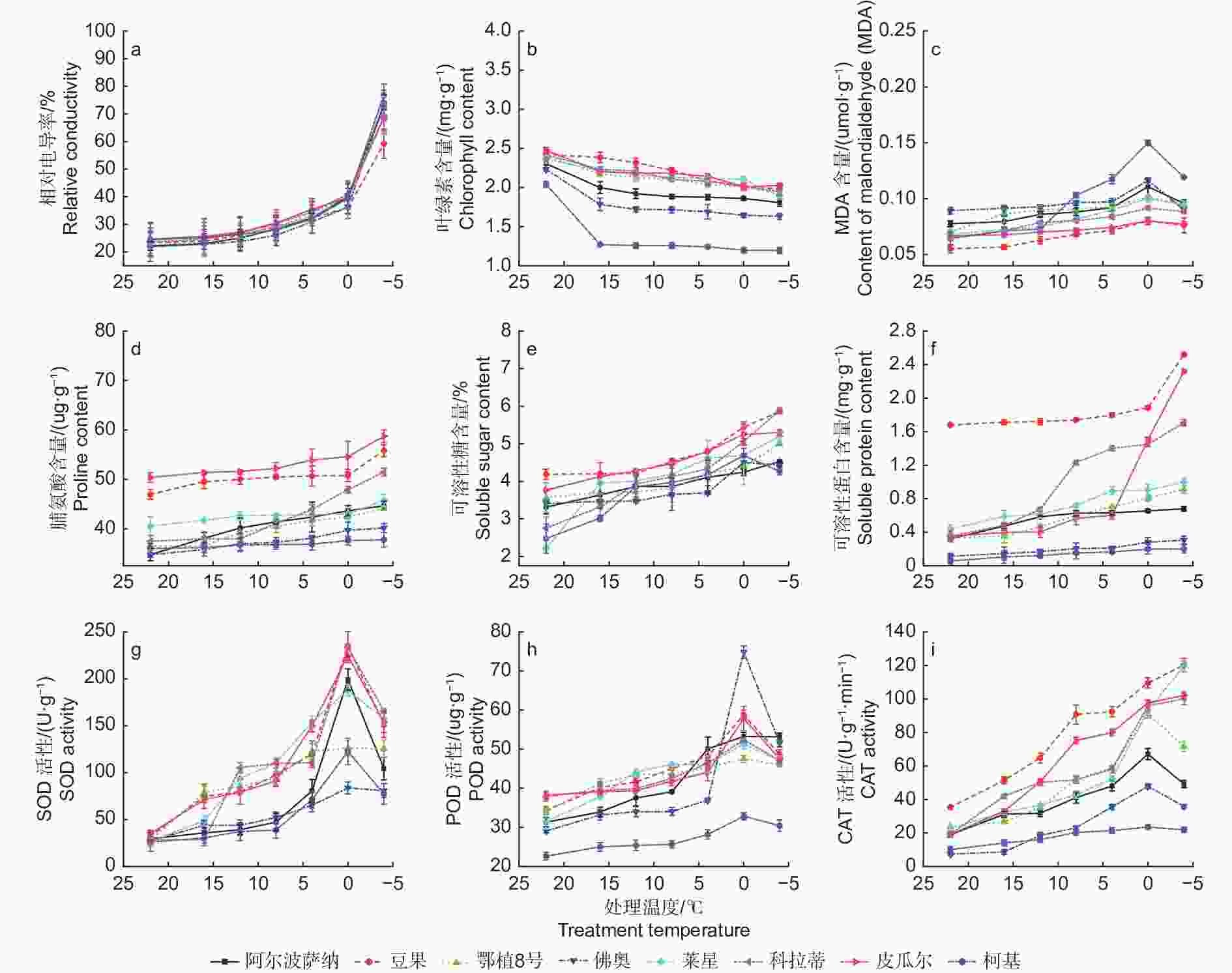
图 1 低温胁迫过程中8个油橄榄品种生理指标变化
Figure 1. The change characteristics of physiological indices in eight olive seedlings under low-temperature stress
表 2 参试品种半致死温度
Table 2. Semi-lethal temperature of tested varieties
品种
CultivarLogistic方程
Logistic equationR2 LT50 / ℃ 阿尔波萨纳
ArbosanaY=100/(1 + 8.123e−0.190x) 0.964 9** −11.019 ± 1.031 bc 豆果
ArbequinaY=100/(1 + 11.333e−0.148x) 0.982 5** −16.359 ± 1.225 a 鄂植8
Ezhi8Y=100/(1 + 7.478e−0.175x) 0.972 4** −11.517 ± 0.879 bc 佛奥
FrantoioY=100/(1 + 7.622e−0.176x) 0.964 4** −11.534 ± 0.586 bc 莱星
LeccinoY=100/(1 + 9.335e−0.166x) 0.965 2** −13.481 ± 1.125 b 科拉蒂
CoratinaY=100/(1 + 8.575e−0.155x) 0.932 8* −13.836 ± 1.111 b 皮瓜尔
PicualY=100/(1 + 9.441e−0.156x) 0.925 5* −14.410 ± 1.263 ab 柯基
KoroneikiY=100/(1 + 7.766e−0.211x) 0.932 8* −9.715 ± 0.774 c 注:*和**表示相关系数达显著和极显著水平。同一列中的不同小写字母表示差异显著(p<0.05)
Notes: *means significant difference at p<0.05;**means significant difference at p<0.01. Values within a column followed by different letters are significantly different at p<0.05. The same below -
8个油橄榄品种叶片叶绿素含量随温度的下降而减少。从22 ℃降至−4 ℃,‘豆果’和‘皮瓜尔’的叶片叶绿素含量降幅较小,分别为18.31%和18.21%,而‘佛奥’和‘柯基’降幅最大,分别为26.88%和41.37%(图1b)。
-
‘豆果’、‘皮瓜尔’、‘科拉蒂’和‘莱星’叶片丙二醛(MDA)含量总体低于其他品种,在低温胁迫加剧的过程中呈先升高后降低的趋势,都在0 ℃达到高峰。0 ℃降低至−4 ℃的过程中,‘柯基’和‘佛奥’降幅度最大,为20.60%和22.61%(图1c)。
-
供试品种叶片脯氨酸含量随着低温胁迫加剧总体呈升高的趋势,在−4 ℃均达到峰值,与0 ℃相比,‘皮瓜尔’增幅较大,为7.58%,而‘柯基’和‘佛奥’增幅较小,分别为0.46%和1.05%(图1d)。
-
叶片可溶性糖含量随着胁迫加剧总体呈升高趋势,在−4 ℃达到峰值,‘豆果’可溶性糖含量显著高于其他品种。在0~−4 ℃,‘柯基’和‘佛奥’的可溶性糖含量均有所下降,‘柯基’降幅明显(图1e)。
-
‘豆果’可溶性蛋白含量显著高于其他品种,叶片可溶性蛋白含量随温度降低而升高。−4 ℃胁迫下,‘皮瓜尔’的增幅最大,为54.14%,‘豆果’次之,而‘柯基’的增幅仅为1.67%,说明其受低温影响较大(图1f)。
-
随着处理温度的降低,各油橄榄品种叶片的SOD活性总体呈先升高后降低的趋势,同一品种在不同低温胁迫下均存在显著差异(P<0.05)。在0 ℃均达到峰值,其中‘豆果’的SOD活性最高,为235.19 U·g−1,‘科拉蒂’次之。与室温CK相比,−4 ℃时,‘莱星’和‘科拉蒂’的增幅最大,‘豆果’次之,而‘柯基’和‘佛奥’增幅最小,分别为197.46%和193.70%(图1g)。
-
8个油橄榄品种叶片的POD活性随着处理温度的降低总体呈先升高后降低的趋势。除‘鄂植8号’在 −4 ℃达到峰值,而其余品种均在0 ℃达到峰值,0~−4 ℃活性降低,其中‘豆果’的POD活性总体高于其他品种,而‘柯基’最小(图1h)。
-
随着处理温度的降低,‘豆果’、‘皮瓜尔’、‘科拉蒂’和‘莱星’的CAT活性均呈上升趋势,在−4 ℃达到峰值,而‘鄂植8号’、‘阿尔波萨纳’、‘佛奥’和‘柯基’均呈先升高后降低的趋势,在0 ℃达到峰值(图1i)。
-
以相对电导率、叶绿素含量、可溶性糖含量和可溶性蛋白质含量等9个参数,计算各参数的平均隶属函数值,并进行耐寒能力综合评价,‘豆果’、‘皮瓜尔’、‘科拉蒂’和‘莱星’的平均隶属函数值差异不显著,但与其它品种之间存在显著差异(P<0.05)。8个品种油橄榄耐寒性由强到弱见表3,依次为:‘豆果’>‘皮瓜尔’>‘科拉蒂’>‘莱星’>‘鄂植8号’>‘阿尔波萨纳’>‘佛奥’>‘柯基’。
表 3 低温胁迫下8种油橄榄幼苗测定指标的隶属函数值
Table 3. Membership function values of the eight olive seedlings under low-temperature stress
指标
Indexes品种 Cultivar 阿尔波萨纳
Arbosana豆果
Arbequina鄂植8号
Ezhi 8佛奥
Frantoio莱星
Leccino科拉蒂
Coratina皮瓜尔
Picual柯基
Koroneiki相对电导率 Relative electric conductivity 0.52 0.54 0.69 0.00 0.66 0.83 0.99 1.00 叶绿素 Chlorophyll content 0.70 1.00 0.89 0.50 0.92 0.93 0.97 0.00 可溶性糖 Soluble sugar 0.16 1.00 0.29 0.03 0.36 0.43 0.82 0.00 可溶性蛋白 Soluble protein 0.25 1.00 0.26 0.04 0.35 0.52 0.43 0.00 脯氨酸 Proline content 0.24 0.84 0.20 0.04 0.36 0.35 1.00 0.00 丙二醛含量 MDA content 0.70 0.00 0.69 0.89 0.49 0.39 0.17 1.00 SOD活性 SOD activity 0.34 0.96 0.64 0.00 0.94 0.94 1.00 0.02 POD活性 POD activity 0.86 1.00 0.88 0.82 0.90 0.91 0.93 0.00 CAT活性 CAT activity 0.37 1.00 0.53 0.11 0.62 0.66 0.76 0.00 平均隶属度 Average degree of membership 0.46 0.82 0.56 0.27 0.62 0.66 0.78 0.22 耐寒排序 Order of cold resistance 6 1 5 7 4 3 2 8 -
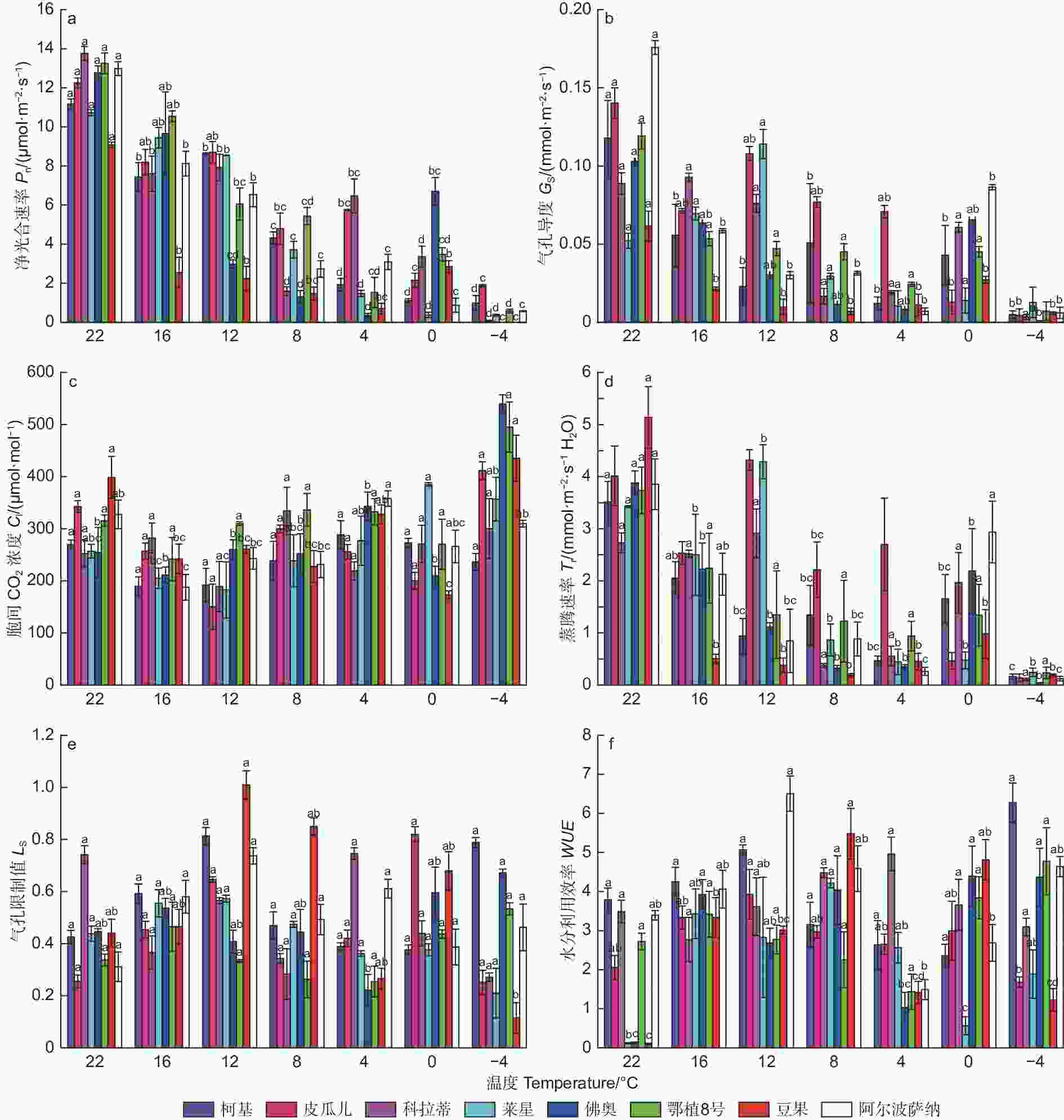
参试油橄榄品种在室温下(22 ℃),各光合参数就有所差异(图2)。随着低温胁迫加剧,参试油橄榄品种叶片净光合速率(Pn)整体呈下降趋势,-4 ℃与对照(CK,22 ℃)相比,‘皮瓜尔’降幅最小为84.79%,其他品种降幅都在90%以上。低温胁迫过程中,气孔导度(Gs)在4 ℃前整体呈下降趋势,4 ℃与CK相比,‘皮瓜尔’和‘科拉蒂’的降幅最小,分别较CK下降了49.57%和78.37%;‘阿尔波萨纳’降幅最大,达到96.02%。胞间CO2浓度(Ci)在8个品种中呈现出不同的变化规律,-4 ℃时‘阿尔波萨纳’和‘柯基’较CK降低了5.36%和12.33%,其他品种都有所上升,其中‘佛奥’增幅最大为119.35%。随着低温胁迫的加剧,蒸腾速率(Tr)在−4 ℃出现明显下降,相较于CK各品种降幅基本一致,介于93.76%~96.80%。低温加剧过程中气孔限制值(Ls) 呈现先升后降再升的趋势,增加时峰值集中出现在16 ℃和12 ℃, ‘皮瓜尔’和‘阿尔波萨纳’增幅最大,分别为153.49%和137.04%(12 ℃)。水分利用效率( WUE )呈现先升后降再升的趋势,再次上升的拐点温度出现在4℃,相比对照‘阿尔波萨纳’降幅最大为56.04%。
-
由图3可见,在低温胁迫下,8个供试油橄榄品种的最大光化学效率(Fv/Fm)整体呈下降趋势。−4 ℃时,‘鄂植8号’较CK降幅较小为33.26%,而‘柯基’较CK降幅最大为50.55%。从16 ℃到4 ℃胁迫过程中,‘佛奥’和‘莱星’变化趋势一致且较为缓和。

图 3 低温胁迫过程中8种油橄榄幼苗叶绿素荧光参数的变化特征
Figure 3. The change characteristics of chlorophyll fluorescence parameters in eight olive seedlings under low-temperature stress
经低温胁迫,实际光化学效率(ΦPSⅡ)在0 ℃前变化趋势较为缓和,0 ℃至−4 ℃出现明显下降,‘阿尔波萨纳’、‘豆果’、‘鄂植8号’、‘佛奥’、‘莱星’和‘科拉蒂’、‘皮瓜尔’和‘柯基’降幅分别为63.20%、60.81%、56.70%、55.01%、62.15%、64.32%、60.35%、64.56%。
各参试品种的化学淬灭系数(qP)整体呈“W形”趋势,最低值出现在8 ℃和0 ℃,4 ℃时有上升趋势,在−4 ℃时骤升出现峰值。‘阿尔波萨纳’、‘豆果’、‘鄂植8号’、‘佛奥’、‘莱星’和‘科拉蒂’、‘皮瓜尔’和‘柯基’增幅分别为24.35%、24.09%、24.35%、13.41%、29.77%、28.69%、23.24%、30.11%。
随温度胁迫的加剧,各供试油橄榄品种的非化学淬灭系数(NPQ)值在22 ℃至0 ℃变幅度不大,介于1.558~3.118,0 ℃至−4 ℃出现急剧下降,降低至0.05左右。
-
采用隶属函数法对8个供试品种光合和叶绿素荧光参数的10个指标进行耐寒性综合评价。由表4可知,8个油橄榄品种的平均隶属度在0.41~0.71之间,从隶属函数综合评价值可得出耐寒性依次为‘科拉蒂’>‘豆果’>‘柯基’>‘鄂植8号’=‘佛奥’=‘莱星’>‘皮瓜尔’>‘阿尔波萨纳’。‘科拉蒂’的综合评价值高达0.71,耐寒性最强;‘阿尔波萨纳’的综合评价值仅为0.41,耐寒性最差。
表 4 低温胁迫下8种油橄榄幼苗测定指标的隶属函数值(光合参数)
Table 4. Membership function values of the eight olive seedlings under low-temperature stress (photosynthetic parameters)
测定指标
Determination index品种 Cultivar 阿尔波萨纳
Arbosana豆果
Arbequina鄂植8号
Ezhi 8佛奥
Frantoio莱星
Leccino科拉蒂
Coratina皮瓜尔
Picual柯基
Koroneiki净光合速率 (Pn)Net photosynthetic rate 0.36 0.94 0.38 0.52 0.48 0.63 0.63 0.36 气孔导度(Gs)Stomatal conductance 0.36 0.44 0.45 0.42 0.51 0.55 0.37 0.56 胞间二氧化碳浓度(Ci)Intercellular CO2 concentration 0.41 0.66 0.50 0.58 0.60 0.42 0.52 0.45 蒸腾速率(Tr)Transpiration rate 0.39 0.45 0.43 0.42 0.54 0.53 0.38 0.52 气孔限制值(Ls)Stomatal limit 0.65 0.34 0.59 0.58 0.41 0.40 0.49 0.47 水分利用效率(WUE)Water use efficiency 0.50 0.34 0.56 0.55 0.45 2.52 0.47 0.60 最大光能转化效率(Fv/Fm)Maximum light energy conversion efficiency 0.39 0.44 0.47 0.46 0.44 0.38 0.39 0.38 有效光化学量子产量(ΦPSⅡ )Effective photochemical quantum yield 0.33 0.50 0.50 0.50 0.50 0.50 0.33 0.56 光化学淬灭系数(qP)Photochemical quenching coefficients 0.62 0.49 0.41 0.41 0.51 0.63 0.62 0.64 非光化学淬灭系数(NPQ)Non-photochemical quenching coefficient 0.11 0.52 0.58 0.44 0.50 0.50 0.58 0.50 平均值 Average 0.41 0.51 0.49 0.49 0.49 0.71 0.48 0.50 耐寒性排序 Order 6 2 4 4 4 1 5 3 -
冷胁迫时,植物细胞中细胞膜最先受到伤害,导致细胞膜电解质外渗,且随着伤害程度的增加,离子渗出率升高,利用相对电导率结合Logistic曲线方程获得植物的半致死温度是一种有效且简便的耐寒性评价方法,该方法已在金光杏梅、花椒、葡萄等诸多植物的耐寒性评价中得到应用[17-19]。本试验中,随着温度从22 ℃降到0 ℃时,油橄榄叶片电解质在缓慢渗出(相对电导率35%左右),当温度从0 ℃降低到−4 ℃时,‘柯基’、‘佛奥’、‘阿尔波萨纳’和‘鄂植8’号叶片相对电导率分别升高至76.63%、72.50%、73.27%和73.00%,说明这4个品种细胞膜受到伤害较大,而‘豆果’、‘皮瓜尔’、‘科拉蒂’和‘莱星’叶片相对电导率均在70%以下。通过Logistic方程对不同品种的处理温度和叶片相对电导率进行拟合,试验中8个油橄榄品种,半致死温度(LT50)介于−16.359~−9.715之间,‘豆果’耐寒性最好,‘柯基’最差,供试品种中‘莱星’、‘鄂植8号’、‘佛奥’的耐寒性排序与令凡等人的研究结果一致[20]。
MDA是植物脂膜过氧化的重要产物之一,积累会使脂膜在逆境中的损伤加剧[21],通过比较MDA含量及其变化程度,可以反映出8个油橄榄品种在低温中的受损程度。本研究中,8 ℃之后‘柯基’MDA含量上升幅度显著高于其它7个品种,说明‘柯基’细胞膜氧化程度更大,符合半致死温度以及耐寒性综合评价结果。
-
Chl、SS、SP、Pro、POD、SOD、CAT等指标虽然都与植物耐寒性关系密切,但是由于植物是一个有机整体,遭受低温胁迫而引起生理生化指标变化也是错综复杂的,因此用单一指标来评价植物耐寒性太过片面。当然,想要准确评价某一种植物耐寒性所应用的指标体系也有所不同,例如细胞膜系中不饱和脂肪酸的变化就不能用于评价苹果(Malus pumila Mill.)、菜蓟(Cynara scolymus)、西蕃莲属(Passiflora L. )植物的耐寒性;脯氨酸含量的累积无法用来评价柑橘属植物的抗冷性。冷胁迫条件下,植物体内会积累大量超氧自由基,从而破坏植物膜系统,抗氧化酶系统可以清除超氧自由基,从而避免植物膜系统在冷害下遭到破坏[22]。本研究中,8个油橄榄品种抗氧化酶活性随着温度的降低呈先上升后下降的趋势,说明抗氧化酶系统在油橄榄耐低温过程中作用明显,但当温度降低到0 ℃以下时,其抗氧化酶系统逐渐失去作用,从而导致活性降低。从本研究中抗氧化酶活性的上升幅度看,‘柯基’上升幅度均最小,说明抗氧化酶系统对低温的响应最不敏感,这可能是导致‘柯基’耐寒性表现不佳的原因之一。相反,耐寒性表现良好的‘豆果’和‘皮瓜尔’等抗氧化酶活性的上升幅度更大。为克服单一指标在耐寒性鉴定中的不足,试验采用8个生理指标利用隶属函数法对其耐寒性进行综合评价,耐寒性强弱顺序为:‘豆果’>‘皮瓜尔’>‘科拉蒂’>‘莱星’>‘鄂植8号’>‘阿尔波萨纳’>‘佛奥’>‘柯基’。
-
光系统的破坏程度也可以用来判定植物的耐寒性。随着低温胁迫加剧,‘鄂植8号’和‘莱星’的 qP 呈下降趋势,NPQ 呈上升趋势,说明低温胁迫严重破坏了‘鄂植8号’和‘莱星’的光合电子传递途径,使得光合电子传递能力不断降低,用于光化学反应的光能部分减少,而以热形式耗散掉的光能部分不断增加。但其热耗散增加缓解了光抑制对其光合功能产生的破坏,增强了光合反应中心的稳定性,从而能减轻低温胁迫对其叶片光合器官的损伤。本研究通过测定8种油橄榄幼苗的光合及叶绿素荧光等相关指标,并利用隶属函数法对其耐寒性做了初步评价,结果为:‘科拉蒂’>‘豆果’>‘柯基’>‘鄂植8号’=‘佛奥’=‘莱星’>‘皮瓜尔’>‘阿尔波萨纳’。
-
低温是限制油橄榄在我国北亚热带扩区发展的主要因素。研究油橄榄幼苗膜系统、渗透调节物质、抗氧化酶系统、光系统对低温胁迫的响应,是低温适应性品种选育至关重要的一步。从评价结果来看,电导率拟合半致死温度评价方法和耐寒相关生理指标隶属函数法评价结果接近,更符合各品种采样区越冬情况。而以光合和叶绿素荧光指标体系的耐寒性评价方法与前2种方法评价结果差异较大,可能与油橄榄叶片近轴表皮角质膜较厚,蜡质结晶致密,气孔密度小等叶片重要形态特征有关[23]。因此评定油橄榄耐寒性时,需多方面综合评价,同时结合田间观察,才能使结果更加准确、科学。
-
通过Logistic方程拟合半致死温度,渗透调节物质、保护酶活性参数,光合和叶绿素荧光参数等指标分析,对8个油橄榄品种进行耐寒性评价,发现油橄榄幼苗膜系统、渗透调节物质、抗氧化酶系统、光系统对低温胁迫的响应并不一致。渗透调节物质、保护酶活性参数隶属函数法所得出耐寒性综合排序与应用电导法配合Logistic方程求出半致死温度的排序基本一致,且符合各品种田间越冬表现,该方法更适合作为油橄榄苗期耐寒性评价方法。利用光合及叶绿素荧光参数10个指标的隶属函数评价方法,很难准确评价油橄榄苗期耐寒性,尤其是难以区分耐寒性差异较小的品种。
8个油橄榄品种扦插苗苗期耐寒性评价
Evaluation of Cold Tolerance of Eight Olive Varieties in Cuttage Seedlings
-
摘要:
目的 为探明油橄榄扦插苗苗期抗寒性评价方法。 方法 以中国北亚热带西秦岭南坡白龙江河谷地引种栽植的8个油橄榄品种2年生扦插苗为研究对象,人工模拟冷胁迫(16、12、8、4、0、−4 ℃),对其渗透调节物质含量,保护酶活性,光合和叶绿素荧光参数等指标进行分析。 结果 随着冷胁迫加剧,8个供试油橄榄品种幼苗叶片相对电导率(REC)、脯氨酸(Pro)、可溶性糖(SS)、可溶性蛋白(SP)含量呈上升趋势,超氧化物歧化酶(SOD)、过氧化物酶(POD)、过氧化氢酶(CAT)活性在0 ℃前呈上升趋势,降至冰点后又开始逐渐降低;温度下降的过程中,各品种叶片叶绿素含量(Chl)、净光合速率(Pn)、蒸腾速率(Tr)、最大光化学效率(Fv/Fm)、实际光化学效率(ΦPSⅡ)均呈现下降趋势,气孔导度( G s)在4 ℃前呈下降趋势。应用半致死温度(LT50),渗透调节物质、保护酶活性参数隶属函数,光合和叶绿素荧光参数隶属函数3种评价体系进行了相关分析,8个油橄榄品种扦插苗半致死温度介于−16.359~−9.715 ℃之间。 结论 通过渗透调节物质、保护酶活性参数隶属函数法所得出的耐寒性综合排序与应用电导法配合Logistic方程求出半致死温度的排序基本一致,并且符合试验地区油橄榄苗期越冬表现,可以作为油橄榄苗期耐寒性评价方法。 Abstract:Objective To investigate the evaluation method of cold resistance of olive cuttings. Methods Eight two-year cuttage seedlings of olive varieties were introduced and planted in the valley of Bailong River on the southern slope of West Qinling Mountains in North subtropical China. Cold stress (16, 12, 8, 4, 0, −4 ℃) was simulated to measure the contents of osmotic regulation substances, protective enzyme activities, photosynthesis and chlorophyll fluorescence parameters. Results With the increase of cold stress, the contents of relative electrical conductivity (REC), proline (Pro), soluble sugar (SS) and soluble protein (SP) in the leaves of 8 tested olive varieties showed an increasing trend, and the activities of superoxide dismutase (SOD), peroxidase (POD) and catalase (CAT) increased before 0 ℃ and then began to gradually decreased after freezing point; During the process of temperature decrease, leaf chlorophyll content (Chl), net photosynthetic rate (Pn), stomatal conductance (Gs), intercellular CO2 concentration (Ci), transpiration rate (Tr), maximum photochemical efficiency (Fv/Fm) and actual photochemical efficiency (ΦPSⅡ) of all varieties showed a decreasing trend,stomatal conductance (Gs) showed a decreasing trend before -4℃. Correlation analysis was conducted using three evaluation systems: semi-lethal temperature (LT50), membership functions of osmotic regulatory substances and protective enzymes, and membership functions of photosynthesis and chlorophyll fluorescence. The results showed that the semi-lethal temperature of eight olive varieties ranged from -16.359 ℃ to -9.715 ℃. Conclusion The comprehensive ranking of cold resistance obtained by the method of subordinate function of the activity parameters of osmotic regulatory substances and protective enzymes is basically consistent with the ranking of semi-lethal temperature obtained by the method of conductivity and Logistic equation, and is consistent with the overwintering performance of olive in the test area. It can be used as an evaluation method for cold resistance of olive at seedling stage. -
Key words:
- olive
- / cold tolerance
- / cold stress
-
表 1 供试油橄榄材料基本情况
Table 1. Information of the test materials of olive seedlings
品种
Cultivar中文译名
Chinese叶长
Leaf length/mm叶宽
Leaf width/mm叶间距
Blade spacing/mm叶厚度
Leaf thickness/mm株高
Plant height/cm茎粗
Stemdia meter/mmArbequina 豆果 51.077 ± 2.729 bc 11.783 ± 1.021 ab 23.553 ± 2.362 ab 0.470 ± 0.036 a 27.367 ± 1.198 a 3.413 ± 0.263 a EZ-8 鄂植8号 50.920 ± 1.506 bc 11.043 ± 0.582 a 25.813 ± 4.445 ab 0.483 ± 0.035 a 30.767 ± 1.453 ab 3.577 ± 0.212 a Frantoio 佛奥 44.043 ± 1.975 a 10.840 ± 0.135 a 28.757 ± 5.191 b 0.467 ± 0.012 a 30.167 ± 4.253 ab 3.730 ± 0.433 a Leccino 莱星 47.233 ± 0.994 ab 11.057 ± 0.734 a 26.393 ± 2.620 ab 0.483 ± 0.032 a 35.233 ± 2.904 b 3.443 ± 0.437 a Koroneiki 柯基 53.810 ± 3.337 c 13.100 ± 0.894 b 22.613 ± 2.121 a 0.567 ± 0.021 b 33.700 ± 1.955 ab 3.500 ± 0.360 a Picual 皮瓜尔 52.523 ± 3.496 bc 11.933 ± 1.708 ab 27.270 ± 1.259 ab 0.563 ± 0.047 b 31.933 ± 0.689 ab 3.743 ± 0.064 a Coratina 科拉蒂 52.507 ± 2.381 bc 10.563 ± 0.108 a 25.207 ± 0.454 ab 0.577 ± 0.031 b 33.700 ± 1.457 ab 3.650 ± 0.437 a Arbosana 阿尔波萨纳 51.250 ± 4.280 bc 10.917 ± 1.042 a 26.097 ± 1.931 ab 0.617 ± 0.021 b 33.200 ± 1.305 ab 3.893 ± 0.072 a 注:表中数值为平均值 ± 标准误(n=3),不同小写字母表示同一品种不同处理间在0.05水平上差异显著(P<0.05)
Notes: The values in the table are the mean ± standard error (n=3), and the different lowercase letters indicate the significant differences in the 0.05 level between the different treatments of the same variety (P <0.05)表 2 参试品种半致死温度
Table 2. Semi-lethal temperature of tested varieties
品种
CultivarLogistic方程
Logistic equationR2 LT50 / ℃ 阿尔波萨纳
ArbosanaY=100/(1 + 8.123e−0.190x) 0.964 9** −11.019 ± 1.031 bc 豆果
ArbequinaY=100/(1 + 11.333e−0.148x) 0.982 5** −16.359 ± 1.225 a 鄂植8
Ezhi8Y=100/(1 + 7.478e−0.175x) 0.972 4** −11.517 ± 0.879 bc 佛奥
FrantoioY=100/(1 + 7.622e−0.176x) 0.964 4** −11.534 ± 0.586 bc 莱星
LeccinoY=100/(1 + 9.335e−0.166x) 0.965 2** −13.481 ± 1.125 b 科拉蒂
CoratinaY=100/(1 + 8.575e−0.155x) 0.932 8* −13.836 ± 1.111 b 皮瓜尔
PicualY=100/(1 + 9.441e−0.156x) 0.925 5* −14.410 ± 1.263 ab 柯基
KoroneikiY=100/(1 + 7.766e−0.211x) 0.932 8* −9.715 ± 0.774 c 注:*和**表示相关系数达显著和极显著水平。同一列中的不同小写字母表示差异显著(p<0.05)
Notes: *means significant difference at p<0.05;**means significant difference at p<0.01. Values within a column followed by different letters are significantly different at p<0.05. The same below表 3 低温胁迫下8种油橄榄幼苗测定指标的隶属函数值
Table 3. Membership function values of the eight olive seedlings under low-temperature stress
指标
Indexes品种 Cultivar 阿尔波萨纳
Arbosana豆果
Arbequina鄂植8号
Ezhi 8佛奥
Frantoio莱星
Leccino科拉蒂
Coratina皮瓜尔
Picual柯基
Koroneiki相对电导率 Relative electric conductivity 0.52 0.54 0.69 0.00 0.66 0.83 0.99 1.00 叶绿素 Chlorophyll content 0.70 1.00 0.89 0.50 0.92 0.93 0.97 0.00 可溶性糖 Soluble sugar 0.16 1.00 0.29 0.03 0.36 0.43 0.82 0.00 可溶性蛋白 Soluble protein 0.25 1.00 0.26 0.04 0.35 0.52 0.43 0.00 脯氨酸 Proline content 0.24 0.84 0.20 0.04 0.36 0.35 1.00 0.00 丙二醛含量 MDA content 0.70 0.00 0.69 0.89 0.49 0.39 0.17 1.00 SOD活性 SOD activity 0.34 0.96 0.64 0.00 0.94 0.94 1.00 0.02 POD活性 POD activity 0.86 1.00 0.88 0.82 0.90 0.91 0.93 0.00 CAT活性 CAT activity 0.37 1.00 0.53 0.11 0.62 0.66 0.76 0.00 平均隶属度 Average degree of membership 0.46 0.82 0.56 0.27 0.62 0.66 0.78 0.22 耐寒排序 Order of cold resistance 6 1 5 7 4 3 2 8 表 4 低温胁迫下8种油橄榄幼苗测定指标的隶属函数值(光合参数)
Table 4. Membership function values of the eight olive seedlings under low-temperature stress (photosynthetic parameters)
测定指标
Determination index品种 Cultivar 阿尔波萨纳
Arbosana豆果
Arbequina鄂植8号
Ezhi 8佛奥
Frantoio莱星
Leccino科拉蒂
Coratina皮瓜尔
Picual柯基
Koroneiki净光合速率 (Pn)Net photosynthetic rate 0.36 0.94 0.38 0.52 0.48 0.63 0.63 0.36 气孔导度(Gs)Stomatal conductance 0.36 0.44 0.45 0.42 0.51 0.55 0.37 0.56 胞间二氧化碳浓度(Ci)Intercellular CO2 concentration 0.41 0.66 0.50 0.58 0.60 0.42 0.52 0.45 蒸腾速率(Tr)Transpiration rate 0.39 0.45 0.43 0.42 0.54 0.53 0.38 0.52 气孔限制值(Ls)Stomatal limit 0.65 0.34 0.59 0.58 0.41 0.40 0.49 0.47 水分利用效率(WUE)Water use efficiency 0.50 0.34 0.56 0.55 0.45 2.52 0.47 0.60 最大光能转化效率(Fv/Fm)Maximum light energy conversion efficiency 0.39 0.44 0.47 0.46 0.44 0.38 0.39 0.38 有效光化学量子产量(ΦPSⅡ )Effective photochemical quantum yield 0.33 0.50 0.50 0.50 0.50 0.50 0.33 0.56 光化学淬灭系数(qP)Photochemical quenching coefficients 0.62 0.49 0.41 0.41 0.51 0.63 0.62 0.64 非光化学淬灭系数(NPQ)Non-photochemical quenching coefficient 0.11 0.52 0.58 0.44 0.50 0.50 0.58 0.50 平均值 Average 0.41 0.51 0.49 0.49 0.49 0.71 0.48 0.50 耐寒性排序 Order 6 2 4 4 4 1 5 3 -
[1] 徐纬英. 中国油橄榄─种质资源利用[M]. 长春: 长春出版社, 2001. [2] LOUREIRO J, RODRIGUEZ E, COSTA A, et al. Nuclear DNA content estimations in wild olive (Olea europaea L. ssp. europaea var. sylvestris Brot. ) and Portuguese cultivars of O. europaea using flow cytometry[J]. Genet Resour Crop Evol, 2007, 54: 21-25. doi: 10.1007/s10722-006-9115-3 [3] D’ANGELI S, MALHÓ R, ALTAMURA M M. Low-temperature sensing in olive tree: calcium signalling and cold acclimation[J]. Plant Science, 2003, 165: 1303-1313. doi: 10.1016/S0168-9452(03)00342-X [4] 张正武. 低温冻害对油橄榄生长发育的影响及其防御措施[J]. 经济林研究, 2018, 36(3):48-56. doi: 10.14067/j.cnki.1003-8981.2018.03.008 [5] 令 凡, 焦 健, 杨北胜, 等. 6个品种油橄榄幼苗耐寒性及其与耐寒指标的灰色关联度分析[J]. 四川农业大学学报, 2016, 34(2):167-184. [6] 杨振亚, 赵建诚, 袁金玲, 等. 5个观赏雷竹变型对低温胁迫的生理响应[J]. 林业科学研究, 2021, 34(2):131-140. doi: 10.13275/j.cnki.lykxyj.2021.02.014 [7] LEE D H, LEE C B. Chilling stress induced changes of antioxidant enzymes in the leaves of cucumber in gelenzyme activity assays[J]. Plant Science, 2000, 159(1): 75-85. doi: 10.1016/S0168-9452(00)00326-5 [8] 江锡兵, 宋跃朋, 马开峰, 等. 低温胁迫下美洲黑杨与大青杨杂种无性系若干生理指标变化研究[J]. 北京林业大学学报, 2012, 34(1):58-63. [9] HUTCHISON R S,GROOM Q,ORT D R. Differential effects of chilling induced photooxidation on the redox regulation of photosynthetic enzymes[J]. Biochemistry, 2000, 39(22): 6679-6688. doi: 10.1021/bi0001978 [10] GÓMEZ M,BARRANCO D. Field evaluation of frost tolerance in 10 olive cultivars[J]. Plant Genetic Resources, 2005, 3(3): 385-390. doi: 10.1079/PGR200592 [11] CANSEV A,GULEN H,ERIS A. Cold-hardiness of olive (Olea europaea L. ) cultivars in cold-acclimated and non-acclimated stages: seasonal alteration of antioxidative enzymes and dehydrin-like proteins[J]. Journal of Agricultural Science, 2009, 147: 51-61. doi: 10.1017/S0021859608008058 [12] 顾 姻, 孙醉君, 毕绘蟾, 等. 油橄榄的适应性育种—实生选育和经济性状早期鉴定的研究[J]. 南京林产工业学院学报, 1981, 2:69-78. [13] 陈明辉, 程世平, 张志录, 等. 低温胁迫下不同果蔗品种光合及荧光特性的变化及耐寒性评价[J]. 热带作物学报, 2018, 39(3):466-471. [14] 邹 娅, 米文博, 徐明霞, 等. 低温胁迫下北方强冬性区甘蓝型冬油菜的低温光合生理特征[J]. 甘肃农业大学学报, 2021, 56(2):105-113. [15] BEN-ARI G,BITON I,MANY Y, et al. Elevated temperatures negatively affect olive productive cycle and oil quality[J]. Agronomy, 2021, 11(8): 1492. doi: 10.3390/agronomy11081492 [16] DAVIDE G,ANTONELLA L,PAOLO B, et al. Transcriptome changes associated with cold acclimation in leaves of olive tree (Olea europaea L. )[J]. Tree Genetics & Genomes, 2015, 11(6): 11. [17] 周会萍, 蔡祖国. 应用电导率法及Logistic方程测定金光杏梅耐寒性研究[J]. 北方园艺, 2011(18):39-41. [18] 刘 冰, 王有科. 应用Logistic方程确定花椒枝条低温半致死温度[J]. 甘肃农业大学学报, 2005, 40(4):475-479. doi: 10.3969/j.issn.1003-4315.2005.04.012 [19] 谢丽芬, 李连国, 李晓燕, 等. 几个引种葡萄品种耐寒性的研究[J]. 内蒙古农业大学学报, 2007, 28(4):116-119. [20] 令 凡, 李朝周, 回振龙, 等. 应用电导率法及Logistic方程测定油橄榄品种的耐寒性[J]. 广东农业科学, 2015(1):13-17. [21] 王玲丽, 贾文杰, 马璐琳, 等. 低温胁迫对不同百合主要生理指标的影响[J]. 植物生理学报, 2014, 50(9):1413-1422. [22] SCANDALIOS J G. Oxygen stress and super oxide dismutases[J]. Plant Physiology, 1993, 101(1): 7-12. doi: 10.1104/pp.101.1.7 [23] 王家训. 耐寒性不同的油橄榄品种和单株叶片扫描电镜观察[J]. 武汉植物学研究, 1986, 4(1):27-30. -




 下载:
下载: