-
林以种为本,种以质为先。林木种质资源是林业种业发展的基础,是林业生产力发展的基础性资源和国家战略性资源,随着中国林业种业创新力度的不断加大,愈发重视各类林木种质资源的保护和利用[1]。然而数量庞大的种质资源会影响种质的保存、评价和利用,特别是多年生林木种质,其树体高大、个体占地面积广、管理成本高,不便于种质资源的有效管理和深入研究[2-4]。因此,Frankel和Brown等提出并逐步发展了核心种质的概念,即运用一定的策略选取最小的种质资源数量以最大程度地代表种质资源的遗传多样性[5-6]。核心种质的构建主要基于表型性状[7-8]或基于分子标记[9-11]。对于树体高大、多年生林木来说,以DNA多态性为基础的分子标记不易受林木生长期和环境的影响,较表型性状更适合其核心种质的构建[3, 12]。目前利用分子标记的方法已在杜仲(Eucommia ulmoides Oliv.)[2]、核桃(Juglans sigillata Dote)[3]、杉木(Cunninghamia lanceolata (Lamb.) Hook)[4, 13]、毛白杨(Populus tomentosa Carr.)[10]、美洲黑杨(P. deltoides Marsh.)[14]、板栗(Castanea mollissima Bl.)[15]、木荷(Schima superba Gardn. et Champ.)[16]、红锥(Castanopsis hystrix Miq.)[17]、刺槐(Robinia pseudoacacia L.)[18]等林木上建立了核心种质。
杉木是我国重要的乡土针叶用材树种,主要分布于我国长江流域、秦岭以南地区。20世纪70年代起,江西省开始收集保存杉木优树种质,建立来源丰富的种质资源库,进行遗传改良工作[19]。持续的种质资源收集为杉木种质创新和遗传改良提供了丰富的材料,但日益剧增的种质资源数量不利于种质资源的保存、评价、创新研究及开发利用[4, 19]。因此江西杉木核心种质的构建对充分利用现有江西杉木种质资源具有重要意义。同时目前的杉木种质资源收集、保存中由于缺乏统一、规范的编目工作等,导致存在本底不清,重复收集保存等问题[20],故开展种质鉴定、分子身份证构建等工作对杉木种质资源的收集、保存和利用十分重要。本研究通过SSR标记分析现有的江西杉木种质资源遗传多样性,构建核心种质,并根据SSR分子指纹图谱、种质资源信息等绘制核心种质分子身份证,为今后江西杉木种质资源的研究与利用提供理论依据和核心材料。
-
试验材料来自江西省安福县陈山林场和信丰县林木良种场国家级杉木良种基地种质资源库,包括江西地方特色杉木优良种源-安福陈山红心杉优树种质群体(安福群体,AF)、赣南地区杉木优树种质群体(赣州群体,GZ)和江西本省其他地区杉木优树种质群体(其他群体,QT)。其中安福陈山红心杉种质群体165份,其主要来自罗霄山脉陈山林区;赣南地区杉木优树种质群体224份,其主要来自江西南部赣州全南、龙南、信丰等地;江西本省其他地区杉木优树种质群体106份,其主要来自江西铜鼓、吉安、上饶、景德镇等地。参试495份材料均为优树无性系材料。
2021年4月,采集健康且无病虫害的新叶,冰袋保存带回实验室放置−80 ℃低温冰箱保存备用。
-
采用改良CTAB法提取杉木新叶DNA,在完成质量及浓度检测后,定量至约30.0 ng·µL−1,−20 ℃保存备用。
基于文献检索及课题组前期的杉木SSR引物开发,最终筛选了20对SSR引物用于后续分析 [19]。SSR引物由北京睿博兴科生物技术有限公司合成,在每对引物的正向引物5′端进行M13 (5'-TGTAAAACGACGGCCAGT-3′)修饰,然后合成3′端具有荧光的M13接头(FAM、HEX),通过序列互补进行标记。SSR-PCR体系(20.0 μL):DNA模板2.0 μL,正向引物和反向引物各0.5 μL,2 × Taq plus PCR Master Mix 10.0 μL,ddH2O 7.0 μL。PCR反应程序:95 ℃ 5 min;95 ℃ 30 s,55 ℃ 30 s,72 ℃ 30 s,35 个循环;72 ℃ 7 min。荧光引物扩增产物送北京睿博兴科生物技术有限公司进行分析。
-
运用PopGene 32软件开展遗传多样性分析,主要参数包括等位基因数(Na)、有效等位基因数(Ne)、Nei’s遗传多样性指数(H)和Shannon’s信息指数(I)等,利用PIC-Calc软件计算SSR标记的多态信息含量(PIC)。通过Ntsys软件采用UPGMA进行聚类分析,构建树状图。
-
利用Core finder软件[21],以等位基因数最大化(M策略)为原则对SSR数据进行分析,从供试江西杉木材料中抽取核心种质。核心种质构建完成后,对构建的核心种质的相关遗传参数进行t检验来评价核心种质的代表性。同时通过主坐标分析(PCoA)对构建的核心种质进行确认。
-
依据SSR标记PIC值的高低,依次增加标记数量进行核心种质的UPGMA聚类分析,筛选能实现所有核心种质有效区分所需的最少SSR标记组合,以这组SSR标记作为高效标记组,用于后续核心种质SSR分子指纹图谱和分子身份证的构建。将高效SSR标记组在核心种质中检测到等位基因,按小到大的顺序排序,然后用数字1~9进行编码,若等位基因数大于9时,则用A~Z编码,缺失位点用0表示,构建每个核心种质的SSR分子指纹图谱。将种质信息和SSR分子指纹图谱相结合,分别利用条码生成器和二维码生成器构建江西杉木核心种质的分子身份证。
-
利用SSR标记对江西杉木种质进行分析以探究其遗传多样性,结果发现(表1):20个SSR标记在495份江西杉木种质中共检测到等位基因数(Na)122个,平均为6.1个位点,其中CLSSR33标记最少,仅有2个,CLSSR9标记最多,达15个。所选择的20个标记中,获得等位基因数(Na)在5个以上的标记有16个,表明本研究选择的SSR标记位点多态性较好,可用于江西杉木种质的遗传多样性分析。此外,20个标记位点的有效等位基因数(Ne)变化范围在1.014~3.405之间,平均值为1.836;Shannon’s信息指数(I)变化范围为0.045~1.428,平均值为0.762;Nei’s遗传多样性指数(H)变化范围在0.014~0.706之间,平均值为0.400;观测杂合度(Ho)和期望杂合度(He)均值分别为0.394和0.400,Ho < He;位点多态性信息含量(PIC)的变化范围为0.014~0.657,平均值为0.357,其中低度多态性位点6个(PIC≤0.25);中度多态性位点11个(0.25<PIC < 0.5);高度多态性位点3个(PIC≥0.5)。以上结果表明495份江西杉木种质的遗传多样性较丰富。
表 1 江西杉木495份种质遗传多样性参数
Table 1. The genetic diversity parameters of C. lanceolata germplasms from Jiangxi
引物
Primer等位基因数
Na有效等位基因数
NeShannon’s信息指数
INei’s遗传多样性指数
H观测杂合度
Ho期望杂合度
He多态性信息含量
PICCLSSR1 3 1.168 0.289 0.144 0.127 0.144 0.135 CLSSR9 15 2.332 1.426 0.571 0.582 0.572 0.554 CLSSR10 6 1.329 0.572 0.248 0.240 0.248 0.237 CLSSR13 7 1.261 0.420 0.207 0.204 0.207 0.191 CLSSR19 6 1.603 0.761 0.376 0.370 0.377 0.349 CLSSR20 5 1.800 0.797 0.445 0.400 0.445 0.396 CLSSR21 5 1.667 0.608 0.400 0.424 0.401 0.323 CLSSR33 2 1.232 0.336 0.188 0.210 0.188 0.170 CLSSR37 5 2.315 0.927 0.568 0.550 0.569 0.474 CLSSR38 6 1.804 0.734 0.446 0.493 0.446 0.365 CLSSR40 3 1.014 0.045 0.014 0.014 0.014 0.014 CLSSR50 3 1.063 0.143 0.059 0.057 0.059 0.057 H7 7 2.136 0.939 0.532 0.527 0.532 0.469 H8 5 2.181 0.880 0.542 0.495 0.542 0.437 H16 6 1.864 0.846 0.464 0.483 0.464 0.410 H33 5 1.800 0.863 0.444 0.440 0.445 0.404 H76 8 2.096 0.984 0.523 0.509 0.524 0.460 H97 10 3.405 1.428 0.706 0.651 0.707 0.657 H201 6 1.975 0.954 0.494 0.501 0.494 0.448 H286 9 2.672 1.279 0.626 0.608 0.626 0.585 均值 Mean 6.1 1.836 0.762 0.400 0.394 0.400 0.357 -
利用Core Finder软件,采用M策略进行抽样构建核心种质,结果表明当抽取种质数量为52份时,等位基因保留比例接近100%。因此,基于SSR基因型数据从495份江西杉木种质中抽取52份核心种质,抽样比例为10.5%,其中安福陈山红心杉种质10份,赣南地区种质20份,江西其他地区的种质22份。
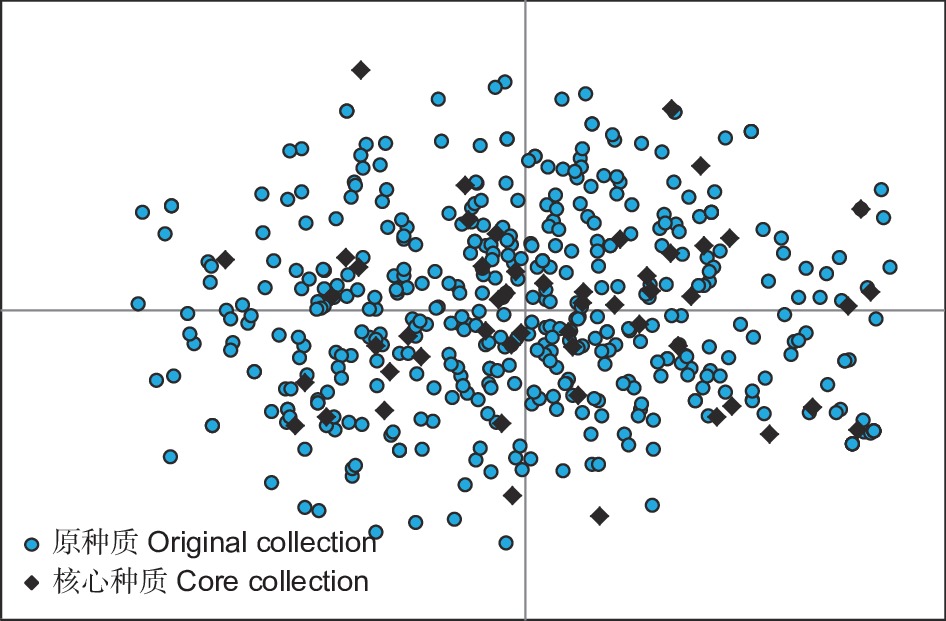
通过遗传多样性参数分析对构建的江西杉木52份核心种质的代表性进行评价,结果表明(表2),与原种质比较,核心种质的等位基因数(Na)、有效等位基因数(Ne)、Shannon’s信息指数(I)、Nei’s遗传多样性指数(H)、观测杂合度(Ho)、期望杂合度(He)和多态信息含量(PIC)的保留比例依次为100.0%、107.4%、115.1%、109.0%、104.1%、110.0%和111.2%,且t检验显示核心种质与原种质间各遗传多样性参数差异不显著,说明构建的核心种质很好的保留了原种质的遗传多样性,因此初步认为52份核心种质能够代表495份原种质。PCoA对核心种质作进一步确认,结果显示,江西杉木52份核心种质较为均匀地分布在495份原种质中(图1),说明构建的核心种质具有较好的代表性。
表 2 江西杉木核心种质与原种质的遗传多样性比较
Table 2. The genetic diversity comparison between core collection and original collection of C. lanceolata germplasms from Jiangxi
种质
Germplasm数量
Number等位基因数
Na有效等位基因数
NeShannon’s信息指数
INei’s遗传多样性指数
H观测杂合度
Ho期望杂合度
He多态信息含量
PIC原种质 495 6.1 1.836 0.762 0.400 0.394 0.400 0.357 核心种质 52 6.1 1.972 0.877 0.436 0.410 0.440 0.397 (百分比) (10.5%) (100.0%) (107.4%) (115.1%) (109.0%) (104.1%) (110.0%) (111.2%) t 0.6696 0.9192 0.5987 0.2592 0.5150 0.7283 p 0.5072 0.3638 0.5529 0.7969 0.6573 0.4709 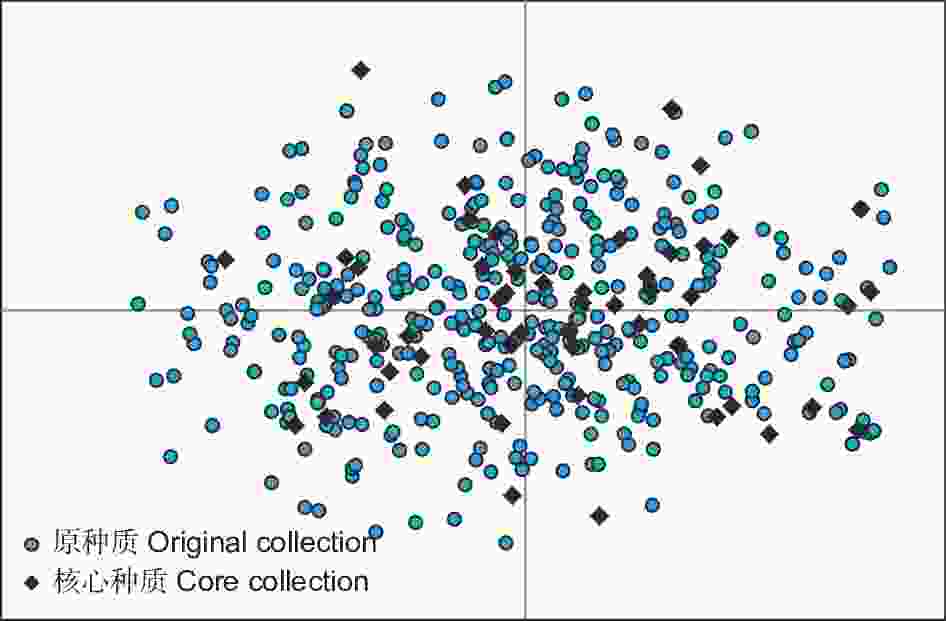
图 1 江西杉木核心种质PCoA分析
Figure 1. The principal coordinates analysis of core collection of C. lanceolata germplasms from Jiangxi
基于聚类分析52份核心种质可分为6大类。其中,核心种质QT065、QT099和GZ012均单独形成一类;核心种质GZ051和GZ209则形成一类,QT059和QT063组成一类;其余45份核心种质则形成一大类。
-
由于杉木为二倍体,每个SSR位点应由2个相同或不同的等位基因组成。SSR标记的等位基因数、基因型越多,PIC值越高,能区分种质的能力也越强,在绘制指纹图谱中价值也越高。基于最少标记区分最多种质的原则,依据SSR标记的PIC值的高低,依次增加标记数量对核心种质进行区分,结合UPGMA聚类,结果发现H97标记与H286、CLSSR9和CLSSR37相结合,就可将52份江西杉木核心种质完全鉴别区分(图2)。
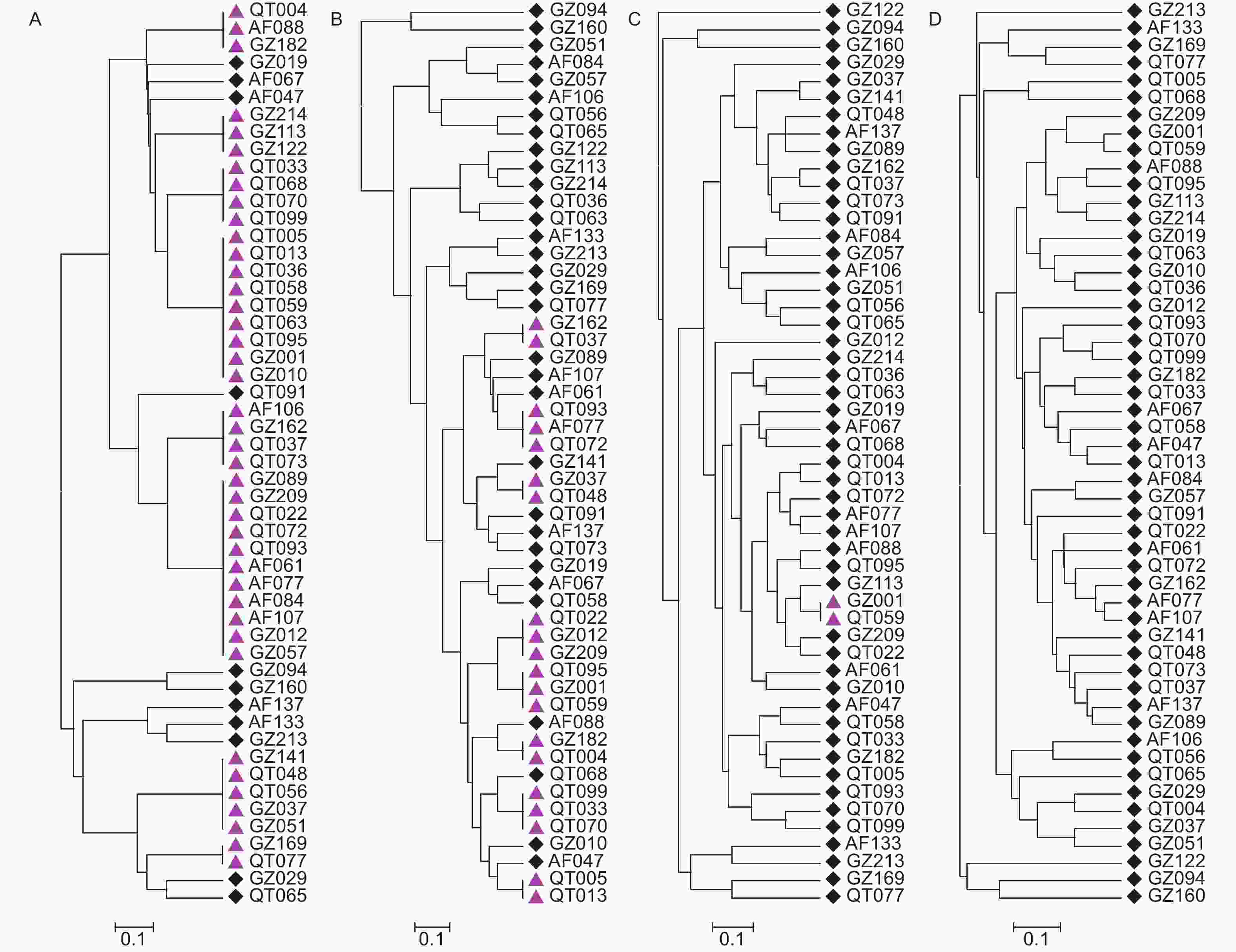
图 2 基于UPGMA聚类的江西杉木核心种质鉴别分析
Figure 2. The identification of core collection of the C. lanceolata germplasms from Jiangxi by UPGMA
通过H97、H286、CLSSR9和CLSSR37这4个高效SSR标记在52份核心种质中检测到的等位基因,构建每份核心种质的SSR分子指纹图谱(图3)。将获得SSR分子指纹图谱数据与种质信息编码一同构建核心种质特异的分子身份证码。参考王华缄等[20],种质信息编码共有6位数字组成,分为3个部分,第1~3位表示种质原产地信息,如001为江西省安福县;第4位是种质资源类别,1表示一代优树,2表示二代优树、3表示三代优树等;第5~6位表示收集、保存时间,如79表示1979年。若上述信息未知或不清楚则用X表示。以AF047为例(图4),其分子身份证号码为00110668444B34,表示该种质原产地江西省安福县,收集、保存的为1代优树,时间为2006年,4个核心标记(H97、H286、CLSSR9和CLSSR37)的指纹图谱依次为68/44/4B/34。最后利用每份种质的14位分子身份证编号,分别制作条形码和二维码(图4)。
-
进行遗传多样性评价是开展种质资源评价工作的重要组成部分。开展杉木种质资源的遗传多样性研究对收集、保存、评价和利用杉木种质材料的意义重大。江西是我国杉木的主要的分布和中心产区之一,栽培历史悠久,在长期的自然选择和人工选择作用下形成一些颇具特色的优良种质资源,如安福“陈山红心杉”、武宁“瓜源木”、遂川“龙泉木”、全南“黄田江杉木”等[22],使得江西拥有丰富的杉木种质资源。本研究采用20个SSR标记在495份江西杉木种质中共检测到122个等位基因(Na),平均Shannon’s信息指数(I)、平均Nei’s遗传多样性指数(H)、平均观测杂合度(Ho)和平均期望杂合度(He)分别为0.762、0.400、0.394和0.400,与其他采用相同技术进行的杉木相关研究结果比较[4, 13, 23-24],江西杉木种质资源具有较丰富的遗传多样性。
在林木育种中,核心种质在亲本选择、杂交育种、种质保存和利用等方面发挥着重要作用。核心种质是通过从整个种质资源中选择出少量且具有代表性的种质材料,可以最大程度的代表原种质的遗传多样性水平。因此,在构建核心种质中应优先考虑选择稀有位点,最大限度保留原种质的等位基因多样性[4, 25]。M策略基于等位基因的最大化,同时兼顾遗传多样性,是目前最具优势的一种方法。通过Core Finder软件以M策略构建核心种质已在杜仲、杉木、木荷等林木上成功应用[2, 4, 16]。因此,本研究选择基于M策略利用Core Finder软件构建江西杉木种质资源的核心种质,结果从495份江西杉木原种质中得到52份核心种质,同时通过t检验和PCoA分析,显示获得的核心种质具有更丰富的遗传多样性,且均匀分布于原种质资源中,表明构建的核心种质可靠有效,具有代表性。
核心种质构建的宗旨是以最小的资源数量和遗传重复包含原种质中最大的遗传多样性。因此,确定合理取样比例是关键[9]。目前研究表明林木种质资源的核心种质取样比例一般在10%~30%之间。方乐成等[26]分析了192份楸树(Catalpa bungei C.)种质的遗传多样性,获得了46份核心种质,抽样比例23.96%;刘松等[15]利用SSR标记建立了占原种质24.85%的中国板栗核心种质;杨汉波等[16]基于SSR标记从754份木荷种质资源中获得了115份核心种质,占原种质的15.3%;李洪果等[2]则从887份杜仲种质中得到189份核心种质和698份保留种质,核心种质占原种质的21.3%。在本研究中,根据SSR标记分析结果,基于M策略从495份原种质中抽取了52份核心种质,经过遗传多样性评价和显著性t检验,确定江西杉木核心种质合适的取样比例为10.5%。这个比例与已报道的同样基于SSR标记获得的广西杉木核心种质占比9.3%接近[4];低于Duan等[13]从南方6个省份700份杉木基础群体中构建300份核心种质的比例,也低于在SNP标记基础上获得杉木核心育种群体占比(64.7%)以及速生优质杉木核心种质占比(50%)[27-28]。本研究的杉木种质均来源江西省,李魁鹏等[4]杉木种质则主要来源广西境内,两者的遗传结构较Duan等[13]700份杉木材料来源南方6省市相对简单。这符合核心种质的取样比例应根据原种质资源的遗传结构和数量规模来决定[29]。江西杉木52份核心种质中安福陈山红心杉种质10份(6.1%)、赣南地区种质20份(8.9%)、江西其他地区的种质22份(20.8%),安福陈山红心杉种质资源较多,但抽取的核心种质反而较少,这可能与陈山红心杉种质资源遗传多样性水平偏低有关[19]。
本研究中,52份核心种质的等位基因数(Na)的保留比例为100%,而有效等位基因数(Ne)、Shannon’s信息指数(I)、Nei’s遗传多样性指数(H)、观测杂合度(Ho)、期望杂合度(He)和多态信息含量(PIC) 6个参数的保留比例大于100%,这主要是由群体中的样本量和等位基因频率改变引起。这些遗传参数都是根据等位基因频率按不同的方法估算获得,用于度量不同群体在多样性上的遗传冗余情况,而核心种质的构建是一个减少频率高等位基因、增加稀有等位基因比例的过程,在去除遗传冗余的过程中,各等位基因频率的不规律增减会导致相应遗传多样性参数保留比例大于100%,这一现象在杜仲[2]、毛白杨[10]、木荷[16]和新疆野杏(Armeniaca vulgaris Lam.) [25]等的核心种质构建中均存在。
随着DNA分子指纹图谱的快速发展,SSR等分子标记的检测结果可进一步转化为字符串、条形码或二维码,即DNA分子身份证[30]。种质鉴定是种质资源收集、评价、保存和利用的基石,DNA分子身份证是种质鉴定的重要工具,目前已被广泛应用在作物、菌类、果树、花卉等种质鉴定[30-32],近年来,这一技术也逐步应用于林木种质资源的鉴定[33]。胡春龙等[34]构建了46份白蜡(Fraxinus sp.)种质资源的分子身份证,为白蜡新品种的审定、DUS测试等奠定了理论基础。张成才等[35]对36个薄壳山核桃(Carya illinoinensis (Wangenh.) K. Koch)国外引种品种建立分子身份证,为区分和鉴别薄壳山核桃品种提供参考。本研究在运用SSR标记分析江西杉木遗传多样性的基础上,构建了其核心种质的DNA指纹图谱,绘制了相应的分子身份证。不同于已报道的杉木分子身份证,本研究构建的分子身份证不仅包含了杉木种质的DNA指纹图谱信息,同时借鉴作物、果树等种质的分子身份证构建方法,设定了包含种质原产地、种质资源类别、收集保存时间的补充码,进一步增加所绘制的种质分子身份证的可靠性和特异性。
-
本研究利用前期筛选的20个杉木SSR标记,分析了495份江西杉木种质的遗传多样性,并利用M策略构建了含有52份材料的江西杉木核心种质,核心种质保留了原种质10.5%,等位基因数(Na)、有效等位基因数(Ne)、Shannon’s信息指数(I)、Nei’s遗传多样性指数(H)的保留比例依次为100.0%、107.4%、115.1%、109.0%,表明本研究建立的核心种质是有效的。同时根据标记的多态性信息含量(PIC)和鉴别能力,确定了H97、H286、CLSSR9和CLSSR37等4个标记能够实现52份核心种质的有效区分,并构建了52份核心种质的分子指纹图谱和分子身份证,为杉木种质资源的收集、保存和利用提供了理论基础。
基于SSR标记构建江西杉木核心种质及其分子身份证
Construction of Core Collection and DNA Fingerprinting of Chinese fir Germplasms from Jiangxi based on SSR Markers
-
摘要:
目的 分析江西杉木种质资源的遗传多样性,构建其核心种质;在此基础上,构建核心种质分子身份证,为江西杉木种质的进一步研究与利用提供理论依据和核心材料。 方法 以江西地区的杉木种质为材料,利用SSR标记开展遗传多样性分析,并基于等位基因数最大化原则(M策略)构建核心种质,通过遗传多样性参数及其保留比例进行核心种质评价,结合遗传多样性参数的t检验和主坐标分析(PCoA)验证和确认核心种质的代表性。基于最少标记鉴定最多种质的原则,选择高效SSR标记,构建江西杉木核心种质的SSR分子指纹图谱和分子身份证。 结果 20个SSR标记在495份种质中共检测到122个等位基因数(Na),平均Shannon’s信息指数(I)、平均Nei’s遗传多样性指数(H)、平均观测杂合度(Ho)和平均期望杂合度(He)分别为0.762、0.400、0.394和0.400,表明江西杉木种质的遗传多样性较丰富。采用M策略构建了含有52份材料的江西杉木核心种质,10.5%的核心种质保留了原种质100.0%的Na、107.4%的有效等位基因数(Ne)、115.1%的I、109.0%的H、104.1%的Ho、110.0%的He和111.2%的PIC; t检验表明以上遗传多样性参数与原种质均没有显著差异,主坐标分析(PCoA)显示核心种质在原种质的主坐标图分布均匀,说明构建的核心种质具有代表性。按多态性信息含量(PIC)值高低顺序,依次增加标记数量,结合UPGMA聚类,发现4个SSR分子标记,H97与H286、CLSSR9、CLSSR37相结合,可将52份江西杉木核心种质鉴别,据此构建了52份核心种质的SSR分子指纹图谱、分子身份证条形码和二维码。 结论 江西杉木种质资源的遗传多样性较丰富,构建的江西52份杉木核心种质具有代表性,选择上诉4个高效SSR标记可有效鉴别核心种质,并成功绘制了江西杉木核心种质的分子身份证。 Abstract:Objective To analyze the genetic diversity of the Cunninghamia lanceolata germplasms from Jiangxi Province, and a core collection of C. lanceolata was constructed. The molecular ID of the germplasms was studied for providing theoretical basis and core materials for further research and utilization of the germplasms. Method The genetic diversity of the germplasms was analyzed by SSR markers. A core collection was constructed through the allele number maximization strategy (M strategy). The core collection of the germplasms was assessed by the genetic diversity parameters and their retention ratio. The the core collection was confirmed with t-test and PCoA analysis. Based on the principle of distinguishing the most varieties using the fewest marker, the more effective SSR markers were selected to construct the molecular fingerprints and IDs of core germplasms. Result A total of 122 alleles were detected in the 495 germplasms by 20 SSR markers. The means of Shannon's information index (I), Nei's genetic diversity index (H), observed heterozygosity (Ho), and expected heterozygosity (He) were 0.762, 0.400, 0.394, and 0.400, respectively, which indicated a relatively high genetic diversity of the germplasms. The core collection of the 52 germplasms was constructed by M strategy in Core finder software. 10.5% of the core collection retained 100.0% Na, 107.4% Ne, 115.1% I, 109.0% H, 104.1% Ho, 110.0% He and 111.2% PIC of the original collection. The t-test analysis suggested that there were no significant differences between the core collection and original collection. This result was further confirmed by the PCoA analysis. Combining with the 4 SSR markers, H97 and H286, CLSSR9 and CLSSR37, the 52 core collections could be identified. And the molecular fingerprints and IDs of core collections were constructed. The molecular IDs were illustrated as barcodes and QR codes. Conclusion There is relatively abundant genetic diversity of C. lanceolata germplasms in Jiangxi. The 52 core collections are representative. The 4 more effective SSR markers mentioned above can identify the 52 core collections of Chinese fir from Jiangxi and can be successfully used for establishing molecular ID codes. -
Key words:
- Chinese fir
- / genetic diversity
- / core collection
- / molecular identity
- / SSR marker
-
表 1 江西杉木495份种质遗传多样性参数
Table 1. The genetic diversity parameters of C. lanceolata germplasms from Jiangxi
引物
Primer等位基因数
Na有效等位基因数
NeShannon’s信息指数
INei’s遗传多样性指数
H观测杂合度
Ho期望杂合度
He多态性信息含量
PICCLSSR1 3 1.168 0.289 0.144 0.127 0.144 0.135 CLSSR9 15 2.332 1.426 0.571 0.582 0.572 0.554 CLSSR10 6 1.329 0.572 0.248 0.240 0.248 0.237 CLSSR13 7 1.261 0.420 0.207 0.204 0.207 0.191 CLSSR19 6 1.603 0.761 0.376 0.370 0.377 0.349 CLSSR20 5 1.800 0.797 0.445 0.400 0.445 0.396 CLSSR21 5 1.667 0.608 0.400 0.424 0.401 0.323 CLSSR33 2 1.232 0.336 0.188 0.210 0.188 0.170 CLSSR37 5 2.315 0.927 0.568 0.550 0.569 0.474 CLSSR38 6 1.804 0.734 0.446 0.493 0.446 0.365 CLSSR40 3 1.014 0.045 0.014 0.014 0.014 0.014 CLSSR50 3 1.063 0.143 0.059 0.057 0.059 0.057 H7 7 2.136 0.939 0.532 0.527 0.532 0.469 H8 5 2.181 0.880 0.542 0.495 0.542 0.437 H16 6 1.864 0.846 0.464 0.483 0.464 0.410 H33 5 1.800 0.863 0.444 0.440 0.445 0.404 H76 8 2.096 0.984 0.523 0.509 0.524 0.460 H97 10 3.405 1.428 0.706 0.651 0.707 0.657 H201 6 1.975 0.954 0.494 0.501 0.494 0.448 H286 9 2.672 1.279 0.626 0.608 0.626 0.585 均值 Mean 6.1 1.836 0.762 0.400 0.394 0.400 0.357 表 2 江西杉木核心种质与原种质的遗传多样性比较
Table 2. The genetic diversity comparison between core collection and original collection of C. lanceolata germplasms from Jiangxi
种质
Germplasm数量
Number等位基因数
Na有效等位基因数
NeShannon’s信息指数
INei’s遗传多样性指数
H观测杂合度
Ho期望杂合度
He多态信息含量
PIC原种质 495 6.1 1.836 0.762 0.400 0.394 0.400 0.357 核心种质 52 6.1 1.972 0.877 0.436 0.410 0.440 0.397 (百分比) (10.5%) (100.0%) (107.4%) (115.1%) (109.0%) (104.1%) (110.0%) (111.2%) t 0.6696 0.9192 0.5987 0.2592 0.5150 0.7283 p 0.5072 0.3638 0.5529 0.7969 0.6573 0.4709 -
[1] 安元强, 郑勇奇, 曾鹏宇, 等. 我国林木种质资源调查现状与策略研究[J]. 世界林业研究, 2016, 29(2):76-81. [2] 李洪果, 许基煌, 杜红岩, 等. 基于等位基因最大化法初步构建杜仲核心种质[J]. 林业科学, 2018, 54(2):42-51. [3] 吴 涛, 陈少瑜, 肖良俊, 等. 基于SSR标记的云南省核桃种质资源遗传多样性及核心种质构建[J]. 植物遗传资源学报, 2020, 21(3):767-774. [4] 李魁鹏, 陈仕昌, 程 琳, 等. 基于SSR标记构建广西杉木核心种质[J]. 广西科学, 2021, 28(5):511-519. [5] FRANKEL O H. Genetic perspectives of germplasm conservation[A] ARBER W, LLIMENSEE K, PEACOCK W J, et al. Genetic manipulation: impact on man and society[C]. Cambridge, UK: Cambridge University Press, 1984: 161-170. [6] BROWN A H D. Core collections: A practical approach to genetic resource management[J]. Genome, 1989, 31(2): 818-824. doi: 10.1139/g89-144 [7] 钟永达, 刘立盘, 李彦强, 等. 中国樟树初级核心种质取样方法与策略研究[J]. 西南林业大学学报(自然科学), 2020, 40(4):1-13. [8] 于晓池, 李 凤, 欧 阳, 等. 基于表型的灰楸核心种质构建[J]. 林业科学研究, 2021, 34(6):38-45. [9] 张 捷, 张 萍, 李勤霞. 新疆野核桃核心种质的构建[J]. 果树学报, 2018, 35(2):168-176. [10] 毛秀红, 朱士利, 李善文, 等. 基于荧光SSR标记的毛白杨核心种质构建[J]. 北京林业大学学报, 2020, 42(7):40-47. [11] 杨 兰, 李慧娥, 郭其强. 青藏高原特有种砂生槐的核心种质构建[J]. 植物生理学报, 2022, 58(6):1133-1144. [12] 张馨方, 张树航, 李 颖, 等. 基于SSR标记构建燕山板栗核心种质[J]. 华北农学报, 2021, 36(S1):31-38. doi: 10.7668/hbnxb.20192435 [13] DUAN H, CAO S, ZHENG H, et al. Genetic characterization of Chinese fir from six provinces in southern China and construction of a core collection[J]. Scientific Reports, 2017, 7(1): 13814. doi: 10.1038/s41598-017-13219-0 [14] 陈 存, 丁昌俊, 张 静, 等. 美洲黑杨群体结构分析及核心种质库构建[J]. 林业科学, 2020, 56(9):67-76. doi: 10.11707/j.1001-7488.20200908 [15] 刘 松, 聂兴华, 李伊然, 等. 基于SSR荧光标记构建板栗品种(系)核心种质群[J]. 果树学报, 2023, 40(2):230-241. [16] 杨汉波, 张 蕊, 王帮顺, 等. 基于SSR标记的木荷核心种质构建[J]. 林业科学, 2017, 53(6):37-46. [17] LI N, YANG Y, XU F, et al. Genetic diversity and population structure analysis of Castanopsis hystrix and construction of a core collection using phenotypic traits and molecular markers[J]. Genes, 2022, 13(12): 2383. doi: 10.3390/genes13122383 [18] GUO Q, LIU J, LI J, et al. Genetic diversity and core collection extraction of Robinia pseudoacacia L. germplasm resources based on phenotype, physiology, and genotyping markers[J]. Industrial Crops and Products, 2022, 178: 114627. doi: 10.1016/j.indcrop.2022.114627 [19] 娄永峰, 宋晓琛, 冷春晖, 等. 陈山红心杉母树林与种子园遗传多样性分析[J]. 南方林业科学, 2023, 51(1):12-13 + 46. [20] 王华缄, 黄 铨, 邓宗富, 等. 杉木基因资源收集、保存和利用的研究[J]. 林业科学, 1999, 35(5):38-45. [21] CIPRIANI G, SPADOTTO A, JURMAN I, et al. The SSR-based molecular profile of 1005 grapevine (Vitis vinifera L. ) accessions uncovers new synonymy and parentages, and reveals a large admixture amongst varieties of different geographic origin[J]. Theoretical and Applied Genetics, 2010, 121(8): 1569-1585. doi: 10.1007/s00122-010-1411-9 [22] 江西省林木种苗和林场管理局. 江西林木种质资源[M]. 北京: 中国林业出版社, 2011. [23] 欧阳磊, 陈金慧, 郑仁华, 等. 杉木育种群体SSR分子标记遗传多样性分析[J]. 南京林业大学学报(自然科学版), 2014, 38(1):21-26. [24] 李 霞, 王利宝, 文亚峰, 等. 杉木不同世代育种群体的遗传多样性[J]. 林业科学, 2020, 56(11):53-61. doi: 10.11707/j.1001-7488.20201106 [25] 刘 娟, 廖 康, 赵世荣, 等. 利用ISSR分子标记构建新疆野杏核心种质资源[J]. 中国农业科学, 2015, 48(10):2017-2028. [26] 方乐成, 夏慧敏, 麻文俊, 等. 基于SSR标记的楸树遗传多样性及核心种质构建[J]. 东北林业大学学报, 2017, 45(8):1-5. [27] ZHENG H, HU D, WEI R, et al. Chinese fir breeding in the high-throughput sequencing era: insights from SNPs[J]. Forests, 2019, 10(8): 681. doi: 10.3390/f10080681 [28] 黄 荣, 胡德活, 邓厚银, 等. 利用SNP标记解析速生优质杉木群体的遗传多样性与结构[J/OL]. 分子植物育种: 1-10[2023-04-14]. http://kns.cnki.net/kcms/detail/46.1068.S.20211130.1703.012.html. [29] 李自超, 张洪亮, 曹永生, 等. 中国地方稻种资源初级核心种质取样策略研究[J]. 作物学报, 2003, 29(1): 20-24. [30] TIAN H L, WANG F G, ZHAO J R, et al. Development ofmaizeSNP3072, a high-throughput compatible SNP array, forDNA fingerprinting identification of Chinese maize varieties[J].Molecular Breeding, 2015, 35(6): 136. [31] 高利慧, 鲍大鹏, 徐 珍, 等. 基于遗传多样性构建金针菇的核心种质群体及分子身份证[J]. 菌物学报, 2021, 40(12):3214-3230. [32] 张 枭, 杜 潇, 孙馨宇, 等. 利用SSR标记构建部分山楂资源的基因身份证[J]. 沈阳农业大学学报, 2021, 52(2):153-159. [33] 林 萍, 王开良, 姚小华, 等. 基于转录组SNP构建油茶主要品种资源的分子身份证[J]. 中国农业科学, 2023, 56(2):217-235. doi: 10.3864/j.issn.0578-1752.2023.02.002 [34] 胡春龙, 张 晨, 刘翠兰, 等. 基于SSR标记构建白蜡种质资源分子身份证[J]. 山东农业科学, 2015, 47(5):6-9 + 22. [35] 张成才, 王亚萍, 王开良, 等. 利用SSR构建薄壳山核桃主要品种的分子身份证[J]. 植物遗传资源学报, 2022, 23(6):1835-1846. -




 下载:
下载: