-
病原菌种内专化型的分化机制是植物病理学研究的基本问题,揭示其中的机制对于认识病害发生规律和提出防治策略均具有重要意义[1]。杨生褐盘二孢(Marssonina brunnea (Ell. et Ev.) P. Magn.)是引起杨树早期落叶和树势衰弱的重要病原菌[2-3],针对不同杨树寄主,该菌分化为多芽管和单芽管两个专化型,并在自然界分别只侵染亲和性黑杨(Aigeiros)(包括青杨Tacamahaca)派系寄主和白杨派系(Leuce)寄主[2, 4]。有研究表明,籍于ITS分子系统发育以及其它遗传分子标记,在一定程度上可区分两个专化型[5-6],尤其ITS2遗传特征能区分聚类不清的专化型[6],这说明两个专化型的分化具有一定的分子遗传基础。但这种分化基础在病原与寄主互作水平上的表现并未给予揭示,专化型是病原侵入寄主过程中与寄主互作的表型体现,是病原与寄主互作生态进化的结果,其中寄主的病程相关蛋白可能参与或奠定了专化性的发生基础[1]。为此,作者在明确黑杨寄主对两个专化型侵染具有响应的基础上,通过分析已有相关病原专化型侵染与杨树互作过程的研究报道,选取了具有抗病标记作用的杨树寄主基因,如水杨酸(SA)诱导表达防卫基因PR5(类奇异果糖蛋白)、抗性基因PR10、SAR(systemic acquired resistance)信号途径中起关键调控因子的非病程相关基因表达基因NPR1(Nonexpressor of Pathogenesis-related Genes1)、抗病调控转录因子WRKY以及和对褐斑病病菌菌丝有抑制作用的无色花色素还原酶基因(PtrLAR)等进行分析研究,结果初步证明了杨生褐盘二孢和寄主的互作是形成杨树专化型的基础之一。
-
杨生褐盘二孢多芽管专化型菌株RHHB分离自河北任丘黑杨(Populus deltoids),单芽管专化型菌株RHBH分离自北京昌平白杨(P. tomentosa)。菌株保藏于中国林业科学研究院森林生态环境与保护研究所病理室。
供试黑杨为一年生扦插苗盆栽苗。扦插于第二年3月份,7—8月份成熟叶片用于接种试验。
-
孢子悬浮液制备:两专化型菌株RHHB和RHBH分别在PDA培养基上培养30 d,无菌水洗脱孢子,分别制备成浓度为106个·mL-1的孢子悬浮液用于接种。
侵染试验及病情分级:7—8月份,选取健康长势相近的一年生的黑杨扦插植株进行处理试验。每株选取7~8片健康成熟叶片用于涂抹接种,塑料袋保湿48 h。对照设置为接种无菌水。选取接种后2、8、24、96 h观察记录侵染过程和发病情况,该时间点对应孢子萌发的不同发育阶段和侵染阶段。发病程度依据病情指数统计,病情指数分级标准见表 1。
表 1 离体叶片接种病情分级标准
Table 1. Disease classification standard of poplar leaves inoculate in vitro
病级
Disease stage病斑数·cm-2叶面
Spots no./cm2 in leaf抗病程度
Disease condition level0 0 免疫 1 0.1-10 高抗 2 10.1-24.0 中抗 3 >24,病斑离散 中感 4 >24,病斑联合 高感 侵染过程观察:黑杨接种叶组织经徒手切片[7]后,放在载玻片上,滴加0.001%的荧光增白剂(18909-100ML-F, Sigma),黑暗条件下染色5 min后,在倒置荧光显微镜(徕卡DMI6000B)观察褐盘二孢孢子在黑杨叶片的发育侵染过程。
-
取接种后第2、24、96 h处理组黑杨和对照叶组织,用锡箔纸包裹立即放到液氮中1 min,然后取出放入-80℃冰箱中保藏至RNA提取。
RNA提取及反转录:实验采用CTAB法提取RNA[8]。用1%琼脂糖凝胶及Nanodrop ND-1000仪对RNA完整性和质量进行检测。反转录前,用RQ1 RNase-Free Dnase (Promega)去除RNA样本中的DNA,并将RNA的浓度稀释为100 ng·μl-1,取10 μlRNA作为反转录起始模板,反转录试剂盒采用Revert Aid First Strand cDNA Synthesis Kit (Thermo),按说明书进行。
-
以病程相关蛋白PR5、PR1、NPR1,WRKY基因家族的基因PtrWRKY89以及无色花色素还原酶基因PtrLAR3为定量表达基因,内参基因为ACTIN。内参基因与目的基因扩增效率M值< 0.1。上述基因扩增引物(表 2)见相关文献[9-12],且其专化性经过实验验证。
表 2 Real-time PCR中目的基因的引物
Table 2. The Primers of target genes in Real-time PCR
基因Gene 蛋白ID Protein ID 5’-引物5’-primer 3’-引物3’-primer 产物大小(bp)Product size PR-5 669475 CGAAACCAATGCCCTTACAC CAATCACCTGTCTCGCACAT 139 PR-10 827390 GTTTGGATGGAGGGAGTTGA CAGTCCTTCGGTCTTCTTGC 122 NPR1 253241 GACGAGGAAGACAAACCAGTGCG CGACGATACTTCCCCAGTTGCTC 154 PtrWRKY89 7484630 TCCAACGATCCACAATAACC TAAAACATCACCGCCGTCTC 157 PtrLAR3 CGGTGATGGGACAGTTAAAG CATGGCAACAAAGCTCTCAA 140 Actin EF418792.1 TCATCGGAATGGAAGCTGCTGGTA TAGTGGAACCACCACTGAGCACAA 117 基因表达定量采用SYBR Green (Life Technologies)相对定量2-ΔΔCt法。其中ΔΔCt的计算方法如下:
ΔCt=Ct(目的基因)— Ct(参考基因)
△△Ct =△Ct(试验样品)—△Ct(基准样品)
△Ct(试验样品) = Ct(试验样品,目的基因)—Ct(试验样品,内参基因)
△Ct(基准样品) = Ct(基准样品,目的基因)—Ct(基准样品,内参基因)
定量PCR的反应体系为20 μL,每个处理3个重复。反应程序:95℃预变性10 min;95℃变性10 s,60℃退火60 s(开启荧光),40个循环。定量PCR仪为Rorot Gene 6000。
-
经接种试验调查,两专化型在供试黑杨上产生的发病率情况分别是:多芽管专化型菌株RHHB从29.2~50%;单芽管专化型菌株RHBH从08.3%,分别表现为感病和抗病(表 3)。这与自然界专化型侵染相应寄主发病的现象是一致的。
表 3 杨生褐盘二孢接种黑杨叶片感病病情分析结果
Table 3. Results of disease condition of P. nigra leaves inoculate M. brunnea
菌株
Strain黑杨 批次
Batch数量
No.病情指数
Disease index病情
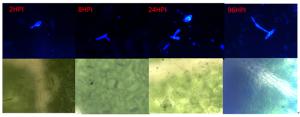
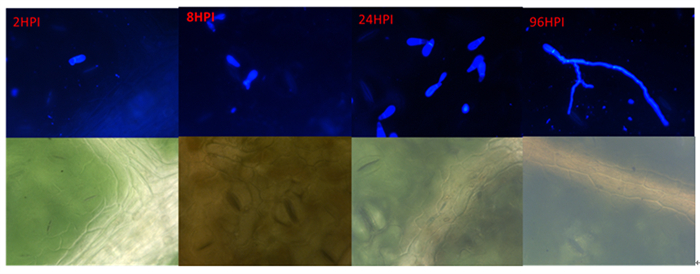
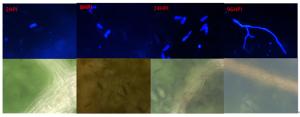
Disease conditionRHHB 2~5 6 29.2~50 中感 RHBH 2~2 6 0~8.3 高抗 注:叶片的感病程度以病情指数作为衡量标准,抗病程度与感病指数之间的对应关系是:免疫,0;高抗0.1~10;中抗10.1~24.0;中感24.1~50.0;高感50.1~100。 杨生褐盘二孢黑杨专化型RHHB和白杨专化型RHBH在黑杨叶片上的发育过程(图 1、2)基本一致,即在接种2 h时,分生孢子开始萌发,在2~12 h逐渐长出芽管;12 h时始见附着孢;在24 h时产生大量附着孢;48~96 h时产生先菌丝。
RHHB在黑杨叶片表面开始大量形成先菌丝,先菌丝先端接触到叶片后膨大形成附着孢,由此开始侵染叶片。菌丝在扩展过程中逐渐形成分生孢子盘,接种叶片在10 d可以看到产生病斑,病斑颜色由褐色逐渐加深至黑色;而RHBH产生少量先菌丝后就不再对叶片侵染,接种10 d后也未发现叶片表面有病斑出现。
-
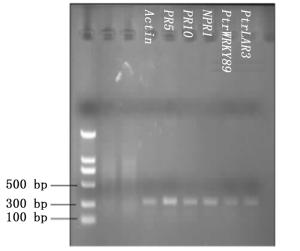
选择内参基因Actin和五个目的基因的标准曲线的相关系数R2>0.97,扩增效率E值为1.05和1.06,两者的M值相差小于0.1 (表 4)。扩增后的产物可通过溶解曲线的峰型图直观判断,内参Actin和五个目的基因的Real-time PCR产物经过电泳均为单一条带(图 3),表明扩增产物特异性较高。这些结果均符合实时荧光定量PCR标准曲线相关标准,满足后续试验要求,可以进行荧光定量PCR试验[13-14]。
表 4 相对定量的相关参数
Table 4. Relative quantitative parameters
基因Gene R2值R2-value M值M-value E值E-value Actin 0.993 76 -3.208 1.05 PR5 0.986 63 -3.218 1.05 PR10 0.974 96 -3.178 1.06 NPR1 0.995 81 -3.177 1.06 PtrWRKY89 0.981 58 -3.208 1.05 PtrLAR3 0.991 92 -3.212 1.05 黑杨5个抗性基因在叶片分别接种孢子2 h、24 h、96 h后的表达情况如下(图 4)。
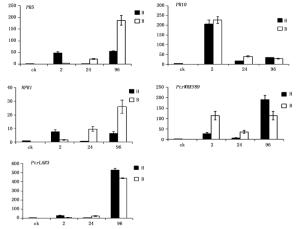
图 4 目的基因在不同时期Real-time PCR相对定量表达
Figure 4. The samples relative expression of target genes in different stages by real-time PCR
在黑杨应答杨盘二孢侵染的过程中,随着孢子在叶片上的萌发生长和侵染,抗病基因对不同专化型的表达也呈现不同的变化。多芽管专化型(黑杨专化型)病菌侵入时,黑杨在接种2 h时孢子萌发时,均上调表达了5个抗性基因,其中PR10上调最为显著;至接种后24 h时病菌附着孢形成,寄主中这5个基因均呈现显著下调表达,显示出寄主对这一时期病菌侵染过程抗性的减弱;而接种96 h时,病菌先菌丝形成并侵入后,仅有PtrWRKY89和PtrLAR3显著上调表达,其余3个基因的表达与孢子萌发期的表达水平几乎持平。
而黑杨对单芽管专化型(白杨专化型)病菌相同发育阶段和侵染过程的应答,则是接种2 h时,PR10和PtrWRKY89显著上调表达,而其余3个基因的表达微式上调;接种24 h时病菌形成附着孢,PR5、NPR1和PtrLAR3持续明显上调,至接种96 h时,这3个参与病菌先菌丝形成和侵入阶段的抗性基因表达达到检测时间内的最高表达量;而PR10在接种24 h和96 h时持续下调,PtrWRKY89则在接种24 h时有所下调后,接种96 h时又有上调至病原菌侵染之处2 h的表达水平。因此,黑杨中5个抗性基因对两专化型的表达谱没有一个是相似的。可见,两专化型在侵染时,与寄主的互作在分子水平上存在显著差异。
-
侵染杨树的杨生褐盘二孢两个专化型具有一定的遗传基础[4-6]。11条随机扩增DNA多态性引物(RAPDs引物)能扩增到76条带,能将国内42株杨盘二孢聚类成主要的两组,并与寄主来源对应;仅有一株不在两组内,而被认为是过渡型[5],而这过渡型在ITS2结构的分型中得以归化为两组之一[6]。因此,杨盘二孢专化型是病原菌适应和遗传进化的结果。但我们不了解这遗传形成的进化压力,最新研究认为病原与寄主分子互作是压力构成的主要因素或主导因素[15]。自然界杨树褐斑病只发生在专化型褐盘二孢与其亲和的杨树组寄主中,不发生交叉侵染。供试的白杨专化型褐盘二孢(单芽管专化型)孢子能在供试黑杨上发育,但不能侵染。虽然在供试黑杨上也出现有8.3%的坏死病斑,但这些均属于过敏性坏死(张琰锋, 资料待发表)。因此,杨树寄主对褐盘二孢的选择性或二者之间的互作是形成专化型的分化的可能因素。
在杨树抗病抗逆的研究中,发现了一些抗性关联的常规表达基因[9-11, 16-17]。本文利用的5个基因中,PR5(类奇异果糖蛋白)是病程相关基因,由水杨酸(SA)诱导表达的防卫基因;PR10蛋白是具有多种小亚类的胞内蛋白,表现抗菌、体外酶活性、参与植物次生代谢、抵御非生物胁迫等复杂的生物学功能;NPR1是系统获得性抗性(systemic acquired resistance,SAS)信号途径关键调控因子之一,诱导PR相关基因表达;PtrWRKY89为WRKY基因家族,参与发育和生理过程调节,高通量转录组分析发现该族蛋白在杨树黑斑病、水杨酸途径、创伤等过程都表现抗性调控,并且加速PR相关基因表达;最后,PtrLAR3为无色花色素还原酶基因(PtrLAR),分离自毛果杨叶片,能抑制黑斑病菌菌丝的生长。这些基因在植物与病原物互作过程中发挥着一定作用,在病原菌侵染的不同时期,其表达也存在差异性。
从这5个抗病相关基因在侵染过程中的表达变化可见(图 4),黑杨寄主对病原菌的调控表达,在病原菌接触起始就有了响应。现已知病原菌孢子在叶组织表面萌发至附着孢形成,寄主的主要应答方式是对病原菌相关分子程式(pathogen-associated molecular patterns,PAMPs)因子识别引起的抗性,这种抗性非常容易被长期进化和适应了的病原菌所克服[13]。自然界杨生褐盘二孢的两个专化型上,与黑杨有着长期互作适应进化的是多芽管专化型。在我们的研究结果中,也呈现出二者的这种适应关系。如在2 h~24 h间,黑杨对多芽管专化型(RHHB)的接触和识别,在5个抗性基因中,寄主除PR10在孢子萌发阶段有强烈上调相应和迅速下调外,其余4个抗性基因并没有显示积极的显著上调表达,说明病原菌进化出适应寄主抗性的能力,并进而分泌效应物克服黑杨对PAMPs的抗性,致使黑杨发生病害[18]。而面对单芽管专化型的病菌侵染,在2 h病原菌萌发开始,黑杨寄主这5个基因就具有强烈应答表现,而且其中三个基因的表达强度随单芽管病原菌发育侵染过程不断增加,显示出该专化型与黑杨寄主的不亲和性。这可能是单芽管专化型在与黑杨寄主长期进化过程中,未发展出适应性互作关系的结果,致使黑杨寄主对此专化型表现出高度抗性或免疫。这种抗性从组织病理学的角度也可以发现(图 1),相对于多芽管专化型孢子发育形成附着孢之后,表现的继续旺盛生长而言,单芽管专化型孢子则在黑杨上萌发形成附着孢后,菌丝的发育即陷入停滞(图 2)。这些观察到的性状比较,在之前的研究中并未给予揭示或提示。当然,更为明确的区别特征有待于进一步通过更细致的分子组织病理学的方法给予阐述。
-
杨生褐盘二孢专化型的分化除了长期进化适应导致的遗传变异外,还可能与寄主互作过程相关。本文通过两个专化型菌株对黑杨侵染过程的组织病理学、及其关联的抗性基因表达变化的研究,发现了黑杨对两个专化型有着不同的应答图谱,进而认为病原菌专化型的分化与寄主的互作是密切相关的,杨生褐盘二孢与杨树寄主的互作对其专化型分化具有选择压力的作用。其机制有待于后续互作转录组学来做进一步的阐明。
黑杨应答杨生褐盘二孢专化型侵染的基因差异表达
Gene Differential Expression on Populus deltoids Responding to Infection by Marssonina brunnea Formae
-
摘要:
目的 杨生褐盘二孢的单芽管专化型和多芽管专化型分别引起白杨组和黑杨组(包括青杨组)杨树的褐斑病,其分化机制有待阐明。 方法 本文在专化性互作体系建立的基础上,利用荧光染色标记研究了病菌孢子在专化性寄主侵染过程中的萌发发育情况,并通过RT-qPCR分析了黑杨寄主抗病相关基因在应答两专化型侵染过程中的不同表达。 结果 结果发现多芽管分生孢子在黑杨寄主上能完成发育并成功侵染,单芽管分生孢子也能成功萌发和发育,但不能侵入黑杨寄主;黑杨抗性基因在两专化型侵染发育过程中均能被诱导表达,但在表达时间和表达量上,除基因WRKY89的表达较为一致外,病程相关基因PR5、PR10、NPR1和LAR3在二者间的表达存在差异。 结论 研究结果初步表明病原专化型可能是寄主与病原专性互作的表型,这一认识将有助于进一步探明杨树褐斑病病原专化型形成和分化的机制。 Abstract:Objective To study the mechanism of Marssonina brunnea sp. monogermtubi formae speciales (RHBH) infecting Populus Section Leuce and M. brunnea sp. multigermtubi formae speciales (RHHB) infecting Populus Section Aigeiros. Method Based on pathogen-host interaction system, the pathogen's spore germination, growth and infection process on poplar leaves were investigated by using fluorescence microscopy strain method and the expression of five pathogen-relative genes in hosts was also analyzed by RT-qPCR technique. Result The results showed that the spores of RHHB were able to grow and successfully infect the hosts of Populus Section Aigeiros, the spores of RHBH were also able to grow but failed to infect the hosts of Populus Section Aigeiros. The pathogen-resistant genes of Populus Section Aigeiros could be induced and express during the infection process of the two formae speciales. The gene express of WRIKY89 followed a similar expression trend, while the other four genes (PR5, PR10, NPR1 and LAR3) followed different expression patterns in time and quantity for the two formae speciales. Conclusion The study provides some references for study the mechanisms of the two formae speciales and their differentiation. -
Key words:
- Marssonina brunnea
- / formae speciales
- / Real-time PCR
- / gene express
-
表 1 离体叶片接种病情分级标准
Table 1. Disease classification standard of poplar leaves inoculate in vitro
病级
Disease stage病斑数·cm-2叶面
Spots no./cm2 in leaf抗病程度
Disease condition level0 0 免疫 1 0.1-10 高抗 2 10.1-24.0 中抗 3 >24,病斑离散 中感 4 >24,病斑联合 高感 表 2 Real-time PCR中目的基因的引物
Table 2. The Primers of target genes in Real-time PCR
基因Gene 蛋白ID Protein ID 5’-引物5’-primer 3’-引物3’-primer 产物大小(bp)Product size PR-5 669475 CGAAACCAATGCCCTTACAC CAATCACCTGTCTCGCACAT 139 PR-10 827390 GTTTGGATGGAGGGAGTTGA CAGTCCTTCGGTCTTCTTGC 122 NPR1 253241 GACGAGGAAGACAAACCAGTGCG CGACGATACTTCCCCAGTTGCTC 154 PtrWRKY89 7484630 TCCAACGATCCACAATAACC TAAAACATCACCGCCGTCTC 157 PtrLAR3 CGGTGATGGGACAGTTAAAG CATGGCAACAAAGCTCTCAA 140 Actin EF418792.1 TCATCGGAATGGAAGCTGCTGGTA TAGTGGAACCACCACTGAGCACAA 117 表 3 杨生褐盘二孢接种黑杨叶片感病病情分析结果
Table 3. Results of disease condition of P. nigra leaves inoculate M. brunnea
菌株
Strain黑杨 批次
Batch数量
No.病情指数
Disease index病情
Disease conditionRHHB 2~5 6 29.2~50 中感 RHBH 2~2 6 0~8.3 高抗 注:叶片的感病程度以病情指数作为衡量标准,抗病程度与感病指数之间的对应关系是:免疫,0;高抗0.1~10;中抗10.1~24.0;中感24.1~50.0;高感50.1~100。 表 4 相对定量的相关参数
Table 4. Relative quantitative parameters
基因Gene R2值R2-value M值M-value E值E-value Actin 0.993 76 -3.208 1.05 PR5 0.986 63 -3.218 1.05 PR10 0.974 96 -3.178 1.06 NPR1 0.995 81 -3.177 1.06 PtrWRKY89 0.981 58 -3.208 1.05 PtrLAR3 0.991 92 -3.212 1.05 -
[1] Vienne D M D, Refrégier G, López-Villavicencio M, et al. Cospeciation vs host-shift speciation: methods for testing, evidence from natural associations and relation to coevolution[J]. New Phytologist, 2013, 198(2): 347-85. doi: 10.1111/nph.12150 [2] 贺伟, 杨旺. 三种杨黑斑病菌的寄主范围及在我国部分地区的分布[J]. 林业科学, 1991, 27(5): 560-564. doi: 10.3321/j.issn:1001-7488.1991.05.001 [3] 赵增仁. 北京市杨树黑斑病病原菌的初步研究[J]. 中国森林病虫, 1990(1): 28-30. [4] 韩正敏, 李传道, 黄敏仁. 我国杨生褐盘二孢菌菌株比较[J]. 林业科学, 1998, 34(3): 59-65. doi: 10.3321/j.issn:1001-7488.1998.03.009 [5] Han Z M, Yin T M, Li C D, et al. Host effect on genetic variation of Marssonina brunnea pathogenic to poplars[J]. Theoretical & Applied Genetics, 2000, 100(3-4): 614-620. [6] 孙晓明, 严东辉, 贺伟, 等. 基于杨生褐盘二孢菌2个专化型的ITS2二级结构特征分析[J]. 林业科学, 2015, 51(11): 60-68. [7] 方中达. 植病研究方法[M]. 中国农业出版社, 1998. [8] Gambino G, Perrone I, Gribaudo I. A rapid and effective method for RNA extraction from different tissues of grapevine and other woody plants[J]. Phytochemical Analysis, 2008, 19(6): 520-525. doi: 10.1002/pca.1078 [9] Rinaldi C, Kohler A, Frey P, et al. Transcript profiling of poplar leaves upon infection with compatible and incompatible strains of the foliar rust Melampsora larici-populina[J]. Plant Physiology, 2007, 144(1): 347-66. doi: 10.1104/pp.106.094987 [10] Yang D, Jiezi H U, Chen X. Genome-wide identification and characterization of the Populus WRKY transcription factor family and analysis of their expression in response to biotic and abiotic stresses[J]. Journal of Experimental Botany, 2014, 65(22): 6629-6644. doi: 10.1093/jxb/eru381 [11] Yuan L, Wang L, Han Z, et al. Molecular cloning and characterization of PtrLAR3, a gene encoding leucoanthocyanidin reductase from Populus trichocarpa, and its constitutive expression enhances fungal resistance in transgenic plants. [J]. Journal of Experimental Botany, 2012, 63(7): 2513-2524. doi: 10.1093/jxb/err425 [12] 苏晓娟, 樊保国, 袁丽钗, 等. 实时荧光定量PCR分析中毛果杨内参基因的筛选和验证[J]. 植物学报, 2013, 48(5): 507-518. [13] 郑亚明, 骆勇, 周益林, 等. 实时荧光定量PCR在植物病害流行学中的应用[J]. 植物保护, 2011, 37(4): 18-22. doi: 10.3969/j.issn.0529-1542.2011.04.004 [14] Atallah Z K, Bae J, Jansky S H, et al. Multiplex Real-Time Quantitative PCR to Detect and Quantify Verticillium dahliae Colonization in Potato Lines that Differ in Response to Verticillium Wilt[J]. Phytopathology, 2007, 97(7): 865-72. doi: 10.1094/PHYTO-97-7-0865 [15] Chisholm S T, Coaker G, Day B, et al. Host-Microbe Interactions: Shaping the Evolution of the Plant Immune Response[J]. Cell, 2006, 124(4): 803-14. doi: 10.1016/j.cell.2006.02.008 [16] Yan D H, Fenning T, Tang S, et al. Genome-wide transcriptional response of Populus euphratica, to long-term drought stress[J]. Plant Science, 2012, 195(3): 24-35. [17] Sheng Z, Cao Y Z, Cong J, et al. Sequencing the genome of Marssonina brunnea, reveals fungus-poplar co-evolution[J]. Bmc Genomics, 2012, 13(1): 1-10. doi: 10.1186/1471-2164-13-1 [18] 梁伟红, 韩正敏. 杨盘二孢菌激发子粗提物生物活性的研究[J]. 南京林业大学学报(自然科学版), 2006, 30(3): 71-74. doi: 10.3969/j.issn.1000-2006.2006.03.015 -




 下载:
下载: