-
思茅松毛虫Dendrolimus kikuchii (鳞翅目:枯叶蛾科)主要分布在我国贵州、江西、安徽和云南等省,是我国危害最严重的6种松毛虫之一,经常对马尾松、云南松和思茅松等寄主植物造成重大危害[1]。该害虫性信息素成分被鉴定为顺5, 反7-十二碳二烯乙酸酯(Z5, E7-12:OAc),顺5, 反7-十二碳二烯醇(Z5, E7-12:OH)和顺5-十二碳烯乙酸酯(Z5-12: OAc)[2-3]。溶剂浸提性信息素腺体发现这3种成分的比例是100∶18∶0.6,固相微萃取法顶空吸附性信息素腺体发现这3种成分的比例是100∶7∶1,而林间试验证明氯化丁基橡胶塞诱芯中这3种成分以100∶20∶25的比例添加诱蛾活性最高[3]。不同性信息素成分提取及应用方法证明雌蛾性信息素成分释放和雄蛾响应间存在较大的比例差异。初步的林间诱捕试验发现相同性信息素诱芯对不同地域思茅松毛虫成虫引诱活性也存在一定的差异,这无疑给该虫的准确预测预报和有效防治带来一定的困难。
蛾类昆虫性信息素通讯系统的变化对于种内雌雄交配行为和近缘种种间生殖隔离具有重要的生物学意义。这种变化主要体现在蛾类昆虫不同地理种群间释放信息素成分量的差异或者释放比例的不同。从昆虫种群间和种群内性信息素信号产生以及行为反应差异方面研究物种特异性交配信号的变异程度具有重要的生物学意义。本研究主要开展不同思茅松毛虫地理种群雄蛾触角对性信息素标准化合物的触角电位反应、不同种群雌蛾性信息素腺体所含性信息素成分比例变化以及对各地理种群进行性信息素活性评价试验,探讨思茅松毛虫性信息素成分在不同地理种群间的变异程度。研究结论有助于开发有针对性地思茅松毛虫种群监测方法和诱捕防控技术。
-
思茅松毛虫虫茧采自湖南省郴州市桂阳县(112.734 1° E,25.754 1° N;寄主是柔毛油杉Keteleeria pubescens Cheng et L.k.Fu)、云南省普洱市震东乡(100.494 6° E,23.252 5° N;寄主是思茅松Pinus kesiya var. langbianensis(A.Chen.)Gaussen)、江西省九江市永修县(115.8265° E,29.035 7° N;寄主是湿地松Pinus elliottii Engelm.)。虫茧置于养虫笼中在光周期15L: 9D,温度25±1℃和湿度60%~80%RH条件待成虫羽化,羽化后的雌雄蛾立即分开,雌蛾用于性信息素提取,雄蛾用于触角电位分析。
-
思茅松毛虫处女雌蛾进入暗期4~7 h,在其求偶召唤状态时用溶剂浸提性信息素腺体。具体方法是:轻轻挤压思茅松毛虫雌虫腹部,性信息素腺体伸出后立即用镊子摘除,置于滤纸上轻轻挤压腺体,去除脂肪体等杂质,然后将腺体转移到装有20~30 μL正己烷的玻璃毛细管中浸泡30 min。用10 μL注射器将腺体移除,玻璃毛细管密封后置于-20℃冰箱中保存备用。信息素提取和稀释所用的溶剂正己烷为色谱纯。
-
标准化合物配制:Z5, E7-12:OAc、Z5, E7-12:OH和Z5-12:OAc标准化合物分别配制成10 μg·μL-1的母液。进行EAG剂量反应测试时,母液由高到低10×稀释成一系列浓度,取稀释液1 μL滴加到巴斯德管中5 cm × 0.6 cm的滤纸条上。按照浓度1 ng·μL-1、10 ng·μL-1、100 ng·μL-1、1 μg·μL-1、10 μg·μL-1从低到高的顺序依次进行EAG测试。进行3种性信息素成分不同比例EAG测试时,以3种信息素成分绝对含量的比例进行样品配制(如,Z5, E7-12:OAc: Z5-12:OAc=500 ng: 125 ng或者Z5, E7-12:OAc: Z5, E7-12:OH=500 ng: 50 ng),测试时各比例样品随机测试,配制比例见图 2。
触角准备:将1~2日龄雄虫触角从基部切下,同时切去端部1~2 mm,触角两端用导电胶(Spectra 360 electrode gel, Parker Laboratories Inc. Orange, NJ, USA)连接在Syntech电极两端((PRG-2, Syntech, Kirchzarten, Germany)。将制备好的触角置于“L”型玻璃管喇叭口内1cm位置。
触角电位测试:每种样品测试30~50头雄虫。湿润纯净的空气流速是800 mL·min-1,持续吹扫制备好的触角。不同浓度或者不同比例样品每次刺激气体体积是2 mL,刺激时间是0.1 s,2次刺激时间间隔是40 s,以使触角恢复活性。采集的触角电位值经电极前置放大器放大10×后传输到AC/DC UN-6放大器和IDAC数模转换器,最后经EAG软件采集分析(Ockenfels Syntech GmbH,Kirchzarten, Germany)。
-
每个种群分析20头雌虫性信息素腺体提取物。性信息素单腺体提取物在HP6890气相色谱仪(Agilent Technologies,Palo Alto,CA,USA)上分析。色谱仪装有无分流进样器、毛细管色谱柱DB-1701(30 m × 0.25 mm外径× 0.25 μm液膜厚,J & W Scientific,Folsom,CA,USA) 和火焰离子化检测器。色谱升温程序:60℃保持1 min,以8℃·min-1 的升温速率升至220℃,保持10 min。氮气为载气。利用Chemstation软件进行数据采集分析。
-
诱芯制备:将不同比例化合物(其中Z5, E7-12:OAc固定为500 μg)的正己烷溶液滴加到灰色袖口式氯化丁基橡胶塞上,待溶剂挥发后,再加20 μL二氯甲烷(含BHT 1 μg·μL-1)溶液使性信息素成分渗到橡胶塞载体中,BHT保护性信息素成分避免氧化分解。制备好的诱芯密封在铝箔袋中低温保存。
诱捕器悬挂:船型粘胶诱捕器(42 cm × 28 cm,北京中捷四方生物科技股份有限公司)挂在离地面大约1.5~2.0 m高的树枝上,诱捕器在试验区域内按照约30 m间距进行随机区组悬挂,区组间距约60 m。每隔2~3天记录诱捕器的诱蛾数并清除诱集到的雄蛾。
林间生物测试3个试验点概况:湖南省郴州市桂阳县(112.734 1° E,25.754 1° N),树种主要为柔毛油杉及少量马尾松,思茅松毛虫林间危害较重,测试时间为6月中旬到7月中旬;云南省普洱市震东乡(100.494 6° E,23.252 5° N),树种主要是思茅松,思茅松毛虫林间危害相对较轻,测试时间为6月上旬到7月中旬;江西省九江市永修县(115.826 5° E,29.035 7° N),树种主要是湿地松,危害最为严重,测试时间段为6上旬到7月中旬,每个处理设置5个重复。
-
将每一处理的GC数据、EAG数据及诱捕雄蛾数据经log(x+1)数据转换后进行单因素方差分析(ANOVA),采用Turkey’s HSD对处理间平均数进行差异显著性检验(α=0.05,SPSS Statistics22)。
-
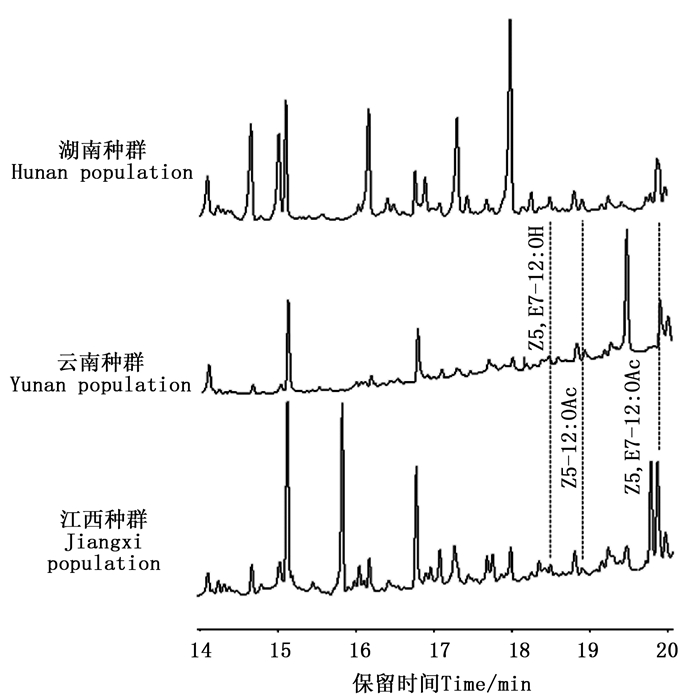
思茅松毛虫3个地理种群雌蛾单腺体提取物GC分析见图 1。3个地理种群雌虫腺体提取物中除含有相对大量的Z5, E7-12:OAc外,还发现微量的Z5, E7-12:OH和Z5-12:OAc(图 1,表 1)。Z5, E7-12:OAc在湖南、江西和云南种群中含量均最高且3个种群间无显著性差异(F(2, 57)=0.008,P=0.992)。Z5, E7-12:OH在湖南和江西种群间差异不显著,但是都显著高于云南种群(F(2, 57) =9.643,P<0.05)。Z5-12:OAc在湖南和江西种群间差异不显著,但都显著低于云南种群(F(2, 57)=7.787,P=0.001)。在3个地理种群雌蛾单腺体提取物中,3种性信息素成分分别以100:10:9(湖南)、100:9:8(江西)和100:6:11(云南)的比例存在(表 1)。

图 1 3个地理种群思茅松毛虫处女雌蛾单腺体提取物GC分析图
Figure 1. Gas chromatography traces from analysis of hexane extracts of the single sex pheromone gland of Dendrolimus kikuchii virgin females collected from 3 geographic populations
表 1 3个地理种群思茅松毛虫处女雌蛾单腺体提取物中性信息素成分GC定量分析结果
Table 1. GC results of spheromone components in single pheromone gland extract of virgin female Dendrolimus kikuchii quantified from 3 geographic populations
成分
Components单个腺体组分的绝对含量(ng,N= 20)
Amount of components in single gland extract (ng, N= 20)湖南种群Hunan population 江西种群Jiangxi population 云南种群Yunnan population Z5, E7-12:OAc 1.34±0.21 a* 1.44±0.22 a 1.34±0.22 a Z5, E7-12:OH 0.14 ±0.03 a 0.12±0.03 a 0.08±0.02 b Z5-12:OAc 0.12 ±0.02 b 0.12±0.03 b 0.15±0.03 a 比例Ratio 100:10:9 100:9:8 100:6:11 *表中差异显著性检验是在α=0.05条件下进行横向比较的结果。 -
利用EAG技术测定思茅松毛虫湖南种群、江西种群和云南种群对性信息素成分Z5, E7-12:OAc,Z5, E7-12:OH和Z5-12:OAc的敏感性差异(表 2)。各性信息素标准品在刺激剂量范围内(1 ng~10 μg) EAG反应值随着刺激剂量的增大而增大,在最大刺激剂量10 μg测试条件下各种群雄虫触角电位反应仍未达到饱和状态。湖南和江西种群对Z5, E7-12:OAc的EAG检测阈值是100 ng·μL-1,对Z5-12:OAc的检测阈值是1 000 ng·μL-1,都比云南种群敏感。云南思茅松毛虫种群对这2种酯类性信息素成分在1~1 000 ng刺激剂量范围内EAG反应值相互间差异不显著,敏感性较低。云南和江西种群对Z5, E7-12:OH的EAG检测阈值是100 ng·μL-1,比湖南种群敏感(1 000 ng·μL-1)。3个性信息素成分在10 μg刺激条件下,湖南种群对Z5, E7-12:OAc的EAG反应值最高(7.66 mV),江西种群次之(5.47 mV),云南种群最低(1.13 mV);江西种群对Z5, E7-12:OH的EAG反应值最高(8.91 mV),云南种群次之(4.95 mV),湖南种群最低(4.34 mV);江西种群对Z5-12:OAc的EAG反应值最高(5.03 mV),云南种群次之(3.98 mV),湖南种群最低(3.03 mV)。
表 2 思茅松毛虫3个地理种群雄虫触角对Z5, E7-12:OAc,Z5, E7-12:OH和Z5-12:OAc的EAG剂量-反应数值
Table 2. Mean EAG responses of three Dendrolimus kikuchii populations to a range of stimulus loads of Z5, E7-12:OAc, Z5, E7-12:OH and Z5-12:OAc
刺激量
Stimulus loads/ngZ5, E7-12:OAc Z5, E7-12:OH Z5-12:OAc 湖南种群
N=45江西种群
N=33云南种群
N=34湖南种群
N=45江西种群
N=33云南种群
N=35湖南种群
N=45江西种群
N=35云南种群
N=351 0.04±0.01 d* 0.15±0.04 c 0.09±0.03 b 0.02±0.01 c 0.26±0.07 c 0.14±0.03 c 0.02±0.01 c 0.02±0.01 c 0.22±0.05 b 10 0.04±0.01 d 0.54±0.14 c 0.09±0.04 b 0.02±0.01 c 0.16±0.04 c 0.36±0.09 c 0.06±0.02 c 0.04±0.01 c 0.13±0.04 b 100 0.39±0.06 c 1.18±0.28 b 0.17±0.05 b 0.05±0.01 c 0.64±0.19 b 1.25±0.24 b 0.27±0.06 c 0.12±0.03 c 0.43±0.10 b 1 000 1.92±0.29 b 2.19±0.41 b 0.29±0.08 b 0.22±0.06 b 2.69±0.47 b 1.44±0.38 b 1.68±0.35 b 0.72±0.12 b 0.64±0.10 b 10 000 7.66±0.81 a 5.47±0.81 a 1.13±0.42 a 4.34±0.68 a 8.91±1.29 a 4.95±0.86 a 3.03±0.41 a 5.03±0.62 a 3.98±0.51 a *每栏后不同小写字母表示雄蛾触角对单一性信息素成分不同浓度梯度的EAG反应有显著差异(α=0.05),N为测定重复数。
Z5, E7-12:OAc:湖南F(4, 220)=184.59,P<0.05;江西F(4, 160)=31.39,P<0.05;云南F(4, 165)=76.62,P<0.05;
Z5, E7-12:OH:湖南F(4, 220)=36.76,P<0.05;江西F(4, 160)=78.66,P<0.05;云南F(4, 170)=30.22,P<0.05;
Z5-12:OAc:湖南F(4, 220)=48.77,P<0.05;江西F(4, 170)=58.64,P<0.05;云南F(4, 170)=45.24,P<0.05。3种性信息素标准化合物不同混合比例的EAG测试结果见图 2。在Z5, E7-12:OAc和Z5-12:OAc比例和含量(500 ng: 125 ng)保持不变的情况下,云南种群Z5, E7-12:OH含量在0~250 ng 6个测试比例条件下,EAG反应值差异不显著;而湖南种群和江西种群在Z5, E7-12:OH含量为50 ng时EAG测试值最大,与其他比例相比差异显著;其他测试比例条件下江西种群差异不显著,湖南种群在200 ng和250 ng时EAG测试值最低,差异显著。在Z5, E7-12:OAc和Z5, E7-12:OH比例和含量(500 ng: 50 ng)保持不变的条件下,湖南种群、云南种群和江西种群在Z5-12:OAc含量为50 ng时EAG测试值最大,与其他测试比例差异显著。在Z5-12:OAc含量为0 ng、100 ng、150 ng、200 ng、250 ng时,云南种群和江西种群EAG测试值差异不显著,湖南种群仅在100 ng时测试值差异显著。
-
林间生物测定确定了Z5, E7-12:OAc、Z5, E7-12:OH和Z5-12:OAc 3组分的最佳诱蛾比例(图 3)。结果表明,在Z5, E7-12:OAc和Z5-12:OAc的含量和比例(500 μg: 125 μg)保持不变的情况下,Z5, E7-12:OH的含量是50 μg时(100:10:25)对3个思茅松毛虫地理种群的诱蛾活性最高。在Z5, E7-12:OAc和Z5, E7-12:OH比例和含量(500 μg: 50 μg)保持不变的情况下,Z5-12:OAc的含量在50 μg时(100:10:10),江西和云南种群的诱蛾活性均最高,但与100:10:25配比相比诱芯诱蛾效果差异不显著;湖南种群在100:10:10配比时的诱芯诱蛾效果也较高,但配比为100:10:25的诱芯诱蛾效果最好且显著高于其他配比诱芯的诱蛾效果。其他不同配比的诱蛾效果均不如这2种配比的诱蛾效果,这与EAG测定结果相吻合(图 3)。
-
思茅松毛虫在长江以南各省广域分布,林间点片发生,危害的寄主植物各地有差异。思茅松毛虫3个地理种群性信息素成分的释放比例有微小的差异,雄蛾对不同比例性信息素成分的响应也有差异,原因可能是思茅松毛虫从南向北蔓延危害过程中,面临不同寄主选择及各地区温湿度和地形等因素的分化干扰造成的。目前,性信息素地理变异研究较全面的是玉米螟。欧洲玉米螟(Ostrinia nubilalis)有2个完全不同的性信息素型种群,危害玉米的种群以顺11-十四碳烯乙酸酯(Z11-14:OAc)和反11-十四碳烯乙酸酯(E11-14:OAc)97:3的比例进行雌雄间化学通讯(Z型)[4],Z型种群在欧美广泛分布[5];而危害艾蒿的种群这2种成分的比例是4:96(E型)[6];同域发生的这2个种群在田间由于危害的寄主不同、其性信息素通讯系统比例差异巨大而完全生殖隔离。另外,欧洲玉米螟与亚洲玉米螟(O. furnacalis)性信息素生物合成过程中脱饱和化酶基因发生了改变,导致这2个近缘种性信息素化学信号成分发生了本质的变化[7-8]。思茅松毛虫雌虫释放的性信息素化学信号及雄虫对化学信号的反应没有发生像玉米螟一样较大的比例变化,说明其化学信号释放面临较弱的性选择压力,化学信号组分、比例的遗传漂变可能是随机的过程[5, 9]。思茅松毛虫性信息素通讯系统仅表现出性信息素成分含量和比例的微小差异,这与各地气候差异、寄主种类差异和人类进行农药喷施、砍伐树木等因素密切相关。今后我们还应该采用分子标记的方法深入研究思茅松毛虫地理种群间的种下变异程度。
-
思茅松毛虫性信息素腺体中含有Z5, E7-12:OAc(1.3-1.5 ng/female),Z5, E7-12:OH(0.08-0.15 ng/female)和Z5-12:OAc(0.12-0.15 ng/female)3个性信息素成分,确认了湖南种群(100∶10∶9)、云南种群(100∶6∶11)和江西种群(100∶9∶8)3种性信息素成分的含量和比例有微小的差异。经EAG测试分析表明,湖南种群最佳EAG反应的3种性信息素成分的比例是100∶10∶25,云南种群是100∶10∶10,江西种群是100∶10∶10或者100∶10∶25。林间生物测试表明,湖南种群3种性信息素成分以100∶10∶25的比例配比诱蛾效果最佳,云南种群和江西种群是100∶10∶25或者100∶10∶10。证明思茅松毛虫性信息素成分的含量与比例多态性存在于南方各地理种群。本研究分析了思茅松毛虫湖南、云南和江西地理种群间性信息素的变异程度,为进一步研究其传播及发生规律、开发有针对性对思茅松毛虫的种群监测方法和诱捕防控技术奠定基础。
思茅松毛虫3个地理种群性信息素成分差异分析
Geographic Variation of Sex Pheromones in Three Populations of Dendrolimus kikuchii (Lepidoptera: Lasiocampidae)
-
摘要:
目的 分析思茅松毛虫雌成虫不同地理种群间性信息素成分、含量和比例差异,比较雄成虫触角敏感性和不同配比诱芯诱捕效果差异,开发不同地域有针对性的思茅松毛虫种群监测方法和诱捕防控技术。 方法 运用气相色谱(GC)分析思茅松毛虫湖南、云南和江西地理种群雌虫性信息素腺体提取物,利用触角电位仪(EAG)测定思茅松毛虫各地理种群雄蛾触角对性信息素标准品及其不同配比组分的电生理敏感性,然后进行林间生物测定,比较不同配比的性信息素成分诱蛾效果。 结果 思茅松毛虫性信息素腺体中含有顺5,反7-十二碳二烯乙酸酯(Z5,E7-12:OAc)、顺5,反7-十二碳二烯醇(Z5,E7-12:OH)和顺5-十二碳烯乙酸酯(Z5-12:OAc)3种成分,3个地理种群间这3种腺体成分含量和比例存在微小差异。3种成分以100:10:25或者100:10:10的比例配比,不同地理种群间均具有很好的触角电位活性和林间诱蛾活性。 结论 思茅松毛虫性信息素组分还没有发生明显的种下分化现象,3个地理种群间性信息素含量和比例的细微差异暗示着与地域差异、寄主植物差异和人为化学防控干扰等因素相关。 Abstract:Objective In order to unveil the mechanism of population divergences to sex pheromone responses and develop a region-specific pheromone lure for successful monitoring and control of Dendrolimus kikuchii (Lepidoptera: Lasiocampidae), we focus on the geographic variation analysis of sex pheromones of D. kikuchii according to its sex pheromone quantity, blend ratio, antennal sensitivity, and biological activity in three populations from Hunan, Jiangxi, and Yunnan Provinces. Method Sex pheromone of D. kikuchii from different populations mentioned above was analyzed by means of Gas chromatography (GC), Electroantennographic recording (EAG), and field behavioral assays. Result GC analyses of virgin female glands demonstrated that three pheromone components, (5Z, 7E)-5, 7-dodecadien-1-yl acetate (Z5, E7-12:OAc), (5Z, 7E)-5, 7-dodecadien-1-ol (Z5, E7-12:OH) and (5Z)-5-dodecenyl acetate (Z5-12:OAc) were present in all three populations. On average, all populations had a similar and abundant quantity of Z5, E7-12:OAc as well as trace amounts of Z5, E7-12:OH and Z5-12:OAc, the blend ratio and quantities of the three components in three populations existed relatively small differences with a blend ratio of 100:10:25 or 100:10:10 showing better EAG and behavioral activities than that of the other blend ratios. Conclusion These results suggested that different geographic populations of D.kikuchii have developed some minor genetic variation but did not form completely independent groups. The subtle changes in sex pheromone quantities and blend ratios in different populations might be related to geographic distribution range, hosts, and man-made pesticide control interference. -
Key words:
- Dendrolimus kikuchii
- / sex pheromone
- / GC analysis
- / geographic populations
- / biological assay
-
表 1 3个地理种群思茅松毛虫处女雌蛾单腺体提取物中性信息素成分GC定量分析结果
Table 1. GC results of spheromone components in single pheromone gland extract of virgin female Dendrolimus kikuchii quantified from 3 geographic populations
成分
Components单个腺体组分的绝对含量(ng,N= 20)
Amount of components in single gland extract (ng, N= 20)湖南种群Hunan population 江西种群Jiangxi population 云南种群Yunnan population Z5, E7-12:OAc 1.34±0.21 a* 1.44±0.22 a 1.34±0.22 a Z5, E7-12:OH 0.14 ±0.03 a 0.12±0.03 a 0.08±0.02 b Z5-12:OAc 0.12 ±0.02 b 0.12±0.03 b 0.15±0.03 a 比例Ratio 100:10:9 100:9:8 100:6:11 *表中差异显著性检验是在α=0.05条件下进行横向比较的结果。 表 2 思茅松毛虫3个地理种群雄虫触角对Z5, E7-12:OAc,Z5, E7-12:OH和Z5-12:OAc的EAG剂量-反应数值
Table 2. Mean EAG responses of three Dendrolimus kikuchii populations to a range of stimulus loads of Z5, E7-12:OAc, Z5, E7-12:OH and Z5-12:OAc
刺激量
Stimulus loads/ngZ5, E7-12:OAc Z5, E7-12:OH Z5-12:OAc 湖南种群
N=45江西种群
N=33云南种群
N=34湖南种群
N=45江西种群
N=33云南种群
N=35湖南种群
N=45江西种群
N=35云南种群
N=351 0.04±0.01 d* 0.15±0.04 c 0.09±0.03 b 0.02±0.01 c 0.26±0.07 c 0.14±0.03 c 0.02±0.01 c 0.02±0.01 c 0.22±0.05 b 10 0.04±0.01 d 0.54±0.14 c 0.09±0.04 b 0.02±0.01 c 0.16±0.04 c 0.36±0.09 c 0.06±0.02 c 0.04±0.01 c 0.13±0.04 b 100 0.39±0.06 c 1.18±0.28 b 0.17±0.05 b 0.05±0.01 c 0.64±0.19 b 1.25±0.24 b 0.27±0.06 c 0.12±0.03 c 0.43±0.10 b 1 000 1.92±0.29 b 2.19±0.41 b 0.29±0.08 b 0.22±0.06 b 2.69±0.47 b 1.44±0.38 b 1.68±0.35 b 0.72±0.12 b 0.64±0.10 b 10 000 7.66±0.81 a 5.47±0.81 a 1.13±0.42 a 4.34±0.68 a 8.91±1.29 a 4.95±0.86 a 3.03±0.41 a 5.03±0.62 a 3.98±0.51 a *每栏后不同小写字母表示雄蛾触角对单一性信息素成分不同浓度梯度的EAG反应有显著差异(α=0.05),N为测定重复数。
Z5, E7-12:OAc:湖南F(4, 220)=184.59,P<0.05;江西F(4, 160)=31.39,P<0.05;云南F(4, 165)=76.62,P<0.05;
Z5, E7-12:OH:湖南F(4, 220)=36.76,P<0.05;江西F(4, 160)=78.66,P<0.05;云南F(4, 170)=30.22,P<0.05;
Z5-12:OAc:湖南F(4, 220)=48.77,P<0.05;江西F(4, 170)=58.64,P<0.05;云南F(4, 170)=45.24,P<0.05。 -
[1] 萧刚柔. 中国森林昆虫[M]: 第二版. 中国林业出版社, 1992, 946-947. [2] 孔祥波, 赵成华, 高伟. 4种松毛虫性信息素成分及在近缘种生殖隔离中的作用[J]. 科学通报, 2001, 46(17): 1435-1439. doi: 10.3321/j.issn:0023-074X.2001.17.007 [3] Kong X B, Sun X L, Wang H B, et al. Identification of components of the female sex pheromone of the Simao pine caterpillar moth, Dendrolimus kikuchiii Matsumura[J]. Journal of Chemical Ecology, 2011, 37(4): 412-419. doi: 10.1007/s10886-011-9932-5 [4] Klun J A, Chapman O L, Mattes K C, et al. Insect sex pheromones: minor amount of opposite geometrical isomers critical to attraction[J]. Science, 1973, 181(4100): 661-663. doi: 10.1126/science.181.4100.661 [5] Klun J A. Insect sex pheromones: intraspecific pheromonal variability of Ostrinia nubilalis in North America and Europe[J]. Environmental Entomology, 1975, 4(6): 891-894. doi: 10.1093/ee/4.6.891 [6] Kochansky J, Cardé R T, Liebherr J, et al. Sex pheromone of the European corn borer, Ostrinia nubilalis (Lepidoptera: Pyralidae), in New York[J]. Journal of Chemical Ecology, 1975, 1(2): 225-231. doi: 10.1007/BF00987871 [7] Roelofs W L, Liu W T, Hao G X, et al. Evolution of moth sex pheromones via ancestral genes[J]. Proceedings of the National Academy of Sciences of the United State of America, 2002, 99(21): 13621-13626. doi: 10.1073/pnas.152445399 [8] Roelofs W L, Rooney A P. Molecular genetics and evolution of pheromone biosynthesis in Lepidoptera[J]. Proceedings of the National Academy of Sciences of the United State of America, 2003, 100(16): 9179-9184. doi: 10.1073/pnas.1233767100a [9] Löfstedt C. Population variation and genetic control of pheromone communication system in moths[J]. Entomologia Experimentalis Et Applicata, 1990, 54(3): 199-218. doi: 10.1111/j.1570-7458.1990.tb01331.x -




 下载:
下载: