-
棉革菌属(Tomentella Pers. Ex Pat)隶属担子菌门(Basidiomycota)伞菌纲(Agaricomycetes)革菌目(Thelephorales)革菌科(Thelephoraceae)。棉革菌属真菌与松科(Pinaceae)、壳斗科(Fagaceae)、桦木科(Betulaceae)、杨柳科(Salicaceae)及部分草本和灌木植物[1-4]间形成互利共生体,其形态特征表现为:棉革菌属真菌在这些植物根系形成表型为棕色至深棕色、外层菌套细胞形状为多角形,具有外延菌丝、囊状体或菌索,多呈锁状联合的外生菌根[5-9]。据报道,棉革菌属在北温带、温带和热带地区森林生态系统的针叶林和阔叶落叶林中普遍存在且占主导地位[10-14],在维持生态系统稳定中发挥了重要作用。
在棉革菌属的外生菌根研究方面,国内外学者对近20种外生菌根的表型进行了详细的描述,同时采用分子鉴定的方法发现了相关的棉革菌属的真菌子实体和菌根序列约3 000条,并提交至GenBank数据库。国内对棉革菌属的外生菌根研究起步较晚,仅在20世纪末才开始逐渐得到关注。谢雪丹等在云南松(Pinus yunnanensis Franch.)的幼苗上发现6种棉革菌属菌根真菌并进行描述[15];樊永军等对青海云杉(Picea crassifolia Kom.)外生菌根的形态类型及分子鉴定中发现了棉革菌属菌根真菌[16];2013年王琴等对油松(P. tabulaeformis Carr.)的5种棉革菌属外生菌根的形态和解剖结构特征进行了报道[17];魏杰等在内蒙古的兴安落叶松(Larix gmelini (Rupr.) Rupr.)、白桦(Betula platyphylla Suk.)、青海云杉、山杨(Populus davidina Dode)和樟子松(P. sylvestris var. mongolica Litv.)等具有地带性分布的主要树种上都发现有棉革菌属外生菌根[18-19]。由此可见,我国棉革菌属真菌资源丰富。
雷公山国家级自然保护区位于贵州省东南部的黔东南州雷山县,处于珠江水系与长江水系的分水岭地带。该自然保护区所处地理位置及得天独厚的自然条件,加上地质历史上未受第四纪冰川侵袭,成为许多古老孑遗生物的避难所,蕴藏着丰富的生物资源,目前关于该自然保护区外生菌根研究尚未见报道。本研究以雷公山国家级自然保护区发现的棉革菌属外生菌根为研究对象,结合表型性状描述和分子鉴定的方法,首次报道雷公山国家级自然保护区的棉革菌属外生菌根的分布情况,为该自然保护区外生菌根真菌研究积累了宝贵基础资料,也为棉革菌属外生菌根与优势林分的共生关系及其在森林生态系统形成过程中的功能研究提供理论依据。
-
分别于2015、2016年的6—8月份,在雷公山国家级自然保护区的4类优势林分,即以苦槠栲(Castanopsis sclerophylla (Lindl.) Schott.)、丝栗栲(C. chinensis Hance)等构成的常绿阔叶林,以光皮桦(B. luminifera H. Winkl.)、响叶杨(P. adenopoda Maxim.)、化香树(Platycarya strobilacea Sieb. et Zucc.)等构成的落叶阔叶林,以马尾松(P. massoniana Lamb.)、秃杉(Taiwania flousiana Gaussen)等构成的暖性针叶林,以及以白栎(Quercus fabri Hance)、麻栎(Q. acutissima Carruth.)构成的灌丛林分中进行采样。
随机取样的方法:选取树龄10 a以上的成年大树为研究对象,用取样铲在样树周围挖取深度20 cm左右土层带小根的土样,装入自封袋,然后与冰袋一同放入采样箱带回实验室,于-20℃条件下冷冻保存待处理。
-
将根系样品置于ddH2O中浸泡,洗净后剪成长度2 cm的根段。将根段置于体视显微镜(Olympus SZX10,日本)下挑出菌根,并依据菌根不同的形态特征分类,每一类型的菌根均分成2份:一份保存于FAA溶液中用于形态观察和特征描述,另一份保存于CTAB溶液中用于分子鉴定。
-
采用体视显微镜观察菌根的表型特征分支类型、分支末端形状、颜色、表面性状和外延菌丝等。选取未分支末端剥离菌套,制成临时玻片,用临时玻片观察其解剖结构特征菌套内外层菌丝组织类型、菌丝排列方式、外延菌丝特征、菌索类型等。
-
DNA提取:对每一类根据形态和解剖结构特征确定的菌根类型,挑取1~2个根尖用于提取DNA。采用TaKaRa MiniBEST Plant Genomic DNA Extraction Kit试剂盒提取DNA。PCR扩增:PCR反应体系50 μL:DNA Template 2 μL,、引物ITS1f(CTTGGTCATTTAGAGGAAGTAA)和ITS4(TCCTCCGCTTATTGATATGC)各2 μL,2×Master Mixture 25 μL,用ddH2O补足至50 μL。PCR扩增反应在Eppendorf Masetercycler PCR仪上进行,扩增程序:94℃预变性5 min,94℃变性40 s,54℃退火60 s,72℃延伸60 s,35个循环,72℃平展10 min,0℃保存。
-
将PCR产物纯化后送南京金斯瑞生物科技有限公司进行测序。将测序所得的序列用Bioedit软件进行编辑,在UNITE中进行比对(BLAST),根据比对结果的一致性初步鉴定其种属类型。
-
运用贝叶斯法对被鉴定的外生菌根真菌DNA中ITS区段的碱基序列进行系统发育分析。首先在UNITE和NCBI中找到相近序列,运用Mafft和Cluster对序列进行编辑。在MrModeltest v2.3(Nylander 2004)程序中运用AIC运算,确定适用于分析的最佳模型为SYM+I+G,贝叶斯分析设置运行代数150万次,运行至平均标准偏差低于0.01时终止[12],其它参数设置保持默认。在MrBayes中后续运行Sump和Sumt指令,舍弃前25%代,对系统发育树进行总结和后验概率(Posterior probabilities,PPs)计算。
-
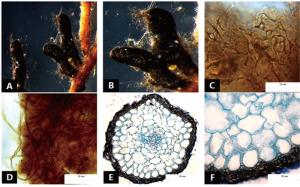
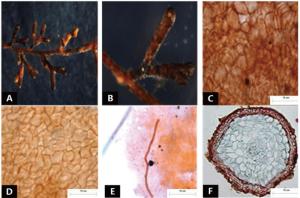
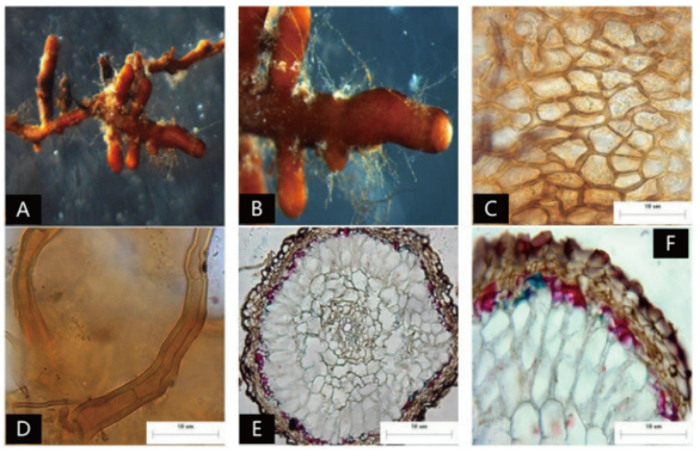
菌根系统单轴分支,呈金字塔状,0~2级,亲水。未分支末端膨大,呈棒状,幼嫩时为红褐色,成熟时棕褐色,表面性状为密羊毛状,有少量较长的外延菌丝,无囊状体(图 1A、B)。菌套表面不光滑,有光泽,菌套为密丝组织排列,菌丝细胞为多角,菌套类型为E型(图 1C)。外延菌丝褐色,菌丝壁较厚,边缘光滑,菌丝有隔,隔处无收缩呈分叉状,无明显锁状联合(图 1D)。该形态型分离自雷公山国家级自然保护区常绿阔叶林苦槠栲、丝栗栲等栲树根系。
-
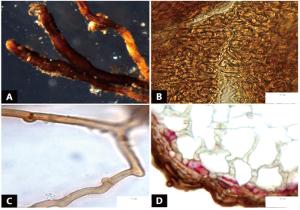
菌根系统单轴无分支,亲水。末端棒状,膨大,棕褐色,表面性状为密羊毛状,有大量外延菌丝,无囊状体(图 2A)。菌套表面凹凸不平,有光泽,不透明,菌套为密丝组织排列,菌丝细胞为三角至多角,菌套类型为L型(图 2B)。外延菌丝红褐色,菌丝壁较厚,边缘光滑,菌丝有隔,隔处无收缩呈分叉状,菌丝呈“十”字排列,无明显锁状联合(图 2C、D)。该形态型分离自雷公山国家级自然保护区落叶阔叶林光皮桦根系。
-
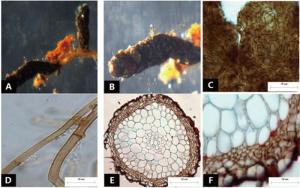
菌根系统单轴无分支,亲水。末端棒状膨大,略弯曲,黑色,表面性状为密羊毛状,有大量外延菌丝,无囊状体(图 3A、B)。菌套有光泽,不透明,菌套为拟薄壁组织排列,菌丝细胞为三角至多角,菌套类型为Q型(图C)。外延菌丝黑色,菌丝壁较厚,边缘光滑,菌丝有隔,隔处无收缩,呈分叉状,分无明显锁状联合(图 3D)。该形态型分离自雷公山国家级自然保护区暖性针叶林马尾松根系。
-
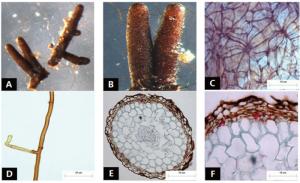
菌根系统单轴棒状,无分支,亲水。末端不膨大,略收缩,棕红色,表面性状为疏羊毛状,有少量外延菌丝,无囊状体(图 4A)。菌套有光泽,不透明,菌套为密丝组织排列,菌丝细胞为多角形,菌套类型为M型(图 4B)。外延菌丝红棕色,菌丝壁较厚,边缘光滑,菌丝有隔,隔处无收缩,呈不规则弯曲,有明显锁状联合(图 4C)。该形态型分离自雷公山国家级自然保护区灌丛的栎树根系。
-
菌根系统单轴棒状,无分支,亲水。末端不膨大,棕黑色,表面性状为密羊毛状,有少量较短的外延菌丝,无囊状体(图 5A、B)。菌套无光泽,不透明,菌套为密丝组织排列,菌丝细胞为多角形,菌套类型为M型(图 5C)。外延菌丝棕褐色,菌丝壁较厚,边缘光滑,菌丝有隔,隔处无收缩,有明显锁状联合(图 5D)。该形态型分离自雷公山国家级自然保护区暖性针叶林马尾松根系。
-
菌根系统单轴分支,呈羽状,0~2级,亲水。末端不膨大,棕褐色,表面性状为密羊毛状,有少量长的外延菌丝,无囊状体(图 6A、B)。菌套无光泽,不透明,菌套为密丝组织排列,菌丝细胞为多角形,菌套类型为G型(图 6C)。外延菌丝棕褐色,菌丝较粗,菌丝壁较厚,边缘光滑,菌丝有隔,隔处无收缩,有明显锁状联合(图 6D)。该形态型分离自雷公山国家级自然保护区暖性针叶林马尾松根系。
-
菌根系统单轴分支,呈二叉状,0~2级,亲水。顶端尖圆,末端不膨大,棕褐色,表面性状为密羊毛状,有少量长的外延菌丝,无囊状体(图 7A、B)。菌套无光泽,不透明,菌套为密丝组织排列,菌丝细胞为多角形,菌套类型为L型(图 7C、D)。外延菌丝红棕色,菌丝较粗,菌丝壁较厚,边缘光滑,菌丝有隔,隔处无收缩,有明显锁状联合(图 7E)。该形态型分离自雷公山国家级自然保护区落叶阔叶林光皮桦根系。
-
本试验中所采集的7种类型的棉革菌属外生菌根颜色均为较深的棕色至黑色,菌套均由角状细胞构成,而且有外延菌丝,这些形态特征与Jakucs等对棉革菌属外生菌根的形态特征描述相符合[20]。7种形态型的形态和解剖结构特征比较见表 1。
表 1 7种形态型的形态和解剖结构特征比较
Table 1. Comparison of morpho-anatomical structure features of 7 morphotypes
形态型Morphotypes 外形结构Overall structure 解剖结构Anatomical structures 颜色Color 表面性状Surface characteristics 外层菌套Outer mantle layer 内层菌套Inner mantle layer 外延菌丝Emanating mycelium 根状菌索Rhizomorph 1 棕褐色 密羊毛状 E型 密丝组织 少,无锁状联合 无 2 棕褐色 密羊毛状 L型 密丝组织 少,无锁状联合 无 3 黑色 密羊毛状 Q型 拟薄壁组织 多,无锁状联合 无 4 棕红色 疏羊毛状 M型 密丝组织 少,有锁状联合 无 5 棕黑色 密羊毛状 M型 密丝组织 少,有锁状联合 无 6 棕褐色 密羊毛状 G型 密丝组织 少,有锁状联合 无 7 棕褐色 密羊毛状 L型 密丝组织 少,有锁状联合 无 -
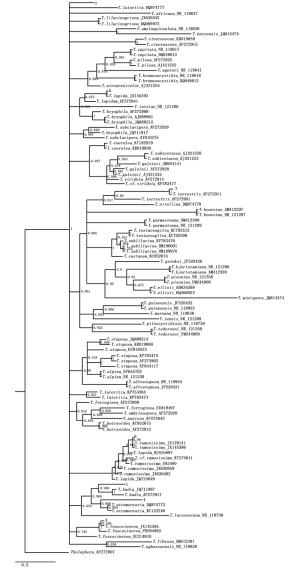
贝叶斯分析结果(图 8)表明:采集的样品中,7种形态型的序列都聚集在棉革菌属真菌的序列中,7种形态型的菌根都是由棉革菌属真菌形成的外生菌根。形态型1与T. badia聚成一支并且有较高的支持率(Bootstrap 0.999 9),形态型2与T. lateritia、T. africana聚成一支,形态型3与T. fuscocinerea构成一个独立分支(Bootstrap 1.000 0),形态型4与T. atramentaria构成一个独立分支(Bootstrap 0.999 9),形态型5与T. lapida构成一个独立分支(Bootstrap 1.000 0), 形态型6与T. ramosissima聚成一支并且有较高的支持率(Bootstrap 0.980 0),形态型7与T. terrestris聚成一支并且有较高的支持率(Bootstrap 1.000 0)。因此,形态型2不能确定到种,其它6种形态型均可以鉴定到种水平。
-
从雷公山国家级自然保护区的4类优势林分中鉴定获得的外生菌根具有棉革菌属的典型特征,并可划分为7种不同形态,但这7种形态的棉革菌属真菌通过表型、解剖和rDNA ITS特征分析仅可划分为6个类型。形态型1与T. badia构成一个独立分支,在形态和解剖结构特征上,二者均具有角状细胞构成的外层菌套,内层菌套为密丝组织,外延菌丝少,厚壁,无锁状联合。形态型2与T. lateritia、T. africana聚成一支,但在形态和解剖结构上它们之间却有很大的差别,形态型2外延菌丝较少,无锁状联合,而T. lateritia、T. africana二者均有大量外延菌丝而且具有锁状联合。形态型3是T. fuscocinerea形成的外生菌根类型,其外层菌套均具有由三角至多角状细胞构成的拟薄壁组织,从外层菌套细胞上延伸出来较多的外延菌丝,该外延菌丝细胞壁厚,而且无锁状联合。T. fuscocinerea在加拿大、丹麦、瑞典、匈牙利等国均有报道,既是外生菌根真菌,也是兰科(Orchidaceae)菌根真菌[20]。形态型4与T. atramentaria构成一个独立分支,在形态和解剖结构特征上,二者均具有角状细胞构成的外层菌套,外延菌丝少,菌丝细胞壁厚,而且具锁状联合。形态型5与T.lapida构成一个独立分支,形态型6与T. ramosissima聚成一支,形态型7与T. terrestris聚成一支,形态结构上均为少量的外延菌丝,均具有锁状联合,这些特征均符合Jakucs等[20]对块菌属(Tuber Micheli: Fr.)外生菌根特征的描述。因此,有6种类型可鉴定到种。
在国际基因库(NCBI和UNITE)中,目前还没有来自中国的棉革菌属真菌子实体的序列信息,这与棉革菌属真菌的子实体常附着于枯枝、腐木和岩石上,不易发现而被忽略有关,事实上对棉革菌属外生菌根的研究可以为该属真菌子实体的研究提供重要线索。
-
本研究从贵州雷公山国家级自然保护区的4类优势林分中分离得到7种不同类型的具有棉革菌属典型特征的外生菌根。采用表型分析、解剖结构和rDNA ITS序列测定的方法可将其中6种类型鉴定到种,分别为:T.badia、T.fuscocinerea、T.atramentaria、T. lapida、T. ramosissima和T. terrestris。棉革菌属外生菌根在雷公山国家级自然保护区的各个林分中均有分布,表明棉革菌属外生菌根真菌与常绿阔叶林、落叶阔叶林、暖性针叶林和灌丛林分形成与发育密切相关,在森林生态系统形成中可能发挥了重要作用。
雷公山国家级自然保护区7种棉革菌外生菌根形态描述和分子鉴定
Morphological Description and Molecular Identification of Seven Tomentella Ectomycorrhizae from Leigong Mountain Nature Reserve
-
摘要:
目的 研究雷公山国家级自然保护区的棉革菌属外生菌根的分布情况,探索外生菌根与林木互利共生的关系。 方法 采用表型分析和rDNA ITS序列分析等方法,对贵州雷公山国家级自然保护区的常绿阔叶林、落叶阔叶林、暖性针叶林、灌丛4种优势林分的外生菌根进行研究。 结果 表明:基于形态及解剖结构特征分析,从4种优势林分中分离得到7种具有棉革菌属(Tomentella)典型特征(如颜色为棕色)的外生菌根;rDNA ITS区段系统发育分析表明,分离得到的7种外生菌根隶属棉革菌属,并可将其中6种形态型分别鉴定为T.badia、T.fuscocinerea、T.atramentaria、T.lapida、T.ramosissima和T.terrestris。 结论 首次从雷公山国家级自然保护区发现棉革菌属外生菌根真菌6种,为该属外生菌根与优势林分的共生关系及功能研究等提供参考。 Abstract:Objective To explore the ectomycorrhizae types and relationship with forest stands at Leigong Mountain Nature Reserve, and to study the ectomycorrhizae in four preponderant forest stands. Method The methods of random sampling and rDNA ITS sequencing were applied in this study. Result The results showed that seven types of genus Tomentella were determined by phenotype with brown morphotypes that was similar with genus Tomentella, and the results was verified by rDNA ITS sequencing, . Six of them were identified as T. badia, T. fuscocinerea, T. atramentaria, T. lapida, T. ramosissima and T. terrestris, respectively. Conclusion This research is the first report that the genus Tomentella was found at Leigong Mountain Nature Reserve, so the results will benefit for next research at commensalism and function with four preponderant forest stands at Leigong Mountain Nature Reserve. -
Key words:
- Tomentella
- / ectomycorrhiza
- / morphological feature
- / molecular identification
-
表 1 7种形态型的形态和解剖结构特征比较
Table 1. Comparison of morpho-anatomical structure features of 7 morphotypes
形态型Morphotypes 外形结构Overall structure 解剖结构Anatomical structures 颜色Color 表面性状Surface characteristics 外层菌套Outer mantle layer 内层菌套Inner mantle layer 外延菌丝Emanating mycelium 根状菌索Rhizomorph 1 棕褐色 密羊毛状 E型 密丝组织 少,无锁状联合 无 2 棕褐色 密羊毛状 L型 密丝组织 少,无锁状联合 无 3 黑色 密羊毛状 Q型 拟薄壁组织 多,无锁状联合 无 4 棕红色 疏羊毛状 M型 密丝组织 少,有锁状联合 无 5 棕黑色 密羊毛状 M型 密丝组织 少,有锁状联合 无 6 棕褐色 密羊毛状 G型 密丝组织 少,有锁状联合 无 7 棕褐色 密羊毛状 L型 密丝组织 少,有锁状联合 无 -
[1] Bidartondo M I, Bruns T D. Extreme specificity in epiparasitic Monotropoideae (Ericaceae):widespread phylogenetic and geographical structure[J]. Molecular Ecology, 2001, 10(9):2285-2295. doi: 10.1046/j.1365-294X.2001.01358.x [2] Selosse M A, Bauer R, Moyersoen B. Basal hymenomycetes belonging to the Sebacinaceae are ectomycorrhizal on temperate deciduous trees[J]. New Phytologist, 2002, 155(3):183-195. [3] McCormick C J, Challinor L, Macdonald A, et al. Introduction of replication-competent hepatitis C virus transcripts using a tetracycline-regulable baculovirus delivery system[J]. Journal of General Virology, 2004, 85(2):429-439. doi: 10.1099/vir.0.19676-0 [4] Julou T, Burghardt B, Gebauer G, et al. Mixotrophy in orchids insights from a comparative study of green individuals and nonphotosynthetic individuals of Cephalanthera damasonium[J]. New Phytologist, 2005, 166(2):639-665. doi: 10.1111/j.1469-8137.2005.01364.x [5] Jakucs E, Kovács G M, Szedlay G, et al. Morphological and molecular diversity and abundance of tomentelloid ectomycorrhizae in broad-leaved forests of the Hungarian Plain[J]. Mycorrhiza, 2005, 15(6):459-470. doi: 10.1007/s00572-005-0351-8 [6] Jakucs E, Erös-Honti Z. Morphological-anatomical characterization and identification of Tomentella ectomycorrhizas[J]. Mycorrhiza, 2008, 18(6-7):277-285. doi: 10.1007/s00572-008-0183-4 [7] Agerer R. Fungal relationships and structural identity of their ectomycorrhizae[J]. Mycological Progress, 2006, 5(2):99-107. [8] Walker J F, Miller O K, Hrton J L. Hyperdiversity of ectomycorrhizal fungus assemblages on oak seedlings in mixed forests in the southern Appalachian Mountains[J]. Molecular Ecology, 2005, 14(4):829-838. [9] Nylander J A A. MrModeltest v2. Program distributed by the author[M]. Uppsala:Evolutionary Biology Centre, Uppsala Universit, 2004. [10] De Roman M, Claveria V, De Miguel A M. A revision of the descriptions of ectomycorrhizas published since 1961[J]. Mycological Research, 2005, 109(10):1063-1104. doi: 10.1017/S0953756205003564 [11] Horton T R, Bruns T D. The molecular revolution in ectomycorrhizal ecology:peeking into the black box[J]. Molecular Ecology, 2001, 10(8):1855-1871. doi: 10.1046/j.0962-1083.2001.01333.x [12] Huelsenbeck J P, Ronquist F. Bayesian analysis of molecular evolution using MrBayes[M]//Nielsen R. Statistical Methods in Molecular Evolution. New York: Springer, 2005. [13] Smith M E, Douhan G W, Fremier A K, et al. Are true multihost fungi the exception or the rule dominant ectomycorrhizal fungi on Pinus sabiniana differ from those on co-occurring Quercus species[J]. New Phytologist, 2009, 182(2):295-299. doi: 10.1111/j.1469-8137.2009.02801.x [14] Wei J, Agerer R. Three ectomycorrhizae of Thelephoraceae on Chinese pine (Pinus tabulaeformis) and a key to thelephoroid Ectomycorrhizae[J]. Nova Hedwigia, 2010, 91(1-2):165-186. [15] 谢雪丹, 刘培贵.云南松幼苗棉革菌属菌根真菌的物种多样性[J].菌物研究, 2011, 9(4):224-231, 243. doi: 10.3969/j.issn.1672-3538.2011.04.008 [16] 樊永军, 闫伟, 王黎元.贺兰山地区青海云杉外生菌根的形态类型及分子鉴定[J].林业科学, 2011, 47(6):108-113. [17] 王琴, 郭良栋.油松外生菌根的形态解剖结构特征[J].林业科学, 2013, 49(2):100-107. [18] 魏杰, 张文泉, 闫伟.樟子松4种深色外生菌根研究[J].干旱区资源与环境, 2015, 29(4):178-183. [19] 魏杰, 郭晓笑, 杨旭东.内蒙古地区5种棉革菌外生菌根形态描述和分子鉴定[J].菌物学报, 2017, 36(7):870-878. [20] Jakucs E, Erös-Honti Z, Seress D, et al. Enhancing our understanding of anatomical diversity in Tomentella ectomycorrhizas:characterization of six new morphotypes[J]. Mycorrhiza, 2015, 25(6):419-429. doi: 10.1007/s00572-014-0622-3 -




 下载:
下载: