-
湿地松(Pinus elliottii Engelm)原产美国,是一种优良的脂材两用树种,现已成为中国南方丘陵区最主要的造林树种之一[1];但因其林下极少有其它物种生长,层次单一,结构简单,造成其抗病、虫能力差,进而导致地力衰退。国内外对湿地松施肥有大量的研究,对各个年龄阶段湿地松增施氮肥6~10 a后,均显著地促进了湿地松的生长[2]。Cropper等[3]和Zhao等[4]对湿地松林反复施肥,使其生长量和生产力提高。徐有明等[5]研究结果表明,磷肥、磷肥与氮、磷肥与钾配比施肥以及氮、磷、钾配比施肥显著促进湿地松树高、胸径的生长;但化学肥料的大量使用容易造成环境污染,进一步加重土壤性质的恶化,化肥利用率持续下降,氮肥利用率仅10%~30%,磷肥利用率低于20%[6]。目前,细菌肥料在培肥地力、降低植物土传病害、净化和修复土壤及保护环境等方面发挥了重要作用。研究表明,细菌肥料可以促进杨树、桉树、马尾松、桑树、油茶及核桃等林木的生长发育[7-13]。目前,湿地松施肥研究大多局限于化学肥料及复合肥,有关细菌肥料的研究论文数量较少,且大部分仅仅局限于对林木生长的促进作用及土壤养分的影响,系统研究细菌肥料对林木生长、土壤物理性质、化学性质、土壤酶、土壤微生物影响的研究报道相对较少。
土壤养分、微生物和土壤酶是森林生态系统的重要组成部分,是评价土壤质量的重要指标[14-15]。土壤养分是存在于土壤中植物生长发育所需要的营养元素,对林木生长发育发挥着重要作用。土壤微生物和土壤酶参与土壤中许多重要的生化反应,对土壤养分循环转化和能量流动起着重要作用,二者一起推动土壤的代谢过程,影响土壤质量,从而影响林木生长发育[16]。因此,关于森林土壤养分、微生物和酶的研究受到广泛重视。本文旨在研究细菌肥料对湿地松幼龄林生长及土壤性质的影响,为施用细菌肥料的作用机理及在湿地松上的应用提供科学依据,以期在湿地松增产的同时又可保持良好的生态环境。
-
试验地位于江西省分宜县大岗山山下林场(27°30′ N,114°30′ E),以低山丘陵为主,土壤为黄壤和红壤,属于中亚热带季风湿润气候,具有四季分明、雨量充沛、阳光充足、气候温和、无霜期长、严冬较短的特征。常年平均气温17.7℃,年平均降水量1 595 mm。
-
2016年6月在分宜试验地选择湿地松幼龄林的代表性样地,选择地径1.6 cm左右、苗高80 cm左右的林木进行试验。试验采用随机区组设计,设置3个区组,3个处理,分别为细菌肥料处理(B)、基质对照处理(M)及不施用任何肥料的空白对照处理(CK),每个处理设置30株湿地松幼苗,合计90株。细菌肥料所用菌株为中国林业科学研究院林业研究所森林土壤研究室筛选的具有溶磷、拮抗土传病原菌能力且能够产生植物生长刺激物的细菌菌株Microbacterium testaceum(专利号:ZL2010 1 0267089.X),基质为农林废弃物经微生物腐熟菌发酵生成的人造腐殖质,由北京天地成微生物技术有限公司生产,细菌肥料有效活菌数可达5×108 cfu·g-1,细菌肥料处理中每株湿地松的菌肥用量为500 g(已进行试验确定的最佳施肥量),基质对照中基质用量为500 g,3种处理日常管理完全一致。
2016年6月对试验地内湿地松幼苗的株高和地径进行测量,同时采集土壤样品对土壤理化性质、酶活性和微生物多样性的本底值进行测定。2016年7月开始对样地进行施肥处理,采用环状沟施法,即在树冠垂直投影外20~30 cm处,以树干为中心,挖一条宽10~20 cm、深20~30 cm的环状沟,沿沟施各种细菌肥料,然后覆土。
-
2017年11月在每个试验处理小区测量每株湿地松的地径和株高。3个区组内的3个处理中均设置9个1 m × 2 m样方,在样方内采用5点取样法采集0~20 cm的土壤,将每个样方内的土样混合均匀后在4℃条件下保存,样地内共采集81个土壤样品,同时采集环刀样,用于测定土壤物理性质,尽快带回实验室进行分析。
株高和地径分别用钢卷尺及电子数显卡尺测量,土壤物理性质采用环刀法进行测定,有机质的测定采用重铬酸钾氧化法,水解性氮采用碱解扩散法,有效磷采用氟化铵—盐酸浸提—连续流动分析仪法进行测定,速效钾采用乙酸铵浸提—电感耦合等离子质谱仪(ICP-MS)测定,蔗糖酶活性采用3,5-二硝基水杨酸比色法[17],脲酶、酸性磷酸酶和过氧化氢酶活性采用酶活性测定试剂盒(青岛捷世康生物科技有限公司)测定。微生物群落功能多样性用Biolog-ECO板进行分析,接种液的制备和测定采用Classen等[18]的方法:首先,将土壤样品在25℃条件下活化24 h,取相当于10 g烘干质量的新鲜土壤放入90 mL 0.145 mol·L-1 NaC1溶液,200 r·min-1振荡30 min,取10 mL上清液加入到90 mL NaC1溶液,混匀后取10 mL上清液加入到90 mL NaC1溶液,最终稀释比例为1:1 000;将接种液移至储液槽,用排枪向ECO板各培养基孔加入150 μL稀释液,每个样品3个重复;将接种好的ECO板放入25℃的恒温培养箱中,分别于24、36、48、72、96、120、144、168 h后用Gen Ⅲ Micro Station自动快速微生物鉴定仪(美国Biolog公司)进行测定,测定波长分别为590 nm(颜色+浊度)和750 nm(浊度)。
-
AWCD是表征微生物代谢强度的指标,计算公式如下:
$AWCD = \frac{1}{n}\sum\limits_{i = 1}^n {(Ci - R)} $
式中:Ci为每个碳源孔在590 nm和750 nm下的吸光度值之差,其中,数值小于0.06的修正为0[19];R为对照孔的光密度值;n为生态板中碳源种类数,本研究中为31。
-
用Shannon指数(H)、Simpson指数(D)、Pielou指数(J)和丰富度指数(S)来表征,用72 h的测定值来计算[20]。
Shannon-Wiener多样性指数(H):
$H = - \sum\limits_{i = 1}^s P i\log Pi $
式中:Pi为第i个非对照孔中的吸光度值(Ci)与所有非对照孔吸光度值总和的比值。
Simpson指数(D):
$D = 1 - \sum {{{(Pi)}^2}} $
丰富度指数(S):指被利用碳源的总数目,该研究中为非对照孔与对照孔吸光度的差值大于0.25的孔数。
Pielou均匀度指数(J):
$J = H/\ln S $
计算所得数据利用Excel进行初步的数据处理,单因素方差分析采用SPSS20.0软件进行(α=0.05)。
-
由图 1可知:不同处理湿地松幼苗株高和地径的相对增长量存在一定差异,变化规律均为细菌肥料处理>基质对照处理>空白对照处理,其中,空白对照、基质对照和细菌肥料处理地径的相对增长量分别为98.27%、105.53%和123.09%,株高的相对增长量分别为55.69%、66.56%和85.18%,细菌肥料处理与基质对照和空白对照处理在地径和株高的相对增长量上均存在显著差异,而基质对照与空白对照在株高的相对增长量上存在显著差异,在地径增长量上则差异不显著。细菌肥料与基质均促进了湿地松幼苗的生长,但细菌肥料的促进作用更显著。
-
与空白对照相比,细菌肥料处理使土壤密度降低,而土壤毛管孔隙度、非毛管孔隙度及最大持水量上升(表 1),其中,土壤毛管孔隙度、非毛管孔隙度及最大持水量在2个处理间差异显著。细菌肥料改善了土壤的疏松程度,有利于根系伸展,增强了土壤的持水能力。基质对照处理也降低了土壤密度,提高了土壤毛管孔隙度、非毛管孔隙度及最大持水量,但与空白对照差异不显著。
表 1 不同处理土壤物理性质
Table 1. Soil physical properties of different treatments
处理
Treatments土壤密度
Soil density/(g·cm-3)毛管孔隙度
Capillary porosity/%非毛管孔隙度
Non-capillary porosity/%最大持水量
Maximum water-holding capacity/(g·kg-1)空白对照Blank control 1.43±0.02 a 34.62±2.34 b 13.28±0.82 b 272.92±5.38 b 基质对照Matrix control 1.41±0.12 a 35.06±2.19 b 13.21±0.33 b 280.45±3.29 b 细菌肥料Bacterial fertilizer 1.38±0.07 a 41.75±1.76 a 15.76±0.12 a 309.27±4.92 a 注:表中不同小写字母表示同一测定指标在不同处理间差异显著(P<0.05)。下同。
Note: Different small letters indicates significant difference in different treatments for the same index(P<0.05).The same below. -
表 2表明:与空白对照相比,基质对照和细菌肥料处理均可以促进湿地松土壤有机质、有效磷、水解性氮和速效钾含量的提高,改良不良立地,其中,细菌肥料与空白对照在有机质、有效磷和速效钾含量上均差异显著,在水解性氮含量上差异不显著,而空白对照与基质对照只在有机质含量上差异显著,在水解性氮、有效磷和速效钾含量上差异不显著。
表 2 不同处理下土壤养分含量
Table 2. Soil nutrient content of different treatments
处理
Treatments有机质
Soil organic matter
/(g·kg-1)水解性氮
Alkali-hydrolyzable nitrogen
/(mg·kg-1)有效磷
Available phosphorous
/(mg·kg-1)速效钾
Available potassium
/(mg·kg-1)空白对照Blank control 24.19±0.86 b 41.71±1.78 a 1.73±0.20 b 34.78±2.92 b 基质对照Matrix control 31.02±0.67 a 42.34±3.13 a 1.96±0.09 b 40.21±3.63 b 细菌肥料Bacterial fertilizer 33.70±2.14 a 45.55±2.72 a 2.33±0.35 a 55.79±3.25 a -
土壤酶活性与土壤中微生物活性及土壤养分转化及其运移能力密切相关,可以作为评价土壤肥力水平的指标[21-22]。表 3表明:土壤中过氧化氢酶、蔗糖酶、磷酸酶和脲酶活性均为细菌肥料处理>基质对照处理>空白对照处理,且细菌肥料处理与基质对照和空白对照间4种土壤酶活性均差异显著,而基质对照与空白对照间仅脲酶活性差异显著。
表 3 不同处理土壤酶活性
Table 3. Soil enzyme activity of different treatments
处理
Treatments过氧化氢酶
Catalase/(mL·g-1)蔗糖酶
Invertase/(mg·g-1)磷酸酶
Phosphatase/(mL·g-1)脲酶
Urease/(mg·g-1)空白对照Blank control 1.41±0.11 b 7.26±0.41 b 26.93±1.06 b 0.146±0.00 c 基质对照Matrix control 1.60±0.08 b 7.89±0.53 b 27.19±0.61 b 0.159±0.02 b 细菌肥料Bacterial fertilizer 1.83±0.06 a 10.87±1.14 a 30.50±2.36 a 0.172±0.01 a -
图 2表明:在培养后24 h内,不同处理土样的AWCD值几乎无变化,此时碳源基本未被利用,表明微生物要利用不同碳源底物需要一个适应时间;随着培养时间的增加,在测定周期内AWCD值呈上升趋势;细菌肥料处理的AWCD在24~168 h内均高于空白对照及基质对照,且细菌肥料与空白对照和基质对照间均差异显著,空白对照与基质对照间差异不显著。
-
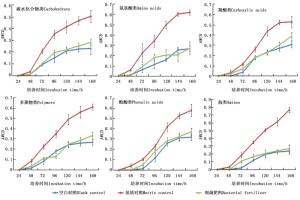
Biolog-ECO板中的31种碳源按化学基团的性质可分为碳水化合物类、羧酸类、氨基酸类、酚酸类、多聚物类和胺类6大类[23]。由图 3可见:与空白对照相比,细菌肥料处理土壤微生物在24~168 h内对6类碳源的利用能力均高于空白对照,基质对照处理的土壤微生物对碳水化合物、羧酸类、酚酸类以及胺类的利用能力在测定时间内均高于空白对照。
对各处理6类碳源72 h的AWCD值进行方差分析,结果表明:细菌肥料与基质对照和空白对照土样中微生物对6类碳源的利用均存在显著差异,而基质对照与空白对照间差异不显著。
-
对不同施肥处理下土壤样品的Shannon指数(H)、Simpson指数(D)、Pielou指数(J)和丰富度指数(S)进行多样性分析,以表明群落本身的物种组成和个体数量分布的特征。由表 4可知:土壤微生物群落的4种指数均为细菌肥料处理>基质对照处理>空白对照处理,且细菌肥料处理与空白对照之间的4种指数均差异显著,而基质对照与空白对照之间则差异不显著。
表 4 不同处理土壤微生物群落功能多样性指数
Table 4. Diversity index of soil microbial community of different treatments
处理Treatments H D S J 空白对照Blank control 1.031±0.056 b 0.841±0.013 b 8.616±0.816 b 0.962±0.039 b 基质对照Matrix control 1.075±0.035 ab 0.862±0.010 b 9.772±0.913 b 1.020±0.026 ab 细菌肥料Bacterial fertilizer 1.157±0.018 a 0.922±0.005 a 12.333±0.471 a 1.146±0.055 a -
研究结果表明,细菌肥料显著提高了土壤微生物对6类碳源的利用能力,增强了土壤微生物群落的代谢活性,同时,土壤微生物群落多样性指数、丰富度指数、均匀度指数及优势度指数均显著高于空白对照,提高了土壤微生物功能多样性,从而增强了土壤微生物群落的生态功能,但基质对照与空白对照间差异不显著。这与已有的研究结果,硅酸盐细菌肥料配施有机肥料提高了土壤真菌、放线菌和硅酸盐细菌数量以及土壤微生物生物量,明显改善农田土壤生态[24];益生菌解淀粉芽孢杆菌和荧光假单胞菌的添加增加了土壤细菌、放线菌、解淀粉芽孢杆菌和荧光假单胞菌数量[25]的结论基本一致。酶是土壤组分中最活跃的有机成分之一,土壤酶和土壤微生物共同推动土壤的代谢过程[26]。土壤酶活性可以作为衡量土壤生物学活性、土壤生产力和土壤肥力的重要指标[27]。本研究表明,施用细菌肥料的土壤中过氧化氢酶、蔗糖酶、磷酸酶及脲酶活性均显著高于空白对照,而基质对照与空白对照间过氧化氢酶、蔗糖酶和磷酸酶活性差异不显著。细菌肥料使土壤酶活性提高可能是由于细菌肥料中的活体微生物起的作用,活的生物菌体在代谢过程中可以释放一些酶[28],也可能是通过改善土壤中外部环境如酸碱平衡、提高土壤养分含量和物理性能等,为土壤酶提供适宜的外部环境条件来提高土壤酶活性。
王旭辉等[29]研究发现,菌肥使土壤中有效磷、有效钾含量增加。吉牛拉惹等[30]也发现,生物菌肥显著提高了土壤中有机质、有效磷、速效钾及水解性氮的含量。本研究中,细菌肥料显著提高了土壤中有效磷含量,可能是因为菌肥中溶磷菌株Microbacterium testaceum的溶磷作用将土壤中的无效磷转化为有效磷,同时细菌肥料使土壤中磷酸酶活性提高,催化土壤中含磷有机物矿化分解为有效磷。细菌肥料还提高了土壤中水解性氮的含量,这与土壤中脲酶活性提高有关,脲酶活性的提高可以促进土壤中稳定性较高的有机氮转化为有效氮。此外,细菌肥料处理的土壤中有机质和速效钾含量也显著高于空白对照,这可能与菌肥中的解钾微生物以及土壤中过氧化氢酶、蔗糖酶等酶活性提高有关。研究表明,过氧化氢酶活性越高,越有利于土壤养分的积累[31],而蔗糖酶可以作为转化酶参与碳素的循环过程。研究发现,细菌肥料降低了土壤密度,使土壤毛管孔隙度、非毛管孔隙度以及最大持水量上升,这可能是由于细菌肥料中的活性益生菌促使植物分泌大量分泌物与矿物胶体、有机胶体相结合,形成了土壤团粒结构[32],从而改善了土壤的疏松程度,提高土壤保水保肥性能,增强土壤的物理性能;同时土壤理化性质的改善为土壤微生物代谢和土壤酶提供了适宜的环境,进而使土壤微生物和土壤酶活性有所提高。土壤物理性能的改善还有利于植物根系的伸展以及土壤水分的保持和渗透,细菌肥料还提高了土壤有效磷、有机质和速效钾等养分含量,二者一起为湿地松的生长提供了良好的生存环境,从而使湿地松的株高和地径均显著高于空白对照,细菌肥料明显地促进了湿地松的生长。
-
细菌肥料显著促进了湿地松幼苗的生长,同时显著提高了土壤中有机质、有效磷、速效钾和碱解氮等养分含量以及土壤毛管孔隙度、非毛管孔隙度和最大持水量,降低了土壤密度,改善了土壤理化性质。此外,土壤微生物活性及微生物群落的多样性、丰富度和均匀度指数均有显著提高。与空白对照相比,基质对照也改善了土壤理化性质、土壤酶活性和微生物代谢活性,进而促进了湿地松幼苗的生长,但效果并不显著。
细菌肥料对湿地松幼龄林生长及土壤性质的影响
Effects of Bacterial Fertilizers on the Growth and Soil Properties of Pinus elliottii Young Stand
-
摘要:
目的 通过研究细菌肥料对湿地松幼龄林生长及对土壤养分、微生物群落功能多样性和酶活性的影响,为细菌肥料对湿地松土壤改良的应用提供参考,以期在促进湿地松生长及改良土壤的同时保持良好的生态环境。 方法 2016年7月在江西省分宜县山下林场采用随机区组设计,设置3个区组,3个处理,分别为细菌肥料处理、基质对照处理及不添加任何肥料的空白对照处理。2017年11月测量湿地松的株高和地径,采用5点取样法采集土壤样品,测定土壤密度、毛管孔隙度、非毛管孔隙度、最大持水量、有机质、有效磷、速效钾、水解性氮以及过氧化氢酶、磷酸酶、蔗糖酶和脲酶活性,用Biolog-ECO板分析微生物群落功能多样性。 结果 细菌肥料显著促进了湿地松幼苗株高和地径的增长,空白对照、基质对照处理和细菌肥料处理地径的相对增长量分别为98.27%、105.53%和123.09%,株高的相对增长量分别为55.69%、66.56%和85.18%,细菌肥料处理和基质对照处理均降低了土壤密度,增加了土壤毛管孔隙度、非毛管孔隙度以及最大持水量,改善了土壤物理性质,但细菌肥料处理的作用更显著。细菌肥料和基质对照均提高了湿地松土壤的有机质、有效磷、水解性氮以及速效钾含量,但细菌肥料处理与空白对照处理之间在4种养分含量上均存在显著性差异,而基质对照与空白对照之间只在有机质含量上存在显著性差异。细菌肥料处理显著提高了土壤磷酸酶、过氧化氢酶、蔗糖酶以及脲酶活性,细菌肥料还使土壤微生物群落代谢活性、对6类碳源(碳水化合物类、氨基酸类、羧酸类、多聚物类、酚酸类和胺类)的利用能力以及土壤微生物群落的Shannon多样性指数(H)、Simpson优势度指数(D)、Pielou均匀度指数(J)和丰富度指数(S)显著提高,基质对照也促进了上述指标的升高,但效果并不显著。 结论 细菌肥料处理和基质对照处理均可以促进湿地松幼苗的生长,提高湿地松土壤有机质、有效磷、速效钾以及水解性氮的含量,同时使土壤过氧化氢酶、磷酸酶、蔗糖酶以及脲酶活性升高,提高土壤微生物多样性、均匀度、丰富度以及优势度指数,提高了微生物对单一碳源的利用能力以及代谢活性,但细菌肥料的作用效果更为显著,基质对照的作用效果并不显著 Abstract:Objective The effects of bacterial fertilizers on the growth of pine young stand, microbial community functional diversity, enzyme activities and soil nutrient content were studied to provide references for the application of bacterial fertilizers, and to promote the growth of Pinus elliottii forest and improve soil while maintaining a good ecological environment. Method Three blocks and three treatments (bacterial fertilizer treatment, matrix control treatment and the blank control treatment adding no fertilizer) for every block were set up in July 2017 by random block design in Fenyi County, Jiangxi Province. In November 2017, The tree height and diameter of P. elliottii were measured, the soil density, capillary porosity, non-capillary porosity, maximum water-holding capacity, organic matter, available phosphorus, available potassium and alkaline nitrogen were measured by 5-point sampling, and the soil catalase, phosphatase, sucrase and urease activity were analyzed. The functional diversity of microbial community was analyzed by Biolog-ECO plate. Result The bacterial fertilizer significantly promoted the growth of P. elliottii seedlings, the growth rate of ground diameter of the blank control treatment, matrix control treatment and bacterial fertilizer treatment were 98.27%, 105.53% and 123.09%, respectively, and the growth rate of tree height were 55.69%, 66.56% and 85.18%. The bacterial fertilizer treatment and matrix control treatment reduced soil density, increased soil capillary porosity, non-capillary porosity and maximum water-holding capacity, and improved soil physical properties, however, the effect of bacterial fertilizer treatment was more significant. The contents of organic matter, available phosphorus, available potassium and alkaline nitrogen in soil increased by matrix control treatment and bacterial fertilizer treatment, and there was significant difference in all of the 4 nutrient contents between the bacterial fertilizer treatment and the blank control treatment, while there was significant difference between the matrix control and the blank control only in the organic matter content. Bacterial fertilizer treatment significantly increased the activities of soil phosphatase, catalase, sucrase and urease, it also promoted the soil microbial community activity, the utilization capacity of six kinds of carbon sources (carbohydrates, amino acids, carboxylic acids, polymers, phenolic acids and amines), and contributed to Shannon's diversity index, Simpson's dominance index, Pielou's evenness index and richness index of soil microbial community. The matrix control also contributed to the increase of the above-mentioned indicators, but the effect was not significant. Conclusion Bacterial fertilizer and matrix control can promote the growth of P. elliottii seedlings, improve soil organic matter, available phosphorus, available potassium and alkaline nitrogen content in soil, and increase the activities of catalase, phosphatase, invertase and urease. In addition, they improve soil microbial diversity, evenness, abundance and dominance index, and improve the utilization and metabolic activity of microorganisms to single carbon sources. The effect of bacterial fertilizer is more significant, while the effect of matrix control is not significant. -
Key words:
- bacterial fertilizer
- / Pinus elliottii
- / growth status
- / soil properties
- / soil enzyme
- / soil microbial diversity
-
表 1 不同处理土壤物理性质
Table 1. Soil physical properties of different treatments
处理
Treatments土壤密度
Soil density/(g·cm-3)毛管孔隙度
Capillary porosity/%非毛管孔隙度
Non-capillary porosity/%最大持水量
Maximum water-holding capacity/(g·kg-1)空白对照Blank control 1.43±0.02 a 34.62±2.34 b 13.28±0.82 b 272.92±5.38 b 基质对照Matrix control 1.41±0.12 a 35.06±2.19 b 13.21±0.33 b 280.45±3.29 b 细菌肥料Bacterial fertilizer 1.38±0.07 a 41.75±1.76 a 15.76±0.12 a 309.27±4.92 a 注:表中不同小写字母表示同一测定指标在不同处理间差异显著(P<0.05)。下同。
Note: Different small letters indicates significant difference in different treatments for the same index(P<0.05).The same below.表 2 不同处理下土壤养分含量
Table 2. Soil nutrient content of different treatments
处理
Treatments有机质
Soil organic matter
/(g·kg-1)水解性氮
Alkali-hydrolyzable nitrogen
/(mg·kg-1)有效磷
Available phosphorous
/(mg·kg-1)速效钾
Available potassium
/(mg·kg-1)空白对照Blank control 24.19±0.86 b 41.71±1.78 a 1.73±0.20 b 34.78±2.92 b 基质对照Matrix control 31.02±0.67 a 42.34±3.13 a 1.96±0.09 b 40.21±3.63 b 细菌肥料Bacterial fertilizer 33.70±2.14 a 45.55±2.72 a 2.33±0.35 a 55.79±3.25 a 表 3 不同处理土壤酶活性
Table 3. Soil enzyme activity of different treatments
处理
Treatments过氧化氢酶
Catalase/(mL·g-1)蔗糖酶
Invertase/(mg·g-1)磷酸酶
Phosphatase/(mL·g-1)脲酶
Urease/(mg·g-1)空白对照Blank control 1.41±0.11 b 7.26±0.41 b 26.93±1.06 b 0.146±0.00 c 基质对照Matrix control 1.60±0.08 b 7.89±0.53 b 27.19±0.61 b 0.159±0.02 b 细菌肥料Bacterial fertilizer 1.83±0.06 a 10.87±1.14 a 30.50±2.36 a 0.172±0.01 a 表 4 不同处理土壤微生物群落功能多样性指数
Table 4. Diversity index of soil microbial community of different treatments
处理Treatments H D S J 空白对照Blank control 1.031±0.056 b 0.841±0.013 b 8.616±0.816 b 0.962±0.039 b 基质对照Matrix control 1.075±0.035 ab 0.862±0.010 b 9.772±0.913 b 1.020±0.026 ab 细菌肥料Bacterial fertilizer 1.157±0.018 a 0.922±0.005 a 12.333±0.471 a 1.146±0.055 a -
[1] 肖兴翠, 李志辉, 张志兰, 等.施肥对湿地松中龄林生长及土壤的影响[J].中国农学通报, 2015, 31(16):6-13. doi: 10.11924/j.issn.1000-6850.casb14120021 [2] Fisher R F, Pritchett W L.Slash pine growth response to different nitrogen fertilizers[J].Soil Science Society of America Journal, 1982, 46(1):133-136. doi: 10.2136/sssaj1982.03615995004600010025x [3] Cropper W P, Gholz H L.Evaluating potential response mechanisms of a forest stand to fertilization and night temperature:a case study using Pinus elliottii[J].Ecological Bulletins, 1994(43):102-108. [4] Zhao D, Kane M, Borders B, et al. 2009.Long-term effects of site preparation treatments, complete competition control, and repeated fertilization on growth of slash pine plantations in the flatwoods of the southeastern United States[J].Forest Science, 2009, 55(5):403-410. [5] 徐有明, 林汉, 李贻锉, 等.施肥对湿地松幼林生长和木材物理力学性质的影响[J].林业科学, 2002, 38(4):125-133. doi: 10.3321/j.issn:1001-7488.2002.04.021 [6] 杨兴明, 徐阳春, 黄启为, 等.有机(类)肥料与农业可持续发展和生态环境保护[J].土壤学报, 2008, 45(5):925-932. doi: 10.3321/j.issn:0564-3929.2008.05.019 [7] 杨承栋, 焦如珍, 孙启武, 等.细菌肥料促进马尾松生长效应的研究[J].林业科学研究, 2002, 15(3):361-363. doi: 10.3321/j.issn:1001-1498.2002.03.018 [8] 杨承栋, 余进, 焦如珍, 等.细菌肥料的研究与应用[J].世界林业研究, 2008, 21(6):41-44. [9] 康丽华.桉树与联合固氮菌相互作用的研究[J].微生物学通报, 2006, 29(4):14-18. [10] 吴凡, 催萍, 夏尚远, 等.桑树根际解磷细菌的分离鉴定及解磷能力的测定[J].蚕业科学, 2007, 33(4):521-526. doi: 10.3969/j.issn.0257-4799.2007.04.001 [11] 杨春华, 胡炳福, 朱秀娥, 等.不同细菌制剂对核桃苗促生效果的试验[J].贵州林业科技, 1998, 26(1):29-31. [12] 王守宗, 杨承栋, 谢应先, 等.细菌肥料对杨树生长效应的研究[J].林业科学研究, 1996, 9(6):654-657. doi: 10.3321/j.issn:1001-1498.1996.06.017 [13] 沈兴亮, 焦如珍.细菌肥料对油茶幼林生长的影响[J].林业科学研究, 2014, 27(4):570-574. [14] 焦燕, 赵江红, 徐柱.农牧交错带开垦年限对土壤理化特性的影响[J].生态环境学报, 2009, 18(5):1965-1970. doi: 10.3969/j.issn.1674-5906.2009.05.069 [15] 赵先丽, 周广胜, 吕国红.辽河三角洲不同植被类型土壤微生物特征研究[J].土壤通报, 2009, 40(6):1266-1269. [16] 薛立, 陈红跃, 邝立刚.湿地松混交林地土壤养分、微生物和酶活性的研究[J].应用生态学报, 2003, 14(1):157-159. doi: 10.3321/j.issn:1001-9332.2003.01.036 [17] 关松荫.土壤酶及其研究法[M].北京:农业出版社, 1986. [18] Classen A T, Boyle S I, Haskins K E.Community level physiological profiles of bacteria and fungi:plate type and incubation temperature influences on contrasting soils[J].FEMS Microbiol Ecol, 2010, 44(3):319-328. [19] Kong X, Wang C, Ji M.Analysis of microbial metabolic characteristics in mesophilic and thermophilic biofilters using Biolog plate technique[J].Chemical Engineering Journal, 2013, 230(16):415-421. [20] Rogers B, Tate Iii R.Temporal analysis of the soil microbial community along a toposequence in Pineland soils[J].Soil Biol Biochem, 2001, 33(10):1389-1401. doi: 10.1016/S0038-0717(01)00044-X [21] Pazj M D, Horra A M, Peuzzo L, et al. Soil quality:a new index based on microbiological and biochemical parameters[J].Biology and Fertility of Soils, 2002, 35(4):302-306. doi: 10.1007/s00374-002-0450-z [22] 刘善江, 夏雪, 陈桂梅, 等.土壤酶的研究进展[J].中国农学通报, 2011, 27(21):1-7. [23] 于镇华, 元野, 刘居东, 等.Biolog-Eco解析垦殖与自然恢复黑土微生物群落代谢功能季节变化[J].土壤与作物, 2013, 2(3):105-111. [24] 付学琴, 龙中儿, 魏赛金, 等.硅酸盐细菌肥料对水稻土壤微生物及肥力的影响[J].中国土壤与肥料, 2009(5):69-71. [25] 曾令涛, 王东升, 王祯祎, 等.蚯蚓堆肥与益生菌配施对土壤肥力及微生物特性的影响[J].土壤, 2016, 19(6):1100-1107. [26] 关松荫, 张德生, 张志明.土壤酶及其研究法[M].北京:农业出版社, 1986. [27] 邱权, 李吉跃, 王军辉, 等.西宁南山4种灌木根际和非根际土壤微生物、酶活性和养分特征[J].生态学报, 2014, 34(24):7411-7420. [28] 万忠梅, 吴景贵.土壤酶活性影响因子研究进展[J].西北农林科技大学学报, 2005, 23(6):87-92. doi: 10.3321/j.issn:1671-9387.2005.06.019 [29] 王旭辉, 丁亚欣, 谈俊.生物菌肥促生机制研究[J].现代农业科技, 2010(4):308-309. doi: 10.3969/j.issn.1007-5739.2010.04.200 [30] 吉牛拉惹, 崔涛, 史光祥, 等.生物菌肥对土壤肥力影响的研究初报[J].西昌学院学报:自然科学版, 2005, 19(4):25-26. [31] 孙双红, 陈立新, 李少博, 等.阔叶红松林不同演替阶段土壤酶活性与养分特征及其相关性[J].北京林业大学学报, 2016, 38(2):20-28. [32] 陈翔兰.生物菌肥的作用及推广应用前景[J].内蒙古农业科技, 2008(4):96. doi: 10.3969/j.issn.1007-0907.2008.04.047 -





 下载:
下载: