-
从生理机制上探讨植物与环境的关系是植物生理生态学的核心内容[1]。在气候变化的大背景下,通过改变植物的生长环境来对比植物生理性状的差异是目前植物生理生态的研究热点[2]。对于许多分布较广的植物而言,其生理及其他性状都有可能随地理纬度变化表现出适应性变异[3-4]。植物的光合生理性状可反映植物对光及CO2的利用特点,其中的叶绿素含量以及叶绿素荧光参数可以作为评价植物对环境的生长适应能力的主要生理指标[5-6]。种源试验不仅是研究植物地理变异(由环境与遗传因素主导)对植物性状作用机制的重要方法,也是预测在气候变化背景下物种分布范围变迁的重要研究手段[7-8]。
栓皮栎(Quercus variabilis Bl.)是东亚天然地理分布最广泛的树种之一,其分布区域包括中国大陆、台湾和海南岛、日本列岛以及朝鲜半岛。栓皮栎在我国分布可北至辽宁,南达广西、台湾等地,是我国暖温带、亚热带落叶阔叶林中具有代表性的树种之一[9-10],也是我国最重要的造林树种之一[11-12]。因而,栓皮栎被认为是在大区域尺度上研究植物对环境适应机理的理想树种之一[13-14]。
本研究选择栓皮栎天然分布的5个不同纬度的种源,并在其分布南界以南(广东鹤山,HS)进行田间栽培试验。通过测定不同种源栓皮栎幼苗的光合荧光参数,分析各种源南移后的光合和荧光生理特性及其对新生境下的适应性差异,为将来气候变化情景下栓皮栎的引种驯化以及理解植物对水平梯度(纬度)带来的环境差异的响应方式和适应策略提供科学参考。
-
2014年9—10月,选择我国5个不同纬度的栓皮栎天然成熟林分收集种子,分别为北京平谷(PG)、河南内乡(NX)、湖北秭归(ZG)、江西永修(YX)及湖南城步(CB)。2015年2月初,将种子播种于广东鹤山(HS)林科所苗圃(112°54′ E,22°41′ N,海拔56 m)。2015年5月,选择健康、大小均一的不同种源栓皮栎幼苗分别移植至广东鹤山试验地进行观察,随机排列各种源幼苗的栽植位置。常规管理,至第2年生长旺季(2016年7月)对每个种源随机选取10株幼苗,分别测量其地径、株高,随机选择3~4株健康植株作为重复,编号,选择每株幼苗中上部有代表性的健康、成熟的叶片进行光合生理指标的测定(包括叶绿素含量、光合及叶绿素荧光的测定)。另外,收集种源地临近气象台站的气象数据(1950—2000年),使用Kriging空间插值法(考虑海拔对温度的影响)进行拟合,根据其经纬度坐标提取所需气象数据(表 1)。
表 1 种源地及试验地地理位置与气候概况
Table 1. Geographical location and climate conditions of the provenance and cultivated sites
种源地/试验地
Sites纬度
NLatitude经度
ELongitude海拔/m
Elevation年均气温/℃
MAT年降水量/mm
MAP气候区
Climatic zone北京平谷 PG 40°16′ 117°07′ ~300 10.3 556 暖温带 河南内乡 NX 33°29′ 111°54′ ~900 10.9 851 暖温带 湖北秭归 ZG 30°46′ 110°20′ ~950 12.6 1 241 北亚热带 江西永修 YX 29°05′ 115°35′ ~820 15.8 1 290 中亚热带 湖南城步 CB 26°18′ 110°07′ ~1 050 13.2 1 540 中亚热带 广东鹤山 HS 22°41′ 112°54′ ~50 22.4 1 462 南亚热带 -
利用Li-6400便携式光合测定系统(LI-COR,USA)测定栓皮栎叶片的光响应曲线(参数统一设定):利用CO2注入系统(CO2小钢瓶)将参比室CO2浓度控制在400 μmol·mol-1;叶室温度控制在25~30℃;相对湿度控制在45%~65%,测定时光强从2 000 μmol·m-2·s-1开始,依次降为1 500、1 200、1 000、800、600、400、200、150、100、75、50、25、0 μmol·m-2·s-1。对各个种源幼苗,选择生长良好的3~4株,设定每个光强值数据采集时间为80 s,分别测定各种源栓皮栎的净光合速率等参数。于2016年7月下旬晴天的上午9:00—12:00在试验地实地测定。
-
光合作用CO2响应曲线使用Li-6400红蓝光源叶室测定,光强设定为1 200 μmol·m-2·s-1,通过光合仪CO2注入系统来控制CO2浓度,设定CO2浓度梯度为400、300、200、150、100、50、400、600、800、1 000、1 200 μmol·mol-1,不同CO2浓度设定数据采集时间为160 s,测定不同CO2浓度下各种源栓皮栎的光合参数。叶室温度控制、相对湿度控制、测定株和测定时间同上。
-
使用便携式叶绿素计(SPAD-502Plus,Konica Minolta Optics,Japan)测定不同种源栓皮栎叶片的相对叶绿素含量(SPAD)。在每个种源选取3~4株栓皮栎作为重复(与光合测定株一致),每株按照不同方向选定2片完好叶片并在每片叶子上选择5个点进行测定,后期数据处理取平均值。叶绿素荧光动力学参数采用超便携式调制叶绿素荧光仪MINI-PAM-II(WALZ,Germany)测定,测定时间与测定叶片同上。统计参数包括光系统II(PSII)原初光能转换效率(Fv/Fm)、光化学淬灭(qP)和非光化学淬灭(NPQ)等。
-
本文按非直角双曲线模型(下式)对光响应曲线[15]测定结果进行估算:
$ {P_n} = \frac{{\alpha \cdot PAR + {P_{{\rm{max}}}} - \sqrt {{{(\alpha \cdot PAR + {P_{{\rm{max}}}})}^2} - 4\theta \alpha \cdot PAR \cdot {P_{{\rm{max}}}}} }}{{2\theta }} - Rd $
式中:Pn为净光合速率;α为光响应曲线的初始斜率,也称为表观量子效率AQY;Pmax为最大净光合速率;PAR为光合有效辐射;Rd为暗呼吸速率。光饱和点(LSP)和光补偿点(LCP)利用弱光(PAR≤200 μmol·m-2·s-1)条件下,Pn与PAR构建线性方程所得,其公式为:
$ {P_n} = m \times PAR + n $
$ LCP = - n/m $
$ LSP=(P\text{max}-n)/m $
式中:参数m和n为拟合直线的斜率和截距[16]。
FvCB光合模型拟合CO2响应曲线(Pn-Ci)参考Duursma[17]和Gu等[18]方法,并根据此模型的分段性分别拟合Rubisco酶最大羧化速率(Vcmax)、最大电子传递速率(Jmax)和光下线粒体呼吸速率(Rp)等参数。在低CO2浓度(≤300 μmol·mol-1)下, 构建Pn与胞间CO2浓度(Ci)线性拟合方程,根据此曲线与X轴的截距求得CO2补偿点(CCP)[19]。
使用R软件(version 3.4.3) (R Core Team, 2017, https://www.r-project.org/)对上述5个种源进行光合曲线拟合,并对各统计参数进行方差分析(ANOVA)和Duncan多重比较,以检验数据之间的差异显著性(a=0.05)。制图应用R软件和Origin2018完成。
-
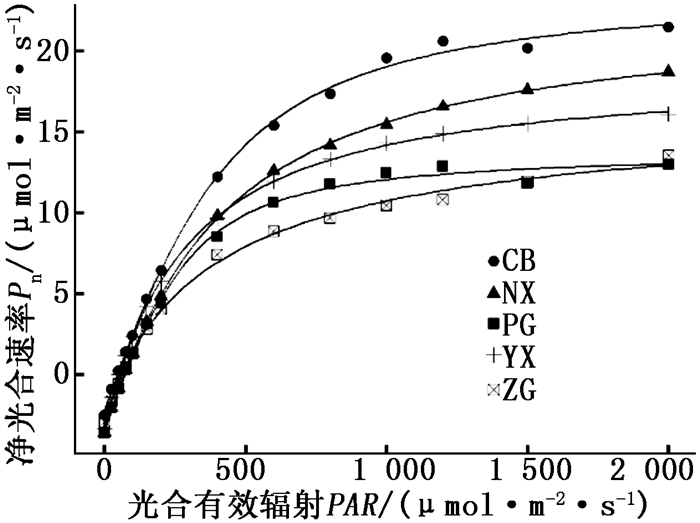
图 1表明:在低光合有效辐射范围内(PAR<450 μmol·m-2·s-1),不同生境下各种源栓皮栎叶片的Pn对光照强度的响应均较敏感,即随着PAR的增加,Pn也随之迅速增加,且各个种源的增长趋势基本一致;当PAR>450 μmol·m-2·s-1之后,各种源栓皮栎在同一PAR下的Pn值大小顺序为CB>NX>YX>PG>ZG,其净光合速率缓慢地逐渐增加,没表现出明显的光饱和现象, 其中,PG种源的净光合速率随光强的增加表现出相对平缓的趋势。
图 1 不同种源栓皮栎叶片的光响应曲线
Figure 1. Light response curve of Q. variabilis leaves among different provenances
光响应曲线参数拟合结果(表 2)表明:YX种源栓皮栎的表观量子效率最高,显著高于ZG种源,而与其它3个种源差异不显著。CB种源的最大净光合速率(Pmax)显著高于PG种源和ZG种源,而NX种源和YX种源的Pmax与上述3个种源差异不显著。不同种源间的暗呼吸速率、光饱和点和光补偿点的差异不显著(P>0.05),但暗呼吸速率和光补偿点有随高纬度(北方)种源向低纬度(南方)种源逐级递减的大致趋势,而低纬度种源CB的光饱和点最高。
表 2 不同种源栓皮栎叶片的光响应拟合参数
Table 2. Fitted photosynthetic parameters of Q. variabilis leaves among various provenances
指标 Parameters 北京平谷 PG 河南内乡 NX 湖北秭归 ZG 江西永修 YX 湖南城步 CB AQY/(μmol·μmol-1) 0.059±0.003ab 0.057±0.002ab 0.045±0.009b 0.069±0.002a 0.055±0.009ab Pmax/(μmol·m-2·s-1) 19.938±0.787b 25.934±4.035ab 17.716±0.347b 22.089±3.255ab 29.653±4.446a Rd/(μmol·m-2·s-1) 3.536±0.732a 3.535±0.223a 2.659±0.298a 3.179±1.439a 2.410±0.448a LSP/(μmol·m-2·s-1) 582.124±64.83a 697.669±91.75a 591.42±105.571a 563.932±149.35a 718.241±62.139a LCP/(μmol·m-2·s-1) 78.145±24.571a 74.99±5.329a 71.474±23.884a 59.17±36.011a 47.701±4.328a 注 Notes:AQY:表观量子效率 Apparent quantum yield;Pmax:最大净光合速率 Maximum net photosynthetic rate;Rd:暗呼吸速率 Dark respiration rate;LSP:光饱和点 Light saturation point;LCP:光补偿点 Light compensation point。数据为平均值±标准偏差,同一行数值带有不同小写字母表示在0.05水平上差异显著(P<0.05);下同 -
采用FvCB模型模拟的5个栓皮栎种源叶片净光合速率对CO2响应的拟合曲线(Pn-Ci)(图 2)表明:在1 200 μmol·m-2·s-1光强下,各种源Pn均随胞间CO2浓度(Ci)的增加而增加,最后逐渐平缓并达到饱和。FvCB模型模拟的Pn-Ci曲线与光响应曲线不同,具有明显的分段性。虚线之前为第一阶段,细线为CO2限制阶段的净光合速率(Ac);虚线之后为第二阶段,细线为最大电子传递速率(Jmax)限制阶段的净光合速率(Aj)。粗线代表 2个阶段的限制速率。第一阶段的Pn随Ci的增加而呈线性增加,此时光合作用受Rubisco酶活性大小的限制;第二阶段的Pn随Ci的增加呈逐渐平缓的曲线增加,此时光合作用受RuBP再生速率大小的限制。虚线处Ci值则为这2个限制阶段的临界胞间CO2浓度(Ac_Aj)。
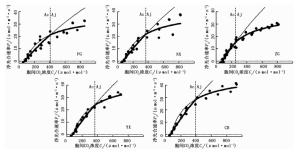
图 2 不同种源栓皮栎叶片的CO2响应曲线(Pn-Ci)
Figure 2. Photosynthesis CO2 response curves(Pn-Ci) of Q. variabilis leaves among various provenances
从表 3看出:栓皮栎幼苗的Rubisco酶最大羧化速率(Vcmax)随纬度的升高而逐渐降低(CB>YX>ZG>NX>PG),但各种源间差异不显著(P>0.05),这表明不同种源栓皮栎叶片叶肉细胞Rubisco酶的羧化能力相差不大。另外,最大电子传递速率(Jmax)、光呼吸速率(Rp)、Ac_Aj和CO2补偿点(CCP)在不同种源间的差异均不显著,但ZG种源的Ac_Aj明显低于其他4个种源。
表 3 不同种源栓皮栎叶片CO2响应的拟合参数
Table 3. Fitted parameters from Pn-Ci curves of Q. variabilis leaves among various provenances
指标 Parameters 北京平谷 PG 河南内乡 NX 湖北秭归 ZG 江西永修 YX 湖南城步 CB Vcmax/(μmol·m-2·s-1) 39.87±17.10a 43.15±11.33a 48.96±12.72a 49.60±0.20a 58.01±6.10a Jmax/(μmol·m-2·s-1) 173.29±2.15a 190.95±77.41a 226.59±58.08a 221.37±31.11a 212.86±14.71a Rp/(μmol·m-2·s-1) 1.170±0.360a 1.020±0.080a 1.140±0.410a 1.140±0.490a 1.130±0.060a Ac_Aj/(μmol·mol-1) 434.46±200.64a 404.17±17.73a 290.06±74.50a 371.95±20.97a 374.47±57.64a CCP/(μmol·mol-1) 72.922±12.905a 66.343±4.467a 74.541±11.537a 74.110±1.774a 65.557±4.513a 注 Notes: Vcmax:Rubisco 酶最大羧化速率 Rubisco enzyme maximum carboxylation rate;Jmax:最大电子传递速率 Maximum electron transport rate;Rp:线粒体在光照下的呼吸速率 Respiration rate of mitochondria under light;Ac_Aj:Rubico 酶限制阶段与 RuBP 限制阶段临界点的胞间CO2浓度 Intercellular CO2 concentration of the transition poin tbetween Rubisco carboxylation-limited and RuBP regeneration-limited state;CCP:CO2补偿点 CO2 compensation point. -
通过对5个种源栓皮栎的叶绿素荧光参数进行统计分析,结果(表 4)表明:光系统Ⅱ(PSⅡ)原初光能转换效率(Fv/Fm)、PSⅡ潜在活性(Fv/F0)和PSⅡ实际光化学反应效率ΦPSⅡ参数在不同种源间差异不显著(P>0.05),且不同种源栓皮栎在非光化学猝灭系数(NPQ)、光化学猝灭系数(qP)和相对电子传递速率(ETR)参数上差异也较小(P>0.05)。叶绿素相对含量(SPAD值)方面,NX种源和CB种源显著高于YX种源(P<0.05),而与其他2个种源的SPAD值差异不显著。表 4还表明:不同种源株高、地径之间差异不显著,但PG种源的地径、株高较大,生长较快。
表 4 不同种源栓皮栎幼苗叶绿素含量及荧光参数
Table 4. Chlorophyll content and chlorophyll fluorescence parameters of Q.variabilis seedlings among different provenances
指标 Parameters 北京平谷 PG 河南内乡 NX 湖北秭归 ZG 江西永修 YX 湖南城步 CB D(mm) 13.50±0.890a 10.77±3.745a 11.61±3.337a 12.25±2.865a 12.51±2.094a H(cm) 112.0±42.48a 80.00±14.54a 77.75±20.19a 90.00±26.24a 93.25±23.37a SPAD 48.00±2.50ab 50.73±4.84a 47.56±1.75ab 44.25±2.28b 49.05±2.76a ΦPSⅡ 0.228±0.034a 0.221±0.027a 0.228±0.018a 0.227±0.026a 0.223±0.009a ETR 78.25±11.85a 76.20±9.18a 78.45±6.17a 78.08±8.95a 76.60±3.09a qP 0.437±0.040a 0.410±0.070a 0.423±0.047a 0.416±0.045a 0.420±0.017a NPQ 2.738±0.519a 2.347±0.521a 2.583±0.364a 2.595±0.364a 2.642±0.165a Fv/Fm 0.800±0.029a 0.797±0.038a 0.807±0.033a 0.810±0.031a 0.805±0.007a Fv/F0 4.071±0.727a 4.057±0.948a 4.276±0.833a 4.365±0.771a 4.133±0.188a 注 Notes: D:地径 Basal diameter;H:高度 Height; SPAD 值:相对叶绿素含量;ΦPSⅡ:PSⅡ 实际光化学反应效率 Effective quantum yield of photosystem Ⅱ photochemistry;ETR:相对电子传递速率 Rel. electron transport rate;qP:光化学猝灭 Photochemical quenching;NPQ:非光化学猝灭 Non-photochemical quenching;Fv/Fm:PSⅡ原初光能转换效率 Primary conversion of light energy of photosystem Ⅱ;Fv/F0:PSⅡ潜在活性 Potential activation ofphotosystem Ⅱ;重复4次。 -
本研究发现,5个栓皮栎种源中, 低纬度湖南城步种源的最大净光合速率(Pmax)最高,可认为南方种源的光合潜能较北方种源更高,这与刘建锋等[13]和王小菲等[5]对不同纬度栓皮栎实生苗的实地研究结果一致。通常认为, 植物在适宜的生长条件下的表观量子效率(AQY)为0.03~0.05 μmol·μmol-1[20]。本研究发现, 各种源栓皮栎幼苗的AQY为0.04~0.07 μmol·μmol-1,与上述范围基本一致或略高,并与李理渊等[21]在黄河小浪底森林生态站所测定栓皮栎在不同光环境下的AQY相似。PSⅡ原初光能转换效率(Fv/Fm)一般在不受光抑制的条件下变化极小,且此参数不受物种和生长条件的影响[22],范围为0.750.85[23],本研究各种源的Fv/Fm均处于此范围。结合上述AQY值,说明本研究涉及的不同种源栓皮栎在过饱和水热条件(相较于种源地)的生境下依然能够正常生长。本研究结果显示,各种源间ΦPSⅡ、非光化学淬灭(NPQ)和光化学猝灭系数(qP)差异不显著,表明各种源的栓皮栎幼苗PSⅡ光能捕获效率、PSⅡ电子传递活性(光合活性)、热耗散和光保护能力相当。
FvCB模型模拟的各种源Pn-Ci曲线均表现出分段性的特征。从图 2可看出,叶片光合作用受到CO2限制[24]和RuBP再生速率的限制[25]后,并没有出现磷酸丙糖利用率(TPU)转运速率限制阶段,这可能与本研究未设置较高CO2浓度有关。如梁星云等[26]对长白山白桦(Betula platyphylla Suk.)的A-Ci曲线进行拟合,胞间CO2浓度(Ci)在>1 000 μmol·mol-1时才会出现TPU转运速率限制;夏国威等[27]在设置高CO2浓度(2 000 μmol·mol-1)的试验中也出现了TPU参数。在FvCB模型模拟的CO2响应的拟合参数中,不同种源间Rubisco酶最大羧化速率(Vcmax)和最大电子传递速率(Jmax)差异不显著,这反映了种源间植物叶片叶肉细胞Rubisco酶的含量及羧化能力和光合电子传递能力都可能相差不大[28]。
叶绿素是主要的吸收光能物质, 直接影响植物光合作用的光能利用[29]。本研究表明,河南内乡和湖南城步种源的相对叶绿素含量(SPAD值)显著高于江西永修种源,说明前二者的捕光能力更强。除上述提到的生理参数外,不同种源栓皮栎幼苗的Rd、LSP、LCP、Rp、CCP和ETR等参数在广东鹤山这一相同生境下差异不显著,说明相对于自身遗传特性,这些参数的环境可塑性较强。从结果看,尽管不同种源栓皮栎在某些光合指标上表现出差异,但在大多数光合生理指标和生长特性上差异不显著,这从侧面反映了栓皮栎适应能力强和分布范围广的树种特性。华南地区的湿热环境条件没有超出栓皮栎的适应范围,然而,竞争是否构成其向南扩散的限制因子尚待进一步研究。
-
尽管不同栓皮栎种源的纬度差异较大,但各种源栓皮栎均对南方气候的适应能力较强,在生理指标上并未出现受高温等胁迫状况,且其光合和叶绿素荧光在内的大多数光合生理参数差异不显著。综上所述,可以初步得出栓皮栎在水热条件过饱和的新生境下有较强的环境适应能力,且适应迅速,光合生理性状最终趋于一致。
南移后不同种源栓皮栎幼苗光合生理性状的比较
Comparison of Photosynthetic Physiological Traits of Quercus variabilis Seedlings among Various Provenances after Southward Movement
-
摘要:
目的 探讨水热条件变化后不同种源栓皮栎幼苗光合生理性状的差异,为栓皮栎优良种源的引种栽培提供理论参考。 方法 收集5个地理种源(北京平谷PG、河南内乡NX、湖北秭归ZG、江西永修YX和湖南城步CB)的栓皮栎种子,选择在其自然分布南缘以南的生境(广东鹤山,HS)下进行培育,测定不同种源栓皮栎的光合生理指标。 结果 表明:低纬度CB种源栓皮栎的潜在最大净光合速率(Pmax)显著高于中高纬的ZG和PG种源(P < 0.05);YX种源的表观量子效率(AQY)最高,而ZG种源的最低;NX和CB种源的叶绿素相对含量(SPAD)显著高于YX种源。PSⅡ原初光能转换效率(Fv/Fm)和PSⅡ潜在活性(Fv/F0)在各种源间均差异不显著,表明各种源栓皮栎均能较好地适应水热丰沛的新生境。同时,各种源栓皮栎在暗呼吸速率(Rd)、光饱和点(LSP)、光补偿点(LCP)、Rubisco酶最大羧化速率(Vcmax)、最大电子传递速率(Jmax)、光呼吸速率(Rp)、生长参数以及叶绿素荧光参数如电子传递速率(ETR)、光化学淬灭系数(qP)和非光化学淬灭系数(NPQ)等均差异不显著。 结论 各种源栓皮栎光合生理性状的异同与其自身遗传因素和较强的生态适应性有关。 Abstract:Objective To explore the differences in photosynthetic physiological traits among Quercus variabilis provenances responding to alternative habitat, and to provide reference for introduction and cultivation of excellent germplasm of Q. variabilis. Method Five Q. variabilis provenances coming from Pinggu of Beijing, Neixiang of He'nan Province, Zigui of Hubei Province, Yongxiu of Jiangxi Province and Chengbu of Hu'nan Province, were collected and cultured in the region beyond the species' southmost range (Heshan of Guangdong Province) to determine the photosynthetic physiological indices of different provenances. Result The potential maximum net photosynthetic rate of Chengbu provenance was significantly higher than the provenances at mid-high latitudes (Zigui and Pinggu) (P < 0.05). Yongxiu provenance showed higher apparent quantum efficiency, while Zigui provenance showed the lowest. The relative chlorophyll content of Neixiang and Chengbu provenances was significantly higher than that of Yongxiu provenance. Primary light energy conversion efficiency of PSII (Fv/Fm) and potential activity of PSII (Fv/F0) differed slightly among provenances, indicating that all these Q. variabilis provenances did not sustain obvious stresses and could adapt to the new habitat. Moreover, dark respiration rate, light saturation point, light compensation point, Rubisco enzyme maximum carboxylation rate, maximum electron transfer rate, photorespiration rate, as well as growth parameters and chlorophyll fluorescence parameters such as electron transfer rate, photochemistry quenching coefficient and non-photochemistry quenching coefficient were comparable. Conclusion The similarities and differences of photosynthetic physiological traits of Q. variabilis from different provenances are related to their own genetic factors and strong environmental adaptability to new habitat. -
表 1 种源地及试验地地理位置与气候概况
Table 1. Geographical location and climate conditions of the provenance and cultivated sites
种源地/试验地
Sites纬度
NLatitude经度
ELongitude海拔/m
Elevation年均气温/℃
MAT年降水量/mm
MAP气候区
Climatic zone北京平谷 PG 40°16′ 117°07′ ~300 10.3 556 暖温带 河南内乡 NX 33°29′ 111°54′ ~900 10.9 851 暖温带 湖北秭归 ZG 30°46′ 110°20′ ~950 12.6 1 241 北亚热带 江西永修 YX 29°05′ 115°35′ ~820 15.8 1 290 中亚热带 湖南城步 CB 26°18′ 110°07′ ~1 050 13.2 1 540 中亚热带 广东鹤山 HS 22°41′ 112°54′ ~50 22.4 1 462 南亚热带 表 2 不同种源栓皮栎叶片的光响应拟合参数
Table 2. Fitted photosynthetic parameters of Q. variabilis leaves among various provenances
指标 Parameters 北京平谷 PG 河南内乡 NX 湖北秭归 ZG 江西永修 YX 湖南城步 CB AQY/(μmol·μmol-1) 0.059±0.003ab 0.057±0.002ab 0.045±0.009b 0.069±0.002a 0.055±0.009ab Pmax/(μmol·m-2·s-1) 19.938±0.787b 25.934±4.035ab 17.716±0.347b 22.089±3.255ab 29.653±4.446a Rd/(μmol·m-2·s-1) 3.536±0.732a 3.535±0.223a 2.659±0.298a 3.179±1.439a 2.410±0.448a LSP/(μmol·m-2·s-1) 582.124±64.83a 697.669±91.75a 591.42±105.571a 563.932±149.35a 718.241±62.139a LCP/(μmol·m-2·s-1) 78.145±24.571a 74.99±5.329a 71.474±23.884a 59.17±36.011a 47.701±4.328a 注 Notes:AQY:表观量子效率 Apparent quantum yield;Pmax:最大净光合速率 Maximum net photosynthetic rate;Rd:暗呼吸速率 Dark respiration rate;LSP:光饱和点 Light saturation point;LCP:光补偿点 Light compensation point。数据为平均值±标准偏差,同一行数值带有不同小写字母表示在0.05水平上差异显著(P<0.05);下同 表 3 不同种源栓皮栎叶片CO2响应的拟合参数
Table 3. Fitted parameters from Pn-Ci curves of Q. variabilis leaves among various provenances
指标 Parameters 北京平谷 PG 河南内乡 NX 湖北秭归 ZG 江西永修 YX 湖南城步 CB Vcmax/(μmol·m-2·s-1) 39.87±17.10a 43.15±11.33a 48.96±12.72a 49.60±0.20a 58.01±6.10a Jmax/(μmol·m-2·s-1) 173.29±2.15a 190.95±77.41a 226.59±58.08a 221.37±31.11a 212.86±14.71a Rp/(μmol·m-2·s-1) 1.170±0.360a 1.020±0.080a 1.140±0.410a 1.140±0.490a 1.130±0.060a Ac_Aj/(μmol·mol-1) 434.46±200.64a 404.17±17.73a 290.06±74.50a 371.95±20.97a 374.47±57.64a CCP/(μmol·mol-1) 72.922±12.905a 66.343±4.467a 74.541±11.537a 74.110±1.774a 65.557±4.513a 注 Notes: Vcmax:Rubisco 酶最大羧化速率 Rubisco enzyme maximum carboxylation rate;Jmax:最大电子传递速率 Maximum electron transport rate;Rp:线粒体在光照下的呼吸速率 Respiration rate of mitochondria under light;Ac_Aj:Rubico 酶限制阶段与 RuBP 限制阶段临界点的胞间CO2浓度 Intercellular CO2 concentration of the transition poin tbetween Rubisco carboxylation-limited and RuBP regeneration-limited state;CCP:CO2补偿点 CO2 compensation point. 表 4 不同种源栓皮栎幼苗叶绿素含量及荧光参数
Table 4. Chlorophyll content and chlorophyll fluorescence parameters of Q.variabilis seedlings among different provenances
指标 Parameters 北京平谷 PG 河南内乡 NX 湖北秭归 ZG 江西永修 YX 湖南城步 CB D(mm) 13.50±0.890a 10.77±3.745a 11.61±3.337a 12.25±2.865a 12.51±2.094a H(cm) 112.0±42.48a 80.00±14.54a 77.75±20.19a 90.00±26.24a 93.25±23.37a SPAD 48.00±2.50ab 50.73±4.84a 47.56±1.75ab 44.25±2.28b 49.05±2.76a ΦPSⅡ 0.228±0.034a 0.221±0.027a 0.228±0.018a 0.227±0.026a 0.223±0.009a ETR 78.25±11.85a 76.20±9.18a 78.45±6.17a 78.08±8.95a 76.60±3.09a qP 0.437±0.040a 0.410±0.070a 0.423±0.047a 0.416±0.045a 0.420±0.017a NPQ 2.738±0.519a 2.347±0.521a 2.583±0.364a 2.595±0.364a 2.642±0.165a Fv/Fm 0.800±0.029a 0.797±0.038a 0.807±0.033a 0.810±0.031a 0.805±0.007a Fv/F0 4.071±0.727a 4.057±0.948a 4.276±0.833a 4.365±0.771a 4.133±0.188a 注 Notes: D:地径 Basal diameter;H:高度 Height; SPAD 值:相对叶绿素含量;ΦPSⅡ:PSⅡ 实际光化学反应效率 Effective quantum yield of photosystem Ⅱ photochemistry;ETR:相对电子传递速率 Rel. electron transport rate;qP:光化学猝灭 Photochemical quenching;NPQ:非光化学猝灭 Non-photochemical quenching;Fv/Fm:PSⅡ原初光能转换效率 Primary conversion of light energy of photosystem Ⅱ;Fv/F0:PSⅡ潜在活性 Potential activation ofphotosystem Ⅱ;重复4次。 -
[1] 蒋高明.当前植物生理生态学研究的几个热点问题[J].植物生态学报, 2001, 25(5):514-519. doi: 10.3321/j.issn:1005-264X.2001.05.002 [2] 周驿之, 程艳霞, 樊莹, 等.长白山不同海拔白桦幼苗移栽至同一生境的光合及反射光谱特性[J].生态学报, 2018, 38(14):5109-5119. [3] Chapin F S, Chapin M C. Ecotypic differentiation of growth processes in Carex aquatilis along latitudinal and local gradients[J]. Ecology, 1981, 62(4):1000-1009. doi: 10.2307/1936999 [4] Maron J L, Vila M, Bommarco R, et al. Rapid evolution of an invasive plant[J]. Ecological Monographs, 2004, 74(2):261-280. doi: 10.1890/03-4027 [5] 王小菲, 高文强, 刘建锋, 等.不同生境对栓皮栎幼苗光合生理特性的影响[J].生态学报, 2016, 36(24):8062-8070. [6] 王建华, 任士福, 史宝胜, 等.遮荫对连翘光合特性和叶绿素荧光参数的影响[J].生态学报, 2011, 31(7):1811-1817. [7] Ågren J, Schemske D W. Reciprocal transplants demonstrate strong adaptive differentiation of the model organism Arabidopsis thaliana in its native range[J]. New Phytologist, 2012, 194(4):1112-1122. doi: 10.1111/j.1469-8137.2012.04112.x [8] Mclean E H, Prober S M, Stock W D, et al. Plasticity of functional traits varies clinally along a rainfall gradient in Eucalyptus tricarpa[J]. Plant Cell & Environment, 2014, 37(6):1440-1451. [9] Fang J, Wang Z, Tang Z. Atlas of woody plants in china:distribution and climate[M]. Berlin:Springer Berlin Heidelberg, 2011:190. [10] 高文强.不同地理梯度上栓皮栎种群动态及其环境解释[D].北京: 中国林业科学研究院, 2017. [11] 孙巧玉, 刘勇.控释肥和灌溉方式对栓皮栎容器苗苗木质量及造林效果的影响[J].林业科学研究, 2018, 31(5):140-147. [12] 王新民, 陆元昌, 宁金魁, 等.北京地区不同起源栓皮栎早期生长过程研究[J].林业科学研究, 2009, 22(6):860-864. doi: 10.3321/j.issn:1001-1498.2009.06.020 [13] 刘建锋, 肖文发, 熊定鹏, 等.不同纬度栓皮栎幼苗生理生态特征的比较[J].植物研究, 2011, 31(4):467-471. [14] 倪妍妍, 胡军, 刘建锋, 等.不同地理种源栓皮栎幼苗生长与物质分配的变化趋势[J].西北植物学报, 2017, 37(3):534-540. [15] Thornley J H M. Mathematical models in plant physiology[M]. London:Academic Press, 1976. [16] 刘建锋, 杨文娟, 史胜青, 等.崖柏与侧柏光合特性和叶绿素荧光参数的比较研究[J].西北植物学报, 2011, 31(10):2071-2077. [17] Duursma R A. Plantecophys-an R package for analysing and modelling leaf gas exchange data[J]. PLoS ONE, 2015, 10(11):e0143346. doi: 10.1371/journal.pone.0143346 [18] Gu L, Pallardy S G, Tu K, et al. Reliable estimation of biochemical parameters from C3 leaf photosynthesis-intercellular carbon dioxide response curves[J]. Plant Cell & Environment, 2010, 33(11):1852-1874. [19] 张昆, 万勇善, 刘风珍, 等.花生幼苗光合特性对弱光的响应[J].应用生态学报, 2009, 20(12):2989-2995. [20] Sharp R E, Matthews M A, Boyer J S. Kok effect and the quantum yield of photosynthesis light partially inhibits dark respiration[J]. Plant Physiology, 1984, 75(1):95-101. doi: 10.1104/pp.75.1.95 [21] 李理渊, 李俊, 同小娟, 等.不同光环境下栓皮栎和刺槐叶片光合光响应模拟[J].应用生态学报, 2018, 29(7):2295-2306. [22] Heraud P, Beardall J. Changes in chlorophyll fluorescence during exposure of Dunaliella tertiolecta to UV radiation indicate a dynamic interaction between damage and repair processes[J]. Photosynthesis Research, 2000, 63(2):123-134. doi: 10.1023/A:1006319802047 [23] 何炎红, 郭连生, 田有亮.白刺叶不同水分状况下光合速率及其叶绿素荧光特性的研究[J].西北植物学报, 2005, 25(11):2226-2233. doi: 10.3321/j.issn:1000-4025.2005.11.016 [24] Wullschleger S D. Biochemical limitations to carbon assimilation in C3 plants-a retrospective analysis of the A/Ci curves from 109 species[J]. Journal of Experimental Botany, 1993, 44(262):907-920. [25] Long S P, Bernacchi C J. Gas exchange measurements, what can they tell us about the underlying limitations to photosynthesis? Procedures and sources of error[J]. Journal of Experimental Botany, 2003, 54(392):2393-2401. doi: 10.1093/jxb/erg262 [26] 梁星云, 刘世荣. FvCB生物化学光合模型及A-Ci曲线测定[J].植物生态学报, 2017, 41(6):693-706. [27] 夏国威, 陈东升, 孙晓梅, 等.日本落叶松冠层光合生理参数的空间异质性研究[J].林业科学研究, 2018, 31(6):133-140. [28] 唐星林, 周本智, 周燕, 等.基于FvCB模型的几种草本和木本植物光合生理生化特性[J].应用生态学报, 2017, 28(5):1482-1488. [29] Maxwell K, Johnson G N. Chlorophyll fluorescence-a practical guide[J]. Journal of Experimental Botany, 2000, 51(345):659-668. doi: 10.1093/jexbot/51.345.659 -




 下载:
下载: