-
竹类是热带和亚热带森林植被的重要组成部分,集生态、社会和经济效益于一身,在生态环境保护和协调区域经济发展中发挥着不可替代的作用[1]。竹子在整个生长过程中,往往会遭受各种环境胁迫,而产生生理可塑性、形态可塑性[2]等。其中,生理可塑性包括水分亏缺的影响,其制约着植物的生长发育[3]。因此,开展竹子干旱胁迫环境下的研究对了解其逆境生理生态响应具有重要的意义。叶绿素色素是光合系统构建最直接的体现,同时也是反映植株光合能力强弱的重要指标[4]。在干旱胁迫下,水稻(Oryza sativa L.)[5]、小麦(Triticum aestivum Linn.)[6]和毛竹(Phyllostachys edulis (Carrière) J. Houz.)[7]等植物光合速率及叶绿素含量都会显著下降,干旱严重时甚至会对叶绿体结构造成破坏。同时,根系作为植物地下部分唯一的营养器官,其新陈代谢活动的强弱能够反映植株根系对于矿质营养和水分的吸收能力,体现根系生长和环境变化之间的动态关系[8]。而在干旱胁迫下,最直接的受害部位就是植物根系[9]。此外,抗氧化保护机制也是植物生理可塑性抗性的一个重要组成部分,保护酶和丙二醛(MDA)能够通过削弱过强的氧化作用所产生的活性氧积累对细胞膜造成的伤害,从而保证其它相关生理活动的有序进行,使得植物能够适应逆境生存。有关植物在干旱胁迫下保护酶及丙二醛含量变化的研究相当多,其对于探究植物逆境生理意义重大[10]。目前,我国干旱、半干旱地区的水资源利用矛盾日益突出,同时,在育苗生产中节水灌溉对高效生产也十分重要,因此,深入了解干旱胁迫下植物的伤害机理和植物细胞对干旱胁迫的响应机制,对培养具有优良抗旱性的种质资源具有重要意义。
绿竹(Dendrocalamopsis oldhami (Munro) Keng f.)隶属禾本科(Gramineae)竹亚科(Bambusoideae)绿竹属(Dendrocalamopsis (Chia et H. L. Fung) Keng f.),其笋形似马蹄又名“马蹄笋”,是绿竹属中经济价值较高的丛生竹种,具有笋期长、易栽培、笋味鲜脆等特点,在福建、浙江、广西、云南、广东等省区广泛栽培,在重庆、四川等地部分引种[11]。绿竹对环境胁迫的生理响应研究,如盐碱[12]、低温胁迫[13]有见报道,但关于绿竹苗期水分胁迫,特别是绿竹组培苗对水分胁迫及其复水后生理响应特性的研究尚未见报道。相关研究显示,对玉米(Zea mays Linn.)[14]、蓝莓(Vaccinium spp.)[15]、鼓节竹(Bambusa tuldoides Munro cv. Swolleninternode N. H. Xia)[16]、铺地竹(Sasa argenteistriatus E. G. Camus)等植物[17]进行干旱处理后,在一定干旱时间内,植物的保护酶活力会随着水分胁迫程度增大而先增加后降低,而叶片光合色素含量随着干旱的进行持续降低。基于以上研究结果,本研究分析了水分胁迫及其复水后绿竹根系活力、抗氧化酶系统、膜脂过氧化与叶片光合色素含量的变化规律,以期为绿竹规模化育苗栽培制订适宜的经营管理措施以及节水灌溉技术方案提供理论依据。
HTML
-
试验选择在福建省永安林业(集团)股份有限公司的遮荫大棚内进行盆栽苗培育,大棚面积约667 m2,满足育苗需求。该公司位于福建省永安市境内(117°22′~117°23′ N,25°57′~25°58′ E),四季分明,冬春季降水较少,夏季炎热,属典型亚热带季风山地气候。海拔高度约201 m,年平均降水量为1 600 mm,年平均气温约为19.3℃,土壤类型以红壤类为主。
-
试验材料为经外殖体诱导无菌环境下培养获得的同一批生长一致的绿竹组培苗,苗高65~80 cm,地径5~7 mm。
-
采用规格为直径25 cm的塑料袋盆栽苗控水方式,盆土为泥炭:谷壳=7:3,经混合均匀后施加一定量的有机肥(66.66 g·kg-1),每盆装干土3.00 kg,测得田间持水量为72.8%。试验共设5个水分处理:正常对照(CK)、中度干旱胁迫(MS)、重度干旱胁迫(SS)、中度干旱胁迫后复水(MS-CK)和重度干旱胁迫后复水(SS-CK)。其中,对照CK的土壤含水量控制在田间持水量的75%以上,中度干旱胁迫处理的土壤含水量控制在田间持水量的50%~55%,重度干旱胁迫处理的土壤含水量控制在田间持水量的30%~35%。试验通过减少浇水对正常供水苗进行逐步失水达到水分胁迫,经2 d达到中度干旱,失水3 d达到重度干旱要求,于苗期(7月23日)开始水分胁迫处理,8月22日结束干旱后,分别对中度干旱处理和重度干旱处理复水至正常水分。每个处理3次重复。复水7 d后(8月29日)开始对干旱处理和复水处理取样并测定各项生理指标。试验棚内地面铺设双层塑料布,以防止根系下扎和毛孔作用从地面吸水,于每日18:00称量并补充损耗水分,经叶片相对含水量测定,发现叶片水分状况与土壤相对含水量一致[18]。试验期间有降雨时大棚覆盖塑料布,两侧距地面20 cm留通风口,保证雨水不会进入以影响试验结果。同时,天气晴朗时去除遮荫,保证试验在自然环境下进行。
-
土壤含水量测量采用称质量法,电子天平量感为1 g。将盆内带有根团土的绿竹整丛取出放入带冰块的采样箱内,保鲜带回试验室,将根部放入水池中浸泡至土壤松散,洗净根系并擦干水分,获得完整植株,从茎基部剪断,分离地上地下部分以备用。
叶绿素(Chl)和类胡萝卜素(Car)采用丙酮与乙醇(1:1)混合法避光提取24 h后用紫外可见分光光度计(UV-1800PC,上海美普达仪器有限公司)测定。
酶液的提取:分别将各处理叶片混匀并取新鲜成熟叶片0.2 g于液氮预冷的研钵中,加入5 mL预冷的50 mmol·L-1磷酸缓冲液(pH=7.8)冰浴研磨,然后用磷酸缓冲液定容至10 mL。并于4℃下10 500 r·min-1离心15 min,取上清液于4℃下保存。超氧化物歧化酶(SOD)活性用氮蓝四唑(NBT)光化还原法测定,以每单位时间内抑制NBT光化还原50%为1个酶活性单位U;过氧化物酶(POD)用愈创木酚氧化法测定,以每分钟OD470升高0.01为1个酶活性单位U;过氧化氢酶(CAT)用紫外吸收法测定,以每分钟OD240减少0.01为1个酶活性单位U;丙二醛(MDA)含量用硫代巴比妥酸法测定;根系活力采用α-萘胺法测定。
-
使用Excel 2013软件对数据进行分析与作图,并用SPSS 19.0软件对各项生理指标进行方差分析和LSD多重对比,所有试验数据均采用均值±标准差展示。
1.1. 试验地概况
1.2. 供试材料
1.3. 试验方法
1.4. 指标测定
1.5. 数据分析
-
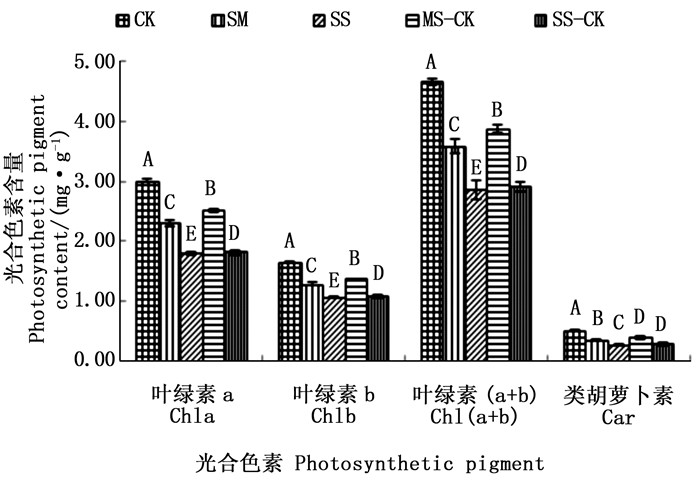
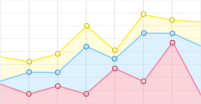
由图 1可以看出,在干旱胁迫下,绿竹叶片叶绿素a、叶绿素b、类胡萝卜素和叶绿素(a+b)含量均随着水分胁迫加重而降低。与对照(CK)相比,中度干旱胁迫(MS)和重度干旱胁迫(SS)的叶绿素a含量分别降低了23.59%和40.20%,中度干旱胁迫后复水(MS-CK)、重度干旱胁迫后复水(SS-CK)叶绿素a含量分别升高9.13%、1.22%,处理间叶绿素a含量均达到差异显著(P < 0.05)。而中度干旱胁迫(MS)和重度干旱胁迫(SS)叶绿素b含量则分别下降22.03%、35.60%,中度干旱胁迫后复水(MS-CK)、重度干旱胁迫后复水(SS-CK)叶绿素b含量分别升高了6.52%、2.26%,处理间叶绿素b含量差异显著(P < 0.05)。中度干旱胁迫(MS)和重度干旱胁迫(SS)类胡萝卜素含量分别降低了29.41%、45.10%,中度干旱胁迫后复水(MS-CK)、重度干旱胁迫后复水(SS-CK)类胡萝卜素含量分别升高了8.33%、2.14%,但未达到对照(CK)水平,中度干旱胁迫(MS)和重度干旱胁迫(SS)处理间类胡萝卜素含量差异显著(P < 0.05),而中度干旱胁迫后复水(MS-CK)及重度干旱胁迫后复水(SS-CK)处理间差异不显著(P>0.05)。
-
根系是植物吸收水分和转化养分的重要器官,同时也是一些内源激素合成的重要部位,根的生长情况和活力水平能够直接影响到地上部分的营养情况及产量水平[19]。由表 1可以看出,随着干旱胁迫程度的加重,绿竹根系活力均显著下降(P < 0.05),但不同水分胁迫降幅不同,中度干旱胁迫(MS)的下降程度显著小于重度干旱胁迫(SS)。其中,中度干旱胁迫(MS)和重度干旱胁迫(SS)的根系活力分别比对照(CK)下降了14.35%、33.31%,而中度干旱胁迫后复水(MS-CK)和重度干旱胁迫后复水(SS-CK)根系活力均有不同程度的恢复,但均未达到对照(CK)的水平,不同干旱处理间均达到差异显著(P < 0.05)。不同程度干旱处理后复水的根系活力恢复能力差异较大,中度干旱胁迫后复水(MS-CK)根系活力恢复达对照(CK)的96.75%,远高于重度干旱胁迫后复水(SS-CK)(CK的73.84%),也即不同程度干旱处理后复水均会产生一定的补偿效应。中度干旱胁迫后复水(MS-CK)根系活力恢复程度明显高于重度干旱胁迫后复水(SS-CK),表明绿竹在未达到严重缺水时,具有较强的根系活力恢复能力。
干旱处理Drought treatment 根系活力Root activity/(μg·g-1·h-1) 对照CK 91.08±1.16A 中度干旱胁迫MS 78.01±1.17C 重度干旱胁迫SS 60.74±1.05E 中度干旱胁迫后复水MS-CK 88.12±0.74B 重度干旱胁迫后复水SS-CK 67.25±0.58D Table 1. Root activity of D.oldhamii with different drought stress and re-watering treatment
-
超氧化物歧化酶(SOD)是植物体内清除活性氧系统的第一道防线,能够清除细胞内的超氧自由基,保护暴露于空气中的细胞,其表达量高低与活性的强弱都直接决定了植物的抗逆性[20]。由图 2可以看出,两种程度干旱胁迫下绿竹容器苗根系及成熟叶片的SOD活性均随着胁迫强度增大而明显增加,但变化幅度不同,重度干旱胁迫(SS)变化幅度明显大于中度干旱胁迫(MS)(P < 0.05)。根系在中度干旱胁迫(MS)和重度干旱胁迫(SS)下的SOD活性分别比对照(CK)增加23.08%、46.15%,叶片在两种程度干旱胁迫下的SOD活性分别比对照(CK)增加23.37%、56.25%。

Figure 2. Root and leaves SOD enzyme activity of D. oldhamii with different drought stress and re-watering treatment
复水后,SOD活性相比于干旱胁迫明显降低,且降低幅度也不同,但均高于对照(CK)。其中,绿竹根系中度干旱胁迫后复水(MS-CK)的SOD活性比中度干旱胁迫(MS)时降低了16.80%,重度干旱胁迫后复水(SS-CK)SOD活性较重度干旱胁迫(SS)降低了11.34%。叶片在中度干旱胁迫后复水(MS-CK)SOD活性比中度干旱胁迫(MS)下降低12.82%,重度干旱胁迫后复水(SS-CK)SOD活性比重度干旱胁迫(SS)时降低9.89%。可见,不同程度干旱胁迫后复水,中度干旱胁迫(MS)SOD活性恢复能力显著强于重度干旱胁迫(SS)(P < 0.05)。
-
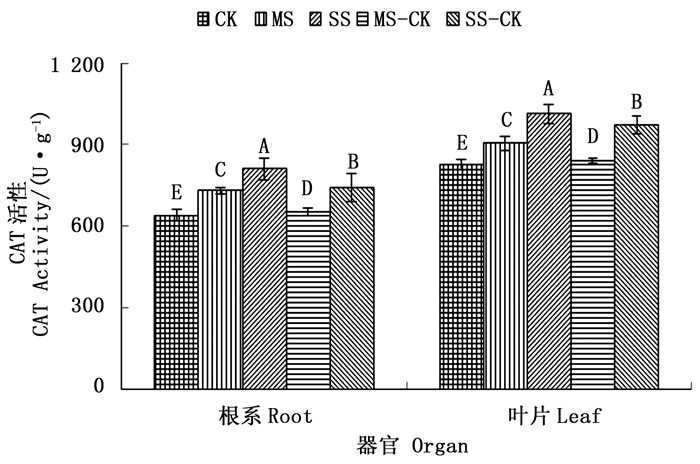
过氧化氢酶(CAT)是植物体内一种重要的保护酶,它能够清除经SOD氧化超氧自由基CO2-而形成的H2O2,使其维持在较低的水平,以保护膜结构免受损伤[21]。由图 3可以看出,两种程度干旱胁迫下绿竹容器苗根系及成熟叶片的CAT活性变化趋势基本相同,但变化幅度不同,重度干旱胁迫(SS)变化幅度明显大于中度干旱胁迫(MS)(P < 0.05)。根系在中度干旱胁迫(MS)和重度干旱胁迫(MS)下的CAT活性分别比对照(CK)增加14.06%、26.88%;叶片在两种程度干旱胁迫下的CAT活性分别比对照(CK)增加9.70%、22.91%。

Figure 3. Root and leaves CAT enzyme activity of D. oldhamii with different drought stress and re-watering treatment
复水后,CAT活性较干旱胁迫明显下降,且降低幅度不同,但均高于对照(CK),各干旱处理间均达到差异显著(P < 0.05)。其中,绿竹根系在中度干旱胁迫后复水(MS-CK)和重度干旱胁迫后复水(MS-CK)的CAT活性,分别比中度干旱胁迫(MS)和重度干旱胁迫(SS)时降低10.55%、8.62%。叶片在中度干旱胁迫后复水(MS-CK)和重度干旱胁迫后复水(SS-CK)的CAT活性,分别比中度干旱胁迫(MS)和重度干旱胁迫(SS)时降低6.96%、4.14%。
-
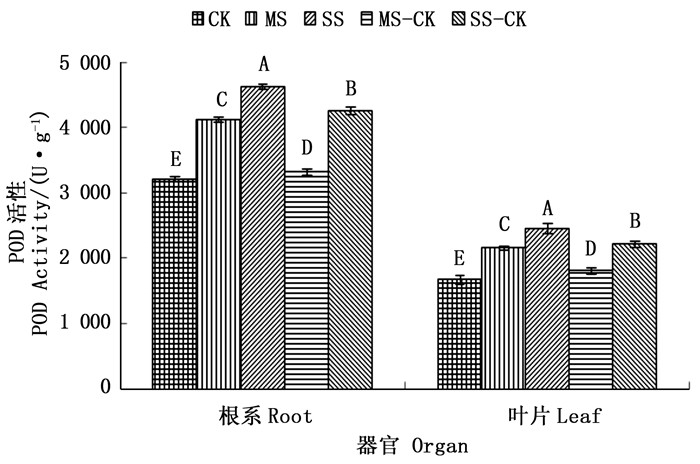
过氧化物酶(POD)是植物体内清除H2O2的主要保护酶,能够在一定程度上催化H2O2,并在其它底物氧化后产生H2O [22]。由图 4可以看出,两种程度干旱胁迫下绿竹容器苗根系及成熟叶片的POD活性均随着胁迫强度增大而明显增加,但变化幅度不同,重度干旱胁迫(SS)变化幅度明显大于中度干旱胁迫(MS)(P < 0.05)。根系在中度干旱胁迫(MS)和重度干旱胁迫(MS)下的POD活性分别比对照(CK)增加28.38%、44.03%,叶片在两种程度干旱胁迫下的POD活性分别比对照(CK)增加28.93%、46.79%,叶片POD活性增加高于根系,且差异显著(P < 0.05)。

Figure 4. Root and leaves POD enzyme activity of D. oldhamii with different drought stress and re-watering treatment
复水后,POD活性呈现降低趋势,但均高于对照(CK),且不同干旱胁迫处理降幅不同。其中,绿竹根系在中度干旱胁迫后复水(MS-CK)和重度干旱胁迫后复水(SS-CK)的POD活性,分别比中度干旱胁迫(MS)和重度干旱胁迫(SS)时降低19.55%、7.92%。叶片在中度干旱胁迫后复水(MS-CK)和重度干旱胁迫后复水(SS-CK)的POD活性,分别比中度干旱胁迫(MS)和重度干旱胁迫(SS)时降低16.25%、9.56%。可见,不同程度干旱胁迫后复水,中度干旱胁迫后复水(MS-CK)POD活性恢复能力显著强于重度干旱胁迫后复水(SS-CK)(P < 0.05),且成熟叶片的POD活性低于根系,但未达到差异显著(P>0.05)。
-
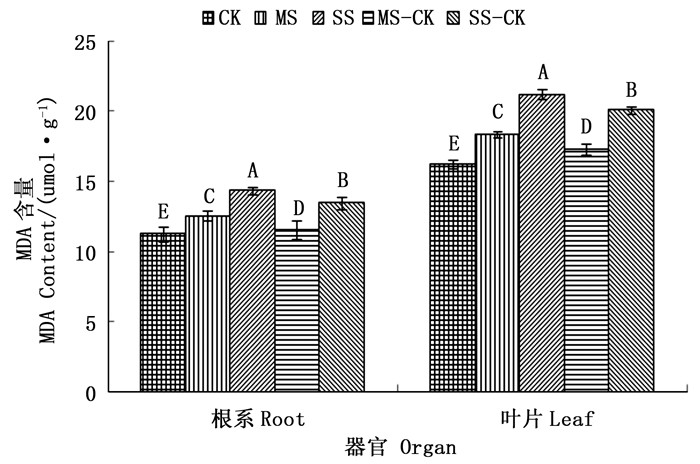
植物在受到干旱胁迫时往往会发生质膜过氧化,丙二醛(MDA)是质膜过氧化的最终分解产物,它的积累会对植物造成一定伤害,因此其含量可以反映出植物遭受干旱伤害的程度[23]。由图 5可以看出,干旱胁迫后,绿竹根系及成熟叶片MDA含量明显增加,且增加的程度与受胁迫程度呈正相关,不同器官的增加幅度不同。干旱胁迫后,中度干旱胁迫(MS)和重度干旱胁迫(SS)的MDA含量均高于对照(CK),且重度干旱胁迫(SS)的MDA含量明显高于中度干旱胁迫(MS),达到差异显著(P < 0.05)。根系的MDA含量在中度干旱胁迫(MS)和重度干旱胁迫(SS)后分别比对照(CK)增加11.69%、27.65%,叶片的MDA含量在两种程度干旱胁迫后则分别比对照(CK)增加13.06%、30.43%。

Figure 5. Root and leaf MDA content of D. oldhamii with different drought stress and re-watering treatment
复水后,绿竹的叶片及根系MDA含量均有不同程度下降,但均高于对照(CK),且不同程度干旱胁迫MDA含量恢复能力也不同。根系在中度干旱胁迫后复水(MS-CK)和重度干旱胁迫后复水(SS-CK)的MDA含量,分别比中度干旱胁迫(MS)和重度干旱胁迫(SS)时降低8.07%、6.22%。叶片在中度干旱胁迫后复水(MS-CK)和重度干旱胁迫后复水(SS-CK)的MDA含量,则分别比中度干旱胁迫(MS)和重度干旱胁迫(SS)时降低5.94%、5.29%。根系及叶片经中度干旱胁迫后复水(MS-CK)的MDA含量降幅明显大于重度干旱胁迫后复水(SS-CK),说明中度干旱胁迫后复水(MS-CK)MDA含量恢复能力要强于重度干旱胁迫后复水(SS-CK),且两者差异显著(P < 0.05)。复水后绿竹根系的MDA含量降幅较大,说明根系具有较强的恢复和补偿能力。
2.1. 不同干旱胁迫下绿竹叶片色素含量的差异
2.2. 干旱胁迫及复水对绿竹根系活力的影响
2.3. 干旱胁迫及复水对绿竹根系保护酶活性的影响
2.3.1. SOD活性差异分析
2.3.2. CAT活性差异分析
2.3.3. POD活性差异分析
2.3.4. MDA含量差异分析
-
在干旱胁迫条件下,高的叶绿素含量能够维持光合作用的进行,有利于提高植物的抗旱性[24]。相关研究显示,随着模拟干旱程度的增强,鼓节竹的叶绿素a、叶绿素b以及类胡萝卜素含量都在降低,同时伴随有叶绿素a/b的升高[25]。类胡萝卜素在植物体内除了担任光合色素以外,也能够作为内源抗氧化剂,可吸收细胞内剩余能量,淬灭活性氧,防止质膜过氧化发生[26]。本研究发现,在不同干旱胁迫下,绿竹光合色素含量随着干旱程度加深均有不同程度的减少。其中,类胡萝卜素含量随着干旱胁迫加剧而明显降低,并且显著低于对照(CK),这与Willekens H等[27]干旱胁迫下烟草叶片类胡萝卜素含量升高,且类胡萝卜素仍具有较强保护能力的研究结果不同。
根系活力能够直接反映植物整个根系代谢程度的强弱,包含了吸收、氧化力、呼吸作用、合成等,是能够客观反映植物根系生命活动的生理指标,对植物生长发育起到了决定性的作用[28]。本试验表明,干旱胁迫能够导致植物根系活力下降,并且在不同程度干旱胁迫下根系活力表现出较大差异。说明干旱胁迫显著影响植物根系吸收水分的能力,这与闫江艳等[29]对黍稷(Panicum miliaceum L.)干旱胁迫的研究结果相一致。
植物为保护其自身免受氧化伤害会在其体内形成一套相应的抗氧化保护酶系统,如超氧化物歧化酶(SOD)、过氧化氢酶(CAT)和过氧化物酶(POD)等,保护敏感分子和细胞膜而免受活性氧的伤害[30]。植物对逆境的适应以及在清除植物体内的超氧自由基(O2-)、过氧化物、过氧化氢等方面都与保护酶的活性密切相关。赵兰等[17]对黄条金刚竹(Pleioblastus kongosanensis f. aureostriatus Muroi et Yuk. Tanaka)、菲白竹(Sasa fortunei (Van Houtte) Fiori)、铺地竹、菲黄竹(Sasa auricoma E. G. Camus)4种观赏竹抗旱胁迫发现,随着人工控水干旱时间延长,细胞的膜脂透性及丙二醛(MDA)含量呈上升趋势,而抗氧化酶活性(CAT、POD、SOD)呈现先升后降的趋势。本研究表明,在干旱胁迫下,绿竹叶片的SOD、CAT、POD活性均随着干旱胁迫程度的增加有不同程度的升高,这与张磊等[7]对伐桩注水下毛竹叶片抗氧化系统的研究结论相一致。受到干旱胁迫后,绿竹成熟叶片和根系的保护酶活性均呈现升高趋势,但在不同营养器官变化幅度也不尽相同,这可能与绿竹根系产生超氧阴离子的比例较大,而产生过氧化氢、羟自由基的比例较小,同时与绿竹中的POD同工酶相关基因表达较少有关[31]。
丙二醛(MDA)是生物体内自由基作用于脂质发生过氧化反应,经一系列氧化作用的终产物,它能与细胞内核酸、蛋白质等一系列生物大分子发生交联聚合,引起细胞膜受损,从而产生细胞毒害,并且在水分胁迫下,植物的MDA含量会随着胁迫加剧而逐渐升高[32]。本研究显示相似的结论,随着干旱胁迫加重,绿竹根系及成熟叶片MDA含量均增加,但增加幅度不同。表现为在干旱胁迫下,叶片较根系具有较高的MDA含量,表明绿竹容器苗根系的细胞膜相对于叶片具有更强的抗膜脂过氧化能力。
-
植物在遭受干旱胁迫后,复水可以检测植物自身是否有适应干旱胁迫的能力[33]。周自云等[34]在对酸枣(Ziziphus jujuba Mill. var. spinosa (Bunge) Hu ex H. F. Chow)进行多次干旱复水后,发现能够锻炼其适应干旱逆境的能力,并且植物在经历适度干旱胁迫后复水,能够产生补偿或超补偿效应,弥补干旱对植物造成的损失。
本试验发现,绿竹中度干旱胁迫后复水(MS-CK)的抗氧化酶活性高于对照(CK),并且产生细胞毒害的丙二醛(MDA)含量迅速降低,表现出一定的耐旱性。其中,(1)中度干旱胁迫后复水(MS-CK)的色素恢复显著高于重度干旱胁迫后复水(SS-CK),这可能是由于过度干旱胁迫后叶绿体片层中的捕光Chl a/b-Pro复合体合成受到抑制或损伤所致,进而阻止了叶绿素积累和原叶绿素酯的形成,造成叶绿素含量降低,同时叶绿素自身存在的氧化降解也是其含量降低的影响因素之一[35]。另外,脂质过氧化作用诱导也可能导致叶绿素含量的降低,因而可以解释其含量与丙二醛(MDA)含量表现为一定的协同性。(2)中度干旱胁迫后复水(MS-CK)和重度干旱胁迫后复水(SS-CK)两个处理的根系活力均有不同程度的恢复,但均未达到对照(CK)的水平。在重度干旱胁迫(SS)下,根系对矿质营养和水分的吸收能力受到严重影响,而中度干旱胁迫(MS)受到的伤害较小,具有更快的恢复能力。这与闫江艳等[29]对黍稷根系干旱后复水的研究结果相一致。(3)反映膜脂抗氧化能力的保护酶活性在复水后均明显降低,且不同营养器官对于解除干旱后消除活性氧及修复适应能力也不尽相同,该结果与李黎等[10]对毛竹的研究结论相似。另外,过氧化氢酶(CAT)在成熟叶片中活性显著高于根系,这可能是由于CAT是清除过氧化氢的辅助酶,因此在此时期起到了关键酶的作用。(4)复水后,根系在不同程度干旱胁迫下,MDA含量增加均低于叶片,并且在复水后下降更迅速。研究结果与王智威等[36]苗期玉米干旱胁迫下水分对根系的影响小于叶片,并且叶片为MDA积累的主要场所的结论相同,这说明绿竹不同器官在启动膜脂过氧化和膜脂脱脂化作用中,根系仍能保持较强的减轻质膜过氧化作用的能力,而叶片的细胞膜已经受到较大伤害,这也与任庆成等[37]对烤烟(Nicotiana tabacum Linn.)的研究结论相同。总体来说,MDA含量变化同抗氧化酶系统具有相似性,表现为中度干旱胁迫(MS)下具有更强的恢复和补偿能力。
3.1. 干旱胁迫下绿竹生理特性变化
3.2. 干旱胁迫继复水后绿竹生理特性变化
-
研究表明,在中度干旱胁迫(田间持水量的50%~55%)下,绿竹受影响程度较小,而在重度干旱胁迫(田间持水量的30%~35%)下,根系活力、抗氧化酶等各项指标都反映了绿竹的主要营养器官受到伤害。复水后,绿竹在抗逆能力上表现出一定的补偿效应,表现为根系活力在中度干旱胁迫下接近正常水平;抗氧化酶活性均高于正常水平,受到了较好的抗逆锻炼;膜脂透性受到轻微伤害后,累积的丙二醛(MDA)含量在中度干旱胁迫下也接近正常水平。一般来说,在干旱胁迫及复水条件下能维持较高的根系活力、保护酶活性等和较低MDA含量的植物,在一定程度上就具有较好的抗旱高产特性,可以为抗旱育种及苗圃节水灌溉技术措施的制订和实施提供理论依据。





 DownLoad:
DownLoad: