-
Paxillus ammoniavirescens (Contu & Dessi) 在分类学上属于担子菌门(Basidiomycota)、伞菌纲(Agaricomycetes)、牛肝菌目(Boletales)、网褶菌科(Paxillaceae)、网褶菌属(Paxillus)。Paxillus Fr.属在北半球分布广泛,与多种寄主树木如杨、桦、栎、椴树、云杉、冷杉等形成外生菌根关系[1-2]。
网褶菌属种类富含褐色色素,受伤则变褐棕色,Paxillus involutus (Batsch) Fr.是“舒筋散”中药的重要成分之一,有治腰腿疼痛、手足麻木、祛风散寒、舒筋活络等功效。该属很多种类在记载中有毒[3]或生吃有毒[4-5],可出现胃肠道病症[3],但在我国北方一些地区却广泛采食[6]。P. involutus在前苏联时期曾被大量腌制后食用,在中欧、德国等地均有食用,但在德国和波兰等国曾发生食用者中毒现象[7]。据报道,摄入该菌后可造成免疫溶血甚至致命[8-9]。肖冬来等人[10]已在P. ammoniavirescens中检测出有溶血素蛋白。然而,根据不同国家的观察者的经验,对该菌和其他近缘种是否有害的评估是不同的。“毒性”评估的差异可能取决于物种的差异鉴定。
P. involutus是研究最广泛的外生菌根 (ECM) 真菌之一。该菌在北半球发生普遍,与许多针叶树和落叶树形成外生菌根[2]。该菌在形态学、生理学和生态学等有关表型性状上表现出明显的变异,也是伞菌纲外生菌根菌生态学或生理学研究的一个重要模式种[11]。在生物修复重金属污染方面,植物和真菌形成的菌根共生体已显示出巨大的应用潜力[12]。菌根真菌可提高宿主植物对重金属的耐受性,在缓解植物受重金属毒害方面具有重要作用[13-15]。P. involutus 不仅能与耐镉植物灰杨(Populus tremula × P.alba) 形成外生菌根,提高灰杨对Cd2+的吸收和耐受能力[16],其本身也具有较强的Cd2+ 富集能力[17]。抗盐菌根菌Paxillus在盐胁迫下具有维持K+/Na+平衡的能力,可提高树木耐盐性[18]。
Paxillus属的特点是难以进行物种鉴定,导致再生困难,因此,需要大量的菌种[1]。为了更好地了解、保护、开发大型野生食用菌资源,有必要对该物种的分类问题进行深入研究。目前,内转录间隔区ITS (internal transcribed spacer) 基因序列分析法广泛应用于野生真菌的鉴定和分类中,是一种非常可靠的方法。目前,国内缺少对网褶菌属的分子系统研究,已有资料多是关于其可食性和生态学特性方面[19-20]。国外对网褶菌属研究较多,常将P. involutus作为外生菌根菌研究的模式种[21]。目前,关于P. involutus和P. rubicundulus P.D. Orton的基因组已经完全测序[22-23]。本研究从黑龙江农业经济职业学院校园内分离获得一株野生网褶菌属菌株,拟通过分子鉴定以及生物学特性研究,为进一步开发利用提供理论基础。
-
供试野生菌样品(图1)于2014年9月采自黑龙江省牡丹江市黑龙江农业经济职业学院校园内云杉(Picea asperata Mast.)树根部周围,菌样编号为DP20140901。
-
取子实体完整部分,观察并描述其表面性状、结构、颜色、质地,进行形态学特征初步鉴定。
-
采用子实体组织分离法分离菌种,在PDA平板上培养8~10 d后,挑取菌落边缘菌丝体进行转接和纯化培养,于25 ℃恒温培养箱中培养2周,置于4 ℃冰箱保存备用。
-
菌丝体培养、收集及DNA提取和检测方法详见文献[24]。
-
采用真菌通用引物ITS5: 5′-GGAAGTAAAAGTCGTAACAAGG-3′;ITS4: 5′-TCCTCCGCTTATTGATATGC-3′,由英骏生物技术有限公司(invitrogen)合成[25]。PCR 扩增体系为:10 × Buffer 5 μL,25 mmol·L−1 MgCl2 4 μL,4 mmol dNTPs 3 μL,5 U·µL−1 Taq DNA polymerase 0.5 μL,10 μmol·L−1引物各2 μL,模板DNA 2 μL,ddH2O 31.5 μL,反应总体积为50 μL。扩增条件:94 ℃预变性1 min;94 ℃变性30 s,60 ℃退火1 min,72 ℃延伸1.5 min,共30个循环;最后于72 ℃延伸8 min,终止温度为4 ℃。扩增产物经1.5%琼脂糖凝胶电泳检测,产物和Marker上样量均为5 μL,电泳结果于Bio-Rad凝胶成像系统成像。PCR扩增产物送交华大基因(北京)公司测序。
-
将测序获得的ITS序列通过NCBI进行Blast搜索,分析同源性。选择与供试菌株ITS序列相似度99%以上的23条序列,以黑木耳Auricularia heimuer F. Wu, B.K. Cui, Y.C. Dai的ITS 序列[26]为外群构建系统发育树,采用Clustal X 1.83程序进行多序列匹配排列,然后通过MEGA-X程序中的Neighbor-Joining (NJ) 方法、采用Jukes-Cantor 计算模型构建系统发育树,进行1 000 次Bootstrap 可信度分析,Kimura 2-parameter 法计算遗传距离,空位作为完全缺失处理。
-
试验碳源:麦芽糖、甘露醇、可溶性淀粉、蔗糖、葡萄糖为分析纯。此外,采用市售玉米粉作为碳源之一。
无碳基础培养基:KH2PO4 1.0 g,MgSO4 0.5 g,蛋白胨2 g,琼脂18 g,水1 L。分别以等量的(2%)麦芽糖、甘露醇、可溶性淀粉、玉米粉、蔗糖、葡萄糖加入到无碳基础培养基中。对P. ammoniavirescens母种培养基中碳源进行单因素筛选试验。各设4个重复。接种菌饼后置于25 ℃下恒温培养。接种2 d后开始记录菌丝体生长速度,观察记录菌落特征、生长势等。其中菌丝体生长速度= 菌落半径(mm)/菌丝生长天数(d)。菌丝体日均生长速度差异显著性采用SPSS 16.0 软件中Duncan式新复极差法进行分析。
-
试验氮源:牛肉膏、硫酸铵、酵母膏、蛋白胨为分析纯。此外,采用市售麦麸和黄豆粉作为有机氮源。
无氮基础培养基:葡萄糖20 g,KH2PO4 1.0 g,MgSO4 0.5 g,琼脂18 g,水1 L。分别以等量的(0.2%)牛肉膏、麦麸、硫酸铵、酵母膏、黄豆粉、蛋白胨加入到无氮基础培养基中。对卷边网褶菌母种培养基中氮源进行单因素筛选试验。其余方法同上。
-
将含有最适碳源和氮源的无菌培养基制成平板,接种菌饼后,分别置于21、23、25、27、29、31 ℃的恒温培养箱中暗培养,其余方法同上。
-
采用1 mol·L−1 HCl 或NaOH 溶液,将含有最适碳源和氮源的液体培养基(可溶性淀粉20 g,蛋白胨2 g,KH2PO4 1.0 g,MgSO4 0.5 g,水1 L)调配为pH 2.0~8.0共13个处理(间隔0.5),每250 mL三角瓶装液量为30 mL,每个处理4次重复,于25 ℃恒温培养箱中静止培养。培养两周测量菌丝体干质量,并记录菌丝体长势、菌丝体及发酵液颜色变化等。
-
从碳源(可溶性淀粉)、氮源(蛋白胨)和无机盐(KH2PO4和MgSO4)中各选出3个水平,进行四因素三水平的正交试验,以确定各组分的最佳使用量。250 mL三角瓶的装液量为50 mL,灭菌前用1 mol·L−1 HCl 或NaOH 溶液调节培养液为pH 4.5,接种菌饼后于25 ℃恒温培养箱中静止培养20 d,其余方法同1.5.4。
-
菌盖半球形,平展或中央下凹近漏斗状,边缘内卷,直径4~15 cm。幼菇菌盖表面微粘,成熟后干燥,中央多成龟裂状。菌盖多绒至平滑,黄至红褐色。菌肉厚,黄褐色,伤后变红变褐黑色。菌褶延生,黄褐色,伤后初转红再转黑褐色。菌柄圆柱状,上下同粗,长4~8 cm,直径1~2 cm,表面光滑,颜色同菌盖,实心。子实体有特异性气味。经查阅图鉴,初步判定为网褶菌属种类[20]。
-
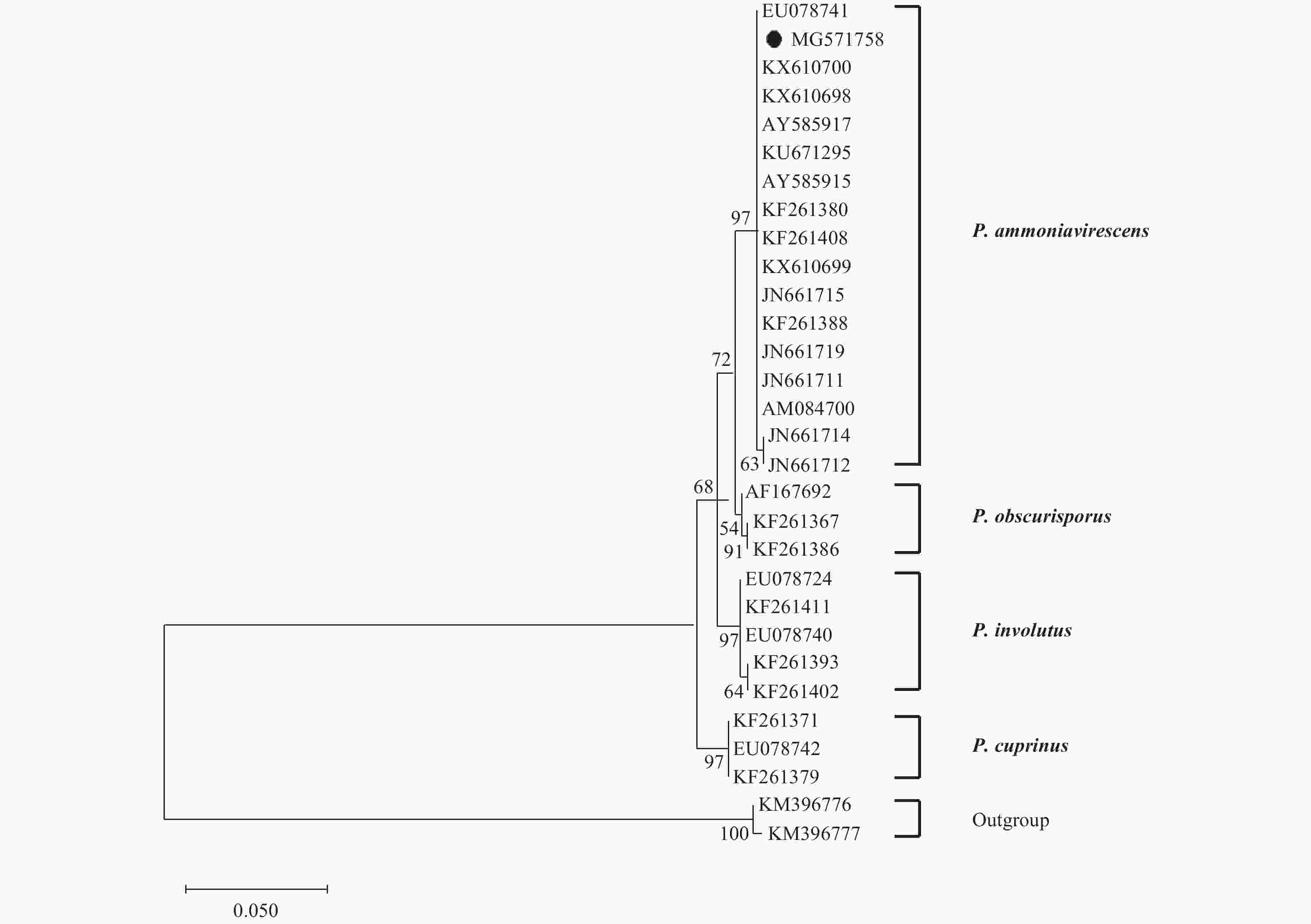
经测序获得菌株ITS区域核苷酸序列总长为746 bp,将样品ITS序列(序列号是MG571758)输入NCBI系统,用Blast进行搜索比对,结果有23株核酸序列与其具有99%以上的相似度,分别来自英国、美国、德国、法国、加拿大、澳大利亚、爱尔兰、西班牙、意大利、波兰等国家,没有发现中国的报道;宿主及生长环境有椴树(Tilia)、栎树(Quercus)、桦树(Betula)、杨树(Populus)、公园、草原等地(表1)。当物种的rDNA ITS区序列与比对序列同源性≥99%时,可认为相同种[27]。因此,鉴定该株野生菌为Paxillus ammoniavirescens。它的5.8 S和内转录间隔区2(ITS 2)具有高度保守性,5.8 S编码序列一般为158 bp,ITS 2一般为229 bp;内转录间隔区1(ITS 1)序列中度保守,在275 bp左右;18 S和28 S基因序列变化幅度较大。ITS序列在655~746 bp左右。
表 1 本研究中使用的物种来源和ITS 区域的GenBank序列号信息
Table 1. A list of species, origin and GenBank accession number of ITS sequences used in this study
序号No. 登录号
Accession no.种名
Species name来源国
Country生长宿主
Recorded trees1 ●MG571758 Paxillus ammoniavirescens China 云杉 Picea asperata 2 AM084700 Paxillus ammoniavirescens England 未知 Unknowna 3 AY585915 Paxillus ammoniavirescens France 栎树Quercusa 4 AY585917 Paxillus ammoniavirescens France 杨树 Populusb 5 KX610700 Paxillus ammoniavirescens Poland 未知 Unknownd 6 KX610698 Paxillus ammoniavirescens Poland 未知 Unknownd 7 JN661712 Paxillus ammoniavirescens England 栎树 Quercuse 8 JN661719 Paxillus ammoniavirescens Italy 杨树 Populuse 9 JN661715 Paxillus ammoniavirescens France 木本植物Woody plantse 10 JN661714 Paxillus ammoniavirescens England 椴树 Tiliae 11 KU671295 Paxillus ammoniavirescens Spain 木本植物 Woody plantsc 12 JN661711 Paxillus ammoniavirescens England 混合林 Mixed foreste 13 EU078741 Paxillus ammoniavirescens Sweden 栎树、桦树Quercus, Betulab 14 KX610699 Paxillus ammoniavirescens Poland 未知 Unknownd 15 KF261380 Paxillus ammoniavirescens France 桦树 Betulaf 16 KF261408 Paxillus ammoniavirescens France 冷杉 Abiesf 17 KF261388 Paxillus ammoniavirescens France 栎树 Quercusf 18 AF167692 Paxillus obscurisporus C. Hahn (1999) Germany 栎树 Quercusf 19 KF261367 Paxillus obscurisporus France 桦树 Betulaf 20 KF261386 Paxillus obscurisporus France 榛树 Corylusf 21 EU078724 Paxillus involutus Sweden 云杉 Piceaf 22 KF261411 Paxillus involutus France 冷杉 Abiesf 23 EU078740 Paxillus involutus Sweden 未知 Unknownb 24 KF261393 Paxillus involutus France 松树、桦树 Pinus, Betulaf 25 KF261402 Paxillus involutus France 冷杉 Abiesf 26 KF261371 Paxillus cuprinus Jargeat, Gryta, J.P. France 未知 Unknownf 27 EU078742 Paxillus cuprinus Sweden 栎树、桦树Quercus, Betulaf 28 KF261379 Paxillus cuprinus France 桦树 Betulaf 29 KM396776 Auricularia heimuer China 栎树 Quercusg 30 KM396777 Auricularia heimuer China 栎树Quercusg 注:a-f字母分别代表参考的文献。
Note: a According to Anderson & Parkin[28]. b According to Hedh et al.[12]. c According to Fernandez & Cagigal[29]. d According to Kalucka et al.[30]. e According to Vellinga et al.[31]. f According to Jargeat et al.[21]. g According to Wu et al.[26].从图2系统发育树可以看出,所有分析菌株共分为4类,即P. ammoniavirescens,P. obscurisporus,P. involutus和P. cuprinus,而实验菌株与P. ammoniavirescens种类聚为一枝,因此,被鉴定为P. ammoniavirescens。
-
由表2、图3可见,P. ammoniavirescens菌丝体在供试碳源培养基上均能生长,菌丝体颜色因碳源种类不同而呈浅黄至黄灰色(图3)。在0.05水平上,菌丝体日均生长速度差异显著(表2),其中在可溶性淀粉和葡萄糖培养基上日均生长速度最快,菌丝体浓密,长势强;其次是甘露醇、蔗糖为碳源的培养基,菌丝体较密,生长整齐,与玉米粉培养基上的菌丝体日均长速差异不显著;而在无碳基础培养基(CK)上生长速度最慢,菌丝体稀疏,颜色浅,长势弱。可见,P. ammoniavirescens菌丝体生长对碳源的需求量较大,且来源广泛。此外,菌丝体颜色因碳源种类不同而呈浅黄至黄灰色,说明碳源种类不同影响 P. ammoniavirescens 菌丝体的颜色。
表 2 碳源对Paxillus ammoniavirescens菌丝体生长的影响
Table 2. Effect of carbon sources on mycelial growth of Paxillus ammoniavirescens
碳源
Carbon source菌丝长势
Hyphal vigor日均长速
Daily growth rate/(mm·d−1)菌丝密度、整齐度
Hyphal density and uniformity麦芽糖
Maltose+++ 0.653c* 浓密、整齐
Dense, tidy甘露醇
Mannitol+++ 0.833b 浓密、整齐
Dense, tidy可溶性淀粉
Soluble starch+++ 0.978a 浓密、不齐
Dense, untidy玉米粉
Corn flour++ 0.713bc 较密、整齐
Relatively dense, tidy蔗糖
Sucrose++ 0.798b 较密、整齐
Relatively dense, tidy葡萄糖
Glucose+++ 0.968a 浓密、较整齐
Dense, relatively tidyCK + 0.469d 稀疏、不整齐
Sparse, untidy注:+表示菌丝体稀疏、生长势较弱;++表示菌丝体较密、生长势较强;+++表示菌丝体浓密、生长旺盛;*差异显著性(0.05)。
Note: + sparse mycelia, weaker growth vigor; ++ relatively dense mycelia and comparatively strong growth vigor; +++ dense mycelia and strong growth vigor. The lower case letters after daily growth rate indicating a significant difference at p 0.05. -
试验菌株菌丝体在不同氮源培养基上均能生长,颜色因培养基种类不同而呈浅黄至黄褐色,并有不同程度的褐色素分泌。在0.05水平上,菌丝体的日均生长速度差异显著(表3),其中在蛋白胨培养基上日均生长速度最快,菌丝体浓密,粗壮,边缘生长整齐,菌丝体日均生长速度为0.857 mm·d−1;其次是麦麸和黄豆粉为氮源的培养基,但菌丝体生长较稀疏;在酵母膏培养基上菌丝体生长浓密,但长速较慢。而在无氮基础培养基(CK)中生长速度最慢,菌丝体稀疏,颜色浅,可见,P. ammoniavirescens菌丝体生长对氮源种类要求较严格。
表 3 氮源对Paxillus ammoniavirescens菌丝体生长的影响
Table 3. Effect of nitrogen sources on mycelial growth of Paxillus ammoniavirescens
氮源
Nitrogen source菌丝长势
Hyphal vigor日均长速
Daily growth rate/(mm·d−1)菌丝密度、整齐度
Hyphal density and uniformity牛肉膏
Beef extract++ 0.644bc* 较密、整齐
Relatively dense, tidy麦麸
Wheat bran++ 0.743b 较密、整齐
Relatively dense, tidy硫酸铵
Ammonium sulfate++ 0.467de 较密、整齐
Relatively dense, tidy酵母膏
Yeast extract+++ 0.563cd 浓密、较整齐
Dense, relatively tidy黄豆粉
Soybean meal+ 0.668b 稀疏、整齐
Sparse, tidy蛋白胨
Peptone+++ 0.857a 浓密,整齐
Dense, tidyCK + 0.429e 稀疏、不齐
Sparse, untidy表注同表1;Foot notes as in Table 1 -
由表4可见,试验菌株通过不同温度试验表明,试验菌株在21~29 ℃范围内均能生长,其中25 ℃时生长速度最快,长势最好,其次为27 ℃,而31 ℃时菌丝体不生长,表明P. ammoniavirescens菌丝体生长对温度要求严格,过高或过低均不利,且适宜生长温度范围较窄。
表 4 温度对Paxillus ammoniavirescens菌丝体生长的影响
Table 4. Effect of temperature on mycelial growth of Paxillus ammoniavirescens
温度/℃
Temperature菌丝体长势
Hyphal vigor日均长速
Daily growth
rate/(mm·d−1)菌丝体密度、整齐度
Hyphal density and uniformity21 ++ 0.514d* 较密、整齐
Relatively dense, tidy23 ++ 0.696c 较密、较整齐
Relatively dense and tidy25 +++ 1.257a 浓密、较整齐
Dense, relatively tidy27 +++ 1.002b 浓密,整齐
Dense, tidy29 +++ 0.785c 较密、整齐
Relatively dense, tidy31 + 0.214e 稀疏、不齐
Sparse, untidy表注同表1; Foot notes as in Table 1 -
由表5可以看出,试验菌株菌丝体在pH 2.0~6.0范围内均能生长,其中在pH 4.5时长势最好,菌丝体干质量均高于其他处理;当pH大于5.0时菌丝体生长速度逐渐减慢,菌丝体生物量减少,当pH≥6.5时菌丝体几乎不生长,说明P. ammoniavirescens喜欢偏酸性环境条件,且适宜生长的酸碱度范围较窄。
表 5 酸碱度对Paxillus ammoniavirescens菌丝体生长的影响
Table 5. Effect of pH on mycelial growth of Paxillus ammoniavirescens
酸碱度
pH菌丝体长势
Hyphal vigor菌丝体干质量
Mycelial
dry weight/mg菌丝体颜色、发酵液颜色
Color of mycelia and
fermentation broth2.0 ++ 15bc* 黄色、淡黄
Yellow, light yellow2.5 ++ 20bc 黄色、淡黄
Yellow, light yellow3.0 +++ 32.5ab 黄棕色、黄棕色
Yellowish brown, yellowish brown3.5 +++ 32.5ab 黄棕色、棕黄色
Yellowish brown, yellowish brown4.0 +++ 33ab 黄棕色、棕黄色
Yellowish brown, yellowish brown4.5 +++ 50a 黄色、黄色
Yellow, yellow5.0 +++ 33ab 黄色、黄色
Yellow, yellow5.5 ++ 25bc 淡黄色、淡黄色
Light yellow, light yellow6.0 + 20bc 淡黄色、黄白色
Light yellow, yellowish white6.5 + 13bc 白色、白色
White, white7.0 + 12.5bc 白色、黄白色
White, yellowish white7.5 + 12.5bc 白色、黄白色
White, yellowish white8.0 + 10c 白色、黄白色
White, yellowish white表注同表1;Foot notes as in Table 1 -
由表6可以看出,P. ammoniavirescens菌丝体在不同碳源、氮源、无机盐用量的培养基中长势良好,菌丝体及发酵液颜色变化不明显(图4)。其中配方4的菌丝体干质量最大,为80 mg,与配方1、2、5、6和8的菌丝体干质量差异不明显,与配方3、7和9的菌丝体干质量差异显著。由正交试验优化的菌丝体培养的最佳组合为:A2B1C2D3,即可溶性淀粉20 g,蛋白胨2 g,KH2PO4 3.0 g,MgSO4 4.5 g,水1 L,pH 4.5。由极差分析可知,各营养因素对菌丝体干质量影响的大小顺序为:可溶性淀粉>KH2PO4>MgSO4>蛋白胨。

图 4 Paxillus ammoniavirescens菌丝体在不同碳源、氮源和无机盐用量培养基中的生长情况
Figure 4. The growth of Paxillus ammoniavirescens mycelia in liquid media with different amount of carbon, nitrogen and inorganic salt
表 6 不同碳源、氮源、无机盐用量对Paxillus ammoniavirescens菌丝体生长的影响
Table 6. Effect of different amount of carbon, nitrogen and inorganic salt on mycelial growth of Paxillus ammoniavirescens
配方
Formula可溶性淀粉
Soluble
starch蛋白胨
PeptoneKH2PO4 MgSO4 菌丝体平均干质量
Average dry
weight of mycelia/mg1 15 2 1 0.5 42.5ab 2 15 4 3 1.5 42.5ab 3 15 6 5 4.5 37.5b 4 20 2 3 4.5 80a 5 20 4 5 0.5 52.5ab 6 20 6 1 1.5 52.5ab 7 25 2 5 1.5 32.5b 8 25 4 1 4.5 45ab 9 25 6 3 0.5 37.5b K1 122.5 155 140 132.5 K2 185 140 160 127.5 K3 115 127.5 122.5 162.5 R 70 27.5 37.5 35 -
通过rDNA ITS序列测定和分析,证明试验菌株为P. ammoniavirescens。在欧洲,Paxillus属可分为P. involutus complex 和P. rubicundulus,后者主要发生在湿地生境中,且只与桤木(Alnus spp., Betulaceae)有关[32]。而P. involutus complex种类则分布在更多样的生境中,并与多种树种有一定的联系。因此,寄主特异性是鉴别P. rubicundulus的一种有效特征,但在P. involutus复合种中进行种类鉴别仍然十分困难[21]。Fries [33]认为P. involutus存在着3个相互兼容的类群,第一类子实体主要分布在针叶林和落叶林中(森林组),第二组和第三组主要分布在公园和花园区域(公园组)。然而,这些群体的子实体之间没有明显的形态学差异,因此,被称为P. involutus同形种(隐蔽种)。不同作者对rDNA的系统发育分析[1,11,21,31]证实了5种不同的物种存在于P. involutus complex中: P. involutus, P. ammoniavirescens, P. cuprinus, P. obscurosporus和P. vernalis Watling (1969)。其中,根据形态特征进行鉴别是极其困难的。
Hedh et al. [11]鉴定EU078741,AY585915,AY585917为P. validus,而Jargeat et al. [21]则鉴定是P. ammoniavirescens,Anderson & Parkin[28]鉴定AM084700为P. involutus,且与AY585915有99.7%的相似度,在NCBI中比对AY585915也是P. involutus,即同一号菌株AY585915曾被鉴定为3个不同种,进一步说明在P. involutus复合种中进行种类鉴别十分困难。
本研究发现,P. ammoniavirescens在可溶性淀粉培养基上气生菌丝体生长旺盛,在葡萄糖、麦芽糖、甘露醇培养基上分泌较多褐色素,菌丝颜色较深,而在蔗糖、可溶性淀粉和玉米粉培养基上分泌褐色素较少,颜色浅。在氮源筛选中发现多数菌丝体在培养中后期有黄褐至黑褐色素形成,尤其在牛肉膏和硫酸铵培养基中分泌较多褐色素,说明培养基成分影响菌丝体的颜色和褐色素的形成。P. ammoniavirescens菌丝体培养中后期气生菌丝旺盛,浓密、粗壮、分枝明显,初期灰褐色,随培养时间的延长而呈黄褐色,褐色素分泌严重,并有少许硬质颗粒(菌核)形成(图5)。P. ammoniavirescens子实体受伤会变褐棕色,而菌丝体在固体培养基中分泌的褐色素可能与其有关,或许具有某种特殊的药用成分。

图 5 Paxillus ammoniavirescens培养中后期菌落特征
Figure 5. Colony of Paxillus ammoniavirescens in the middle and late stage of culture
Jargeat 等[21]采用完全固态MP(麦芽浸粉、蛋白胨)培养基(C+,含有18种无机盐和6种抗生素)和仅含2.5 g·L−1葡萄糖作为碳源的MP培养基(C−)于24 ℃条件下培养P. involutus、P. ammoniavirescens和P. cuprinus的菌丝体35 d,发现在C+培养基上3种菌丝体均产生棕色色素,在基质中扩散,并在菌丝上形成串珠(硬质颗粒)。P. cuprinus气生菌丝灰褐色,有褐色液滴,菌丝体日均生长速度为0.398~0.655 mm,在富含高碳量的培养基(葡萄糖、麦芽提取物、酪蛋白)中菌丝体更致密,由于色素产量高,培养基会产生棕色染色。P. involutus在加富培养基中,色素生成少,无褐色液滴,菌丝日均生长速度为0.463~0.773 mm。而绝大多数P. ammoniavirescens菌株生长迅速,在3~4周内可覆盖整个培养基,在加富培养基和贫瘠培养基上均有浓密的棉絮状气生菌丝、褐色液滴和硬的颗粒(菌核)。菌丝体日均生长速度为0.587~0.950 mm。本研究中菌丝体日均生长速度均快于这3个种,但与P. ammoniavirescens更接近,这与ITS序列比对和系统发育关系显示的该野生菌株为P. ammoniavirescens的分析结果相吻合。
-
本研究通过ITS序列比对及系统发育关系分析,证明该野生菌株为Paxillus ammoniavirescens。利用单因子试验筛选出了P. ammoniavirescens菌丝体生长的适宜碳源为可溶性淀粉,适宜氮源为蛋白胨,最适培养温度为25 ℃,最适pH为4.5。由正交试验优化的液体菌种培养的最佳配方为可溶性淀粉20 g、蛋白胨2 g、KH2PO4 3.0 g、MgSO4 4.5 g、水1 L。在此培养条件下可获得平均干质量为80 mg的菌丝体,明显高于其他配方。菌丝体在固体和液体培养基中的颜色差异较大,在固体培养基中的颜色因碳氮源种类不同而不同,分泌褐色素的程度有差异;在液体培养基中无褐色素分泌,菌丝体和培养液均呈鲜黄色。该研究结果将为P. ammoniavirescens种的菌丝体液体深层发酵培养、人工驯化栽培及药用成分开发利用提供理论基础,并可作为外生菌根菌在生物修复重金属污染、抗逆境胁迫等方面得以应用。
野生Paxillus ammoniavirescens菌的分子鉴定及生物学特性研究
Molecular Identification and Biological Characteristics of Wild Paxillus ammoniavirescens Strain
-
摘要:
目的 对野生食用菌进行分子鉴定及生物学特性研究,为其进一步液体深层发酵培养和开发利用奠定基础。 方法 采用rDNA ITS序列分析方法对一野生菌进行分子鉴定,通过单因素和正交试验确定了该菌株的生物学特性。 结果 由新鲜子实体分离得到的纯菌株为Paxillus ammoniavirescens,其菌丝体生长的最适碳源和氮源分别为可溶性淀粉和蛋白胨,最适培养温度为25 ℃,最适pH为4.5。 结论 卷边网褶菌菌丝体液体培养的最佳配方为:可溶性淀粉20 g,蛋白胨2 g,KH2PO4 3.0 g,MgSO4 4.5 g,水1 L。按此配方培养,可获得平均干质量为80 mg的菌丝体,明显高于其他配方。 -
关键词:
- Paxillus ammoniavirescens
- / 菌种分离
- / 转录间隔区(ITS)
- / 系统发育学
- / 生物学特性
Abstract:Objective To Understand the molecular identity and biological characteristics of wild edible fungi and lay foundation for their further culture, development and utilization. Method A wild strain of edible mushroom was examined by rDNA ITS sequence analysis and its biological characteristics were investigated by single factor and orthogonal test. Result The molecular feature of the mycelia generated from the fresh fruit body of the edible mushroom was proved to be Paxillus ammoniavirescens. The optimal carbon and nitrogen sources of its mycelial growth were found to be soluble starch and peptone with most favorable conditions of 25 ℃ and pH 4.5. Conclusion The best formula for mycelial liquid culture is 20 g soluble starch, 2 g peptone, 3.0 g KH2PO4, 4.5 g MgSO4 and 1 liter of water. In average, 80 mg dry weight of mycelia can be generated, which is obviously higher than other culture formulas. -
Key words:
- Paxillus ammoniavirescens
- / strain separation
- / ITS
- / phylogeny
- / biological characteristics
-
表 1 本研究中使用的物种来源和ITS 区域的GenBank序列号信息
Table 1. A list of species, origin and GenBank accession number of ITS sequences used in this study
序号No. 登录号
Accession no.种名
Species name来源国
Country生长宿主
Recorded trees1 ●MG571758 Paxillus ammoniavirescens China 云杉 Picea asperata 2 AM084700 Paxillus ammoniavirescens England 未知 Unknowna 3 AY585915 Paxillus ammoniavirescens France 栎树Quercusa 4 AY585917 Paxillus ammoniavirescens France 杨树 Populusb 5 KX610700 Paxillus ammoniavirescens Poland 未知 Unknownd 6 KX610698 Paxillus ammoniavirescens Poland 未知 Unknownd 7 JN661712 Paxillus ammoniavirescens England 栎树 Quercuse 8 JN661719 Paxillus ammoniavirescens Italy 杨树 Populuse 9 JN661715 Paxillus ammoniavirescens France 木本植物Woody plantse 10 JN661714 Paxillus ammoniavirescens England 椴树 Tiliae 11 KU671295 Paxillus ammoniavirescens Spain 木本植物 Woody plantsc 12 JN661711 Paxillus ammoniavirescens England 混合林 Mixed foreste 13 EU078741 Paxillus ammoniavirescens Sweden 栎树、桦树Quercus, Betulab 14 KX610699 Paxillus ammoniavirescens Poland 未知 Unknownd 15 KF261380 Paxillus ammoniavirescens France 桦树 Betulaf 16 KF261408 Paxillus ammoniavirescens France 冷杉 Abiesf 17 KF261388 Paxillus ammoniavirescens France 栎树 Quercusf 18 AF167692 Paxillus obscurisporus C. Hahn (1999) Germany 栎树 Quercusf 19 KF261367 Paxillus obscurisporus France 桦树 Betulaf 20 KF261386 Paxillus obscurisporus France 榛树 Corylusf 21 EU078724 Paxillus involutus Sweden 云杉 Piceaf 22 KF261411 Paxillus involutus France 冷杉 Abiesf 23 EU078740 Paxillus involutus Sweden 未知 Unknownb 24 KF261393 Paxillus involutus France 松树、桦树 Pinus, Betulaf 25 KF261402 Paxillus involutus France 冷杉 Abiesf 26 KF261371 Paxillus cuprinus Jargeat, Gryta, J.P. France 未知 Unknownf 27 EU078742 Paxillus cuprinus Sweden 栎树、桦树Quercus, Betulaf 28 KF261379 Paxillus cuprinus France 桦树 Betulaf 29 KM396776 Auricularia heimuer China 栎树 Quercusg 30 KM396777 Auricularia heimuer China 栎树Quercusg 注:a-f字母分别代表参考的文献。
Note: a According to Anderson & Parkin[28]. b According to Hedh et al.[12]. c According to Fernandez & Cagigal[29]. d According to Kalucka et al.[30]. e According to Vellinga et al.[31]. f According to Jargeat et al.[21]. g According to Wu et al.[26].表 2 碳源对Paxillus ammoniavirescens菌丝体生长的影响
Table 2. Effect of carbon sources on mycelial growth of Paxillus ammoniavirescens
碳源
Carbon source菌丝长势
Hyphal vigor日均长速
Daily growth rate/(mm·d−1)菌丝密度、整齐度
Hyphal density and uniformity麦芽糖
Maltose+++ 0.653c* 浓密、整齐
Dense, tidy甘露醇
Mannitol+++ 0.833b 浓密、整齐
Dense, tidy可溶性淀粉
Soluble starch+++ 0.978a 浓密、不齐
Dense, untidy玉米粉
Corn flour++ 0.713bc 较密、整齐
Relatively dense, tidy蔗糖
Sucrose++ 0.798b 较密、整齐
Relatively dense, tidy葡萄糖
Glucose+++ 0.968a 浓密、较整齐
Dense, relatively tidyCK + 0.469d 稀疏、不整齐
Sparse, untidy注:+表示菌丝体稀疏、生长势较弱;++表示菌丝体较密、生长势较强;+++表示菌丝体浓密、生长旺盛;*差异显著性(0.05)。
Note: + sparse mycelia, weaker growth vigor; ++ relatively dense mycelia and comparatively strong growth vigor; +++ dense mycelia and strong growth vigor. The lower case letters after daily growth rate indicating a significant difference at p 0.05.表 3 氮源对Paxillus ammoniavirescens菌丝体生长的影响
Table 3. Effect of nitrogen sources on mycelial growth of Paxillus ammoniavirescens
氮源
Nitrogen source菌丝长势
Hyphal vigor日均长速
Daily growth rate/(mm·d−1)菌丝密度、整齐度
Hyphal density and uniformity牛肉膏
Beef extract++ 0.644bc* 较密、整齐
Relatively dense, tidy麦麸
Wheat bran++ 0.743b 较密、整齐
Relatively dense, tidy硫酸铵
Ammonium sulfate++ 0.467de 较密、整齐
Relatively dense, tidy酵母膏
Yeast extract+++ 0.563cd 浓密、较整齐
Dense, relatively tidy黄豆粉
Soybean meal+ 0.668b 稀疏、整齐
Sparse, tidy蛋白胨
Peptone+++ 0.857a 浓密,整齐
Dense, tidyCK + 0.429e 稀疏、不齐
Sparse, untidy表注同表1;Foot notes as in Table 1 表 4 温度对Paxillus ammoniavirescens菌丝体生长的影响
Table 4. Effect of temperature on mycelial growth of Paxillus ammoniavirescens
温度/℃
Temperature菌丝体长势
Hyphal vigor日均长速
Daily growth
rate/(mm·d−1)菌丝体密度、整齐度
Hyphal density and uniformity21 ++ 0.514d* 较密、整齐
Relatively dense, tidy23 ++ 0.696c 较密、较整齐
Relatively dense and tidy25 +++ 1.257a 浓密、较整齐
Dense, relatively tidy27 +++ 1.002b 浓密,整齐
Dense, tidy29 +++ 0.785c 较密、整齐
Relatively dense, tidy31 + 0.214e 稀疏、不齐
Sparse, untidy表注同表1; Foot notes as in Table 1 表 5 酸碱度对Paxillus ammoniavirescens菌丝体生长的影响
Table 5. Effect of pH on mycelial growth of Paxillus ammoniavirescens
酸碱度
pH菌丝体长势
Hyphal vigor菌丝体干质量
Mycelial
dry weight/mg菌丝体颜色、发酵液颜色
Color of mycelia and
fermentation broth2.0 ++ 15bc* 黄色、淡黄
Yellow, light yellow2.5 ++ 20bc 黄色、淡黄
Yellow, light yellow3.0 +++ 32.5ab 黄棕色、黄棕色
Yellowish brown, yellowish brown3.5 +++ 32.5ab 黄棕色、棕黄色
Yellowish brown, yellowish brown4.0 +++ 33ab 黄棕色、棕黄色
Yellowish brown, yellowish brown4.5 +++ 50a 黄色、黄色
Yellow, yellow5.0 +++ 33ab 黄色、黄色
Yellow, yellow5.5 ++ 25bc 淡黄色、淡黄色
Light yellow, light yellow6.0 + 20bc 淡黄色、黄白色
Light yellow, yellowish white6.5 + 13bc 白色、白色
White, white7.0 + 12.5bc 白色、黄白色
White, yellowish white7.5 + 12.5bc 白色、黄白色
White, yellowish white8.0 + 10c 白色、黄白色
White, yellowish white表注同表1;Foot notes as in Table 1 表 6 不同碳源、氮源、无机盐用量对Paxillus ammoniavirescens菌丝体生长的影响
Table 6. Effect of different amount of carbon, nitrogen and inorganic salt on mycelial growth of Paxillus ammoniavirescens
配方
Formula可溶性淀粉
Soluble
starch蛋白胨
PeptoneKH2PO4 MgSO4 菌丝体平均干质量
Average dry
weight of mycelia/mg1 15 2 1 0.5 42.5ab 2 15 4 3 1.5 42.5ab 3 15 6 5 4.5 37.5b 4 20 2 3 4.5 80a 5 20 4 5 0.5 52.5ab 6 20 6 1 1.5 52.5ab 7 25 2 5 1.5 32.5b 8 25 4 1 4.5 45ab 9 25 6 3 0.5 37.5b K1 122.5 155 140 132.5 K2 185 140 160 127.5 K3 115 127.5 122.5 162.5 R 70 27.5 37.5 35 -
[1] Cagigal E F M, Sánchez A C. Influence of the culture media and the organic matter in the growth of Paxillus ammoniavirescens (Contu & Dessi)[J]. Mycobiology, 2017, 45(3): 172-177. doi: 10.5941/MYCO.2017.45.3.172 [2] Wallander H, Söderström B. Paxillus. [M]// Cairney J W G, Chambers S M (eds). Ectomycorrhizal Fungi: key genera in profile. Berlin: Springer-Verlag, 1999: 231–252. [3] 刘春光. 鞍山地区常见毒蘑菇分布及中毒情况分析[J]. 中国公共卫生, 2000, 16(7):632. doi: 10.3321/j.issn:1001-0580.2000.07.027 [4] 马启明. 铁岭地区的食用蘑菇[J]. 中国食用菌, 1986, 3(14):23-24, 49. [5] 马庭杰, 马文惠. 黄山和大别山区有毒大型真菌初探[J]. 食用菌, 1988, 9(1):6. [6] 卯晓岚, 陈玉梅, 何 俭. 呼伦贝尔采菇行[J]. 食用菌, 1987, 8(3):1-2. [7] 应建浙. 菌蕈拾零[J]. 食用菌, 1981, 2(2):48-49. [8] Winkelmann M, Stangel W, Schedel I, et al. Severe hemolysis caused by antibodies against the mushroom Paxillus involutus and its therapy by plasma exchange[J]. Klinische Wochenschrift, 1986, 64(19): 935-938. doi: 10.1007/BF01728620 [9] Anthowiak R, Anthowiak W Z, Banczyk I, et al. A new phenolic metabolite, involutone, isolated from the mushroom Paxillus involutus[J]. Canadian Journal of Chemistry, 2003, 81(1): 118-124. doi: 10.1139/v02-194 [10] 肖冬来, 马 璐, 应正河, 等. 广叶绣球菌溶血素基因的序列分析及表达动态[J]. 食用菌学报, 2016, 23(4):7-13. [11] Hedh J, Samson P, Erland S, et al. Multiple gene genealogies and species recognition in the ectomycorrhizal fungus Paxillus involutus[J]. mycological research, 2008, 112(8): 965-975. doi: 10.1016/j.mycres.2008.01.026 [12] 朱智梅, 张玉红, 撒 刚, 等. 外生菌根真菌Paxillus involutus 吸收Cd2+ 及H2O2对Cd2+ 内流的调控作用[J]. 北京林业大学学报, 2018, 40(4):24-32. [13] Colpaert J V, Assche J A V. The effects of cadmium on ectomycorrhizal Pinus sylvestris L[J]. New Phytologist, 1993, 123(2): 325-333. doi: 10.1111/j.1469-8137.1993.tb03742.x [14] Miransari M. Hyperaccumulators, arbuscular mycorrhizal fungi and stress of heavy metals[J]. Biotechnology Advances, 2011, 29(6): 645-653. doi: 10.1016/j.biotechadv.2011.04.006 [15] Khullar S, Reddy M S. Ectomycorrhizal fungi and its role in metal homeostasis through metallothionein and glutathione mechanisms[J]. Current Biotechnology, 2016, 5(3): 1-11. [16] 马永禄. 外生菌根真菌Paxillusinvolutus 提高灰杨(Populus×canescens) 对重金属Cd 的吸收和耐受能力[D]. 陕西杨凌: 西北农林科技大学, 2013. [17] Ott T, Fritz E, Polle A, et al. Characterization of antioxidative systems in the ectomycorrhiza-building basidiomycete Paxillus involutus (Bartsch) Fr. and its reaction to cadmium[J]. FEMS Microbiology Ecology, 2002, 42(3): 359-366. doi: 10.1111/j.1574-6941.2002.tb01025.x [18] 李 静. 抗盐菌根菌Paxillus与吸水剂提高树木耐盐机制研究[D]. 北京: 北京林业大学, 2011. [19] 陈应山, 陈国卿, 李春燕. 沈阳地区主要食用菌的生态观察[J]. 食用菌, 1988, 9(3):5. [20] 托马斯·莱瑟斯.蘑菇[M]. 北京:中国友谊出版社, 2008: 35. [21] Jargeat P, Chaumeton J P, Navaud O, et al. The Paxillus involutus (Boletales, Paxillaceae) complex in Europe: Genetic diversity and morphological description of the new species Paxillus cuprinus, typification of P. involutus s.s., and synthesis of species boundaries[J]. Fungal Biology, 2014, 118(1): 12-31. doi: 10.1016/j.funbio.2013.10.008 [22] Martin F, Cullen D, Hibbett D, et al. Sequencing the fungal tree of life[J]. New Phytologist, 2011, 190(4): 818-821. doi: 10.1111/j.1469-8137.2011.03688.x [23] Martin F, Bonito G M. Ten years of genomics for ectomycorrhizal fungi: what have we achieved and where are we heading? In: Zambonelli A, Bonito GM (eds), Edible Ectomycorrhizal Mushrooms[M]. Berlin Heidelberg: Springer-Verlag, 2012: 383–401. [24] 杜 萍. 中国野生毛木耳遗传多样性研究[D]. 北京: 北京林业大学, 2011. [25] 杜 萍, 曹天旭, 崔宝凯. 野生毛尖蘑菌株分子鉴定及碳氮源筛选试验[J]. 中国食用菌, 2019, 38(9):16-20. [26] Wu F, Yuan Y, Malysheva V F, et al. Species clarification of the most important and cultivated Auricularia mushroom “Heimuer”: evidence from morphological and molecular data[J]. Phytotaxa, 2014, 186(5): 241-253. doi: 10.11646/phytotaxa.186.5.1 [27] 雷 琼, 汪 俭, 范晓丹, 等. 1株野生大型食用菌的分子鉴定与同源性分析[J]. 长江大学学报: 自然科学版, 2013, 10(35):52-55, 68. [28] Anderson I C, Parkin P I. Detection of active soil fungi by RT-PCR amplification of precursor rRNA molecules[J]. Journal of Microbiological Methods, 2007, 68(2): 248-253. doi: 10.1016/j.mimet.2006.08.005 [29] Fernandez M, Cagigal E. Ectomycorrhizal fungi of woody plants on degraded lands of Asturias by mining and industrial activities[C]. Spain: University of Oviedo, 2014. [30] Kalucka I L, Jagodzinski A M, Nowinski M. Biodiversity of ectomycorrhizal fungi in surface mine spoil restoration stands in Poland - first time recorded, rare, and red-listed species[J]. Acta Mycologica, 2016, 51(2): 1080. [31] Vellinga E C, Blanchard E P, Kelly S, et al. Paxillus albidulus, P. ammoniavirescens, and P. validus revisited[J]. Mycotaxon, 2012, 119(1): 351-359. doi: 10.5248/119.351 [32] Orton PD. Notes on British agarics III[J]. Notes from the Royal Botanical Garden Edinburgh, 1969, 29: 75-127. doi: 10.1080/03746609609468919 [33] Fries N. Intersterility groups in Paxillus involutus[J]. Mycotaxon, 1985, 24: 403-409. -




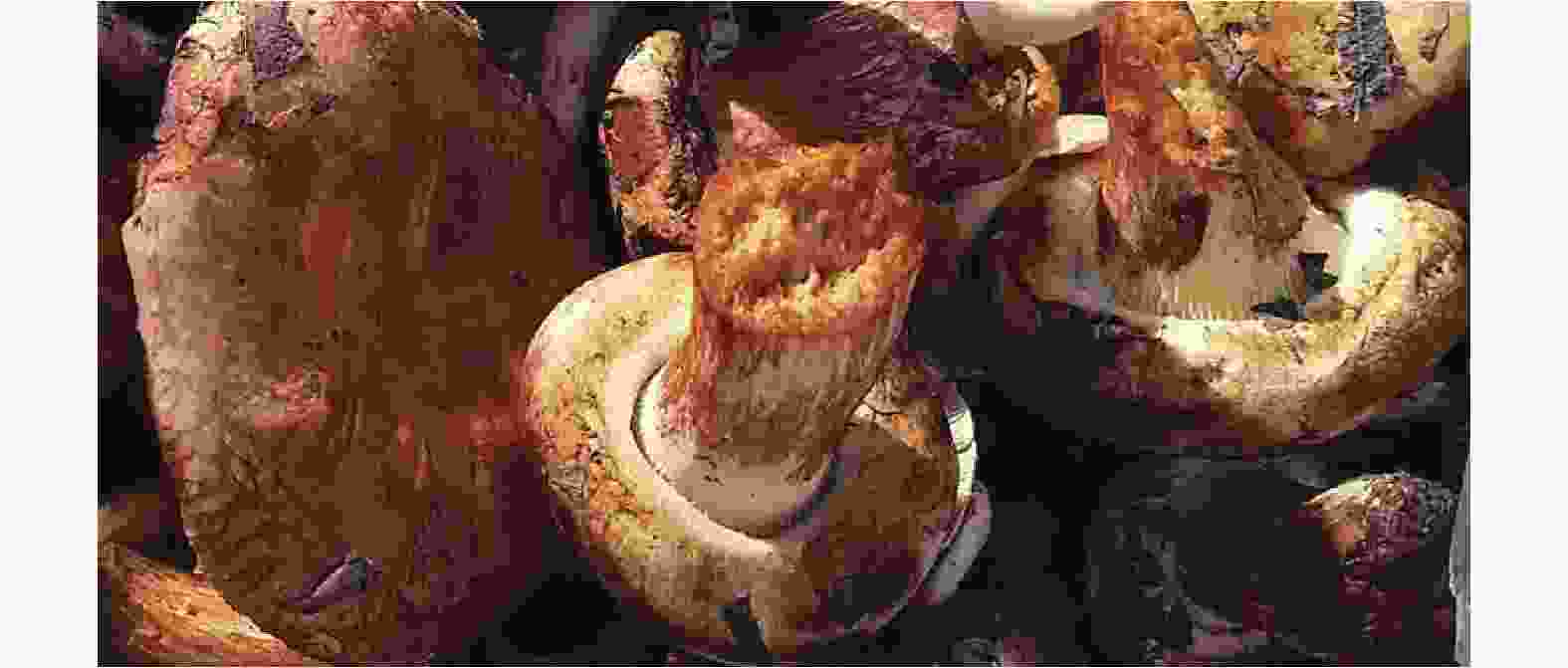
 下载:
下载: