-
人工林是世界森林资源的重要组成部分,在木材供给、改善生态环境和应对气候变化等方面发挥重要作用。随着中国对木材需求日益增长及生态环境保护意识的不断提高,大规模的造林和再造林促使中国人工林面积继续保持世界首位[1-2]。我国南亚热带地区气候条件优越,是重要的商品用材林基地,多年来大面积多代连栽的马尾松(Pinus massoniana Lamb.)、杉木(Cunninghamia lanceolata (Lamb.) Hook.)等人工针叶纯林以及外来速生树种桉树(Eucalyptus)等短轮伐期工业用材林,为区域经济发展和农民脱贫致富做出了重大贡献;但这些人工纯林极易造成土壤肥力衰退、生物多样性下降及病虫害日益严重等生态环境问题[3-5]。因此,当前倡导并实施人工林生态系统适应性经营亟需解决的关键问题,是如何科学合理地营造和经营管理人工林,从而有效提高其生产力并维持多重生态服务功能。建立乡土阔叶人工林可以兼顾珍贵用材生产、生物多样性保护、生态功能和生态系统稳定性改善[1]。采用红锥(Castanopsis hystrix Miq.)、米老排(Mytilaria laosensis Lec.)、火力楠(Michelia macclurei Dandy)和山白兰(Paramichelia bailonii (Pierre) Hu)等不同生物学特性的乡土珍贵阔叶树种造林已成为我国亚热带地区人工林经营的发展趋势[6]。
细菌是土壤中数量最多、分布最广并参与土壤有机质分解和矿化过程的主要微生物,在土壤结构形成与土壤肥力调节等方面起极其重要作用[7]。土壤细菌群落多样性是评价土壤质量的重要指标之一,土壤中细菌群落多样性愈高,越有利于提高土壤恢复力与抗压力[8]。土壤细菌群落从土壤有机质的分解和矿化中获取能量,且土壤的碳、氮和磷供给对细菌多样性有显著影响[9-10]。树种可通过其凋落物和根系分泌物等影响土壤理化性质[11-13],而土壤性质的改变会驱动土壤微生物群落组成和多样性的响应[14-15]。谭宏伟等[16]基于PCR-DGGE技术比较分析了广西红壤区桉树人工林、马尾松人工林和天然阔叶林对土壤细菌群落多样性的影响,罗达等[17]运用磷脂脂肪酸法(PLFAs)研究了我国南亚热带格木(Erythrophleum fordii Oliv.)、马尾松人工纯林及二者混交林林地土壤微生物生物量和群落结构特征,黄雪蔓等[18]采用磷脂脂肪酸法探究了固氮树种对第2代桉树人工林土壤微生物生物量和结构的影响。然而,有关我国南亚热带地区不同造林树种,尤其是乡土树种与外来树种对林地土壤细菌群落多样性影响的比较研究甚少。
本文以位于广西凭祥市中国林业科学研究院热带林业实验中心的马尾松、红锥、米老排、火力楠和尾巨桉(Eucalyptus urophylla×E.grandis)等不同树种人工林为研究对象,利用PCR-DGGE技术分析不同树种人工林对土壤细菌群落多样性的影响,并探讨土壤细菌群落多样性与土壤理化性质因子之间的内在联系,旨在提高对人工林土壤细菌多样性变化规律的认识,以期为该地区倡导并实施人工林生态系统适应性经营策略的树种选择提供土壤微生物生态学方面的理论依据。
-
研究区地处广西凭祥市中国林业科学研究院热带林业实验中心伏波试验场(106°51′~106°53′ E,22°02′~22°04′ N),该地区属于南亚热带季风区,为半湿润-湿润气候,干湿季节明显。年平均气温20.5~21.7℃,年平均降水量1 200~1 500 mm,年均蒸发量1 261~1 388 mm,空气相对湿度80%~84%。该地区地貌类型以低山丘陵为主,海拔430~680 m,土壤类型为红壤,土层厚度大于80 cm,pH值为4.8~5.5[19]。
-
2014年8月在研究区选取立地条件和经营措施相似的马尾松、红锥、米老排和火力楠等4种乡土树种人工林以及外来速生尾巨桉人工林为研究对象,其中,马尾松、红锥人工林于1983年营造,并分别于1993、1998、2009年进行了3次间伐(强度约30%);米老排、火力楠人工林在1981年种植,分别于1993年和2003年进行了2次间伐(强度约30%);尾巨桉人工林为2008年营造。上述5种林分均是在杉木人工林皆伐迹地上营建,初植密度均为2 500株·hm−2。5种林分的平均树高、平均胸径、保留株数如下:马尾松林的分别为19.4 m、29.2 cm、1 470株·hm−2,红锥林的分别为17.1 m、23.4 cm、1 075株·hm−2,米老排林的分别为19.7 m、19.2 cm、1 208株·hm−2,火力楠林的分别为18.0 m、17.4 cm、1 225株·hm−2,桉树林的分别为16.9 m、11.1 cm、2 300株·hm−2。
-
在5种人工林中按上、中、下坡位各设置1个20 m × 20 m的样地,并进行林分调查。在每个样地内的对角线上随机选取3个土壤采集点,挖取0~20 cm土层土壤剖面,将3个取样点土壤充分混合形成一个土壤样品,然后将这个土壤样品分成3份。一份装入铝盒用于测定土壤含水量;另一份装入布袋用于测定土壤化学性质;第三份装入聚乙烯保鲜袋并用生物冰袋保存带回实验室,挑出土壤样品中大的石砾、植物根系等杂物后过2 mm筛,放入−80℃超低温冰箱保存用于土壤细菌多样性测定。
-
土壤含水量(SWC)采用烘干法测定,pH值采用电位法测定(水:土为2.5:1)(Prtavo 907 MULTI pH,德国),土壤总碳(TC)含量采用Multi N/C 3100 TOC分析仪(Analytik Jena,德国)测定,全氮(TN)含量采用H2SO4-HClO4消解后用SmartChem200全自动化学元素分析仪(Alliance,法国)测定,土壤硝态氮(NO3−-N)和铵态氮(NH4+-N)含量采用SmartChem200全自动分析仪(Alliance,法国)测定,土壤全磷(TP)含量采用酸溶-钼锑抗比色法测定,有效磷(AP)含量采用盐酸-氟化铵法测定,全钾(TK)含量采用氢氧化钠碱熔-火焰光度法测定,速效钾(AK)含量采用乙酸铵浸提-火焰光度法测定[20]。土壤有效氮(AN)含量为硝态氮和铵态氮含量总和。
-
将新鲜土壤样本采用PowerSoil® DNA Isolation Kit试剂盒(MoBio,USA)进行基因组抽提,并取3 μL基因组DNA采用1.0%琼脂糖凝胶电泳检测,以确定基因组DNA是否可用于后续实验。以提取的土壤微生物DNA为模板,采用PCR对土壤细菌16S rRNA V3可变区进行扩增,其上游引物为357 F-GC(序列为CGCCCGCCGCGCGCGGCGGGCGGGGCGGGGGCACGGGGGG)和下游引物518 R(序列为ATTACCGCGGCTGCTGG)[16]。第1次PCR扩增体系为:BioLinker 2 × Taq Mix 20 μL,引物上游和下游各1 μL,DNA模板1 μL,补ddH2O至40 μL;其扩增程序为:94℃、2 min,然后94℃、30 s,56℃、30 s,72℃、30 s,25个循环,最后72℃延伸5 min。将PCR扩增产物采用AXYGEN公司的AxyPrepDNA凝胶回收试剂盒回收。回收产物进行二次PCR扩增。第2次PCR扩增体系为:BioLinker 2 × Taq Mix 20 μL,引物上游和下游各2 μL,DNA模板4 μL,补ddH2O至40 μL;扩增程序为:94℃、2 min,然后94℃、30 s,56℃、30 s,72℃、30 s,5个循环,最后72℃延伸5 min。PCR产物用1%琼脂糖凝胶电泳检测。
变性梯度凝胶电泳(DGGE)分析:采用Bio-Rad公司DcodeTM的基因突变检测系统对PCR反应产物进行分离。样品在变性剂浓度50%~75%(100%的变性胶为7 mol·L−1的尿素和40%的去离子甲酰胺的混合物)的8%丙烯酰胺凝胶中,在70 V的恒定电压下,60℃电泳15.5 h。电泳完毕后,加入400 mL Biolinker DNA Red染色液进行染色40 min后置于Bio-Rad凝胶成像系统中观察拍照。上述土壤细菌DNA提取、PCR扩增和DGGE分析由微基生物科技(上海)有限公司完成。
-
采用Quantity One分析软件(Bio-Rad)对各土壤样品的电泳条带数量进行统计分析,分别计算不同林分土壤细菌群落的丰富度(S)、Shannon指数(H)、Simpson指数(D)和均匀度(EH)等多样性指数[21]。采用单因素方差分析(One-Way ANOVA)及Duncan多重比较方法检测不同林分之间土壤理化性质参数、细菌群落多样性指数的差异显著性(p < 0.05)。在分析前,对各变量指标进行正态分布(Shapire-Wilk test)及方差齐性检验(Levene test),若不满足则对数据进行Box-Cox变换。采用Pearson相关性分析土壤细菌群落多样性指数与土壤理化性质的相关性。上述计算由IBM SPSS 24.0软件完成。
-
从表1可知:5种人工林的土壤总碳含量差异不显著(p > 0.05);尾巨桉人工林的土壤含水量、pH、全钾和速效钾含量明显高于4种乡土树种人工林,但其土壤全磷和有效磷含量却低于4种乡土树种人工林;4种乡土树种人工林相比,马尾松林具有较低的土壤含水量、pH、全氮和有效磷含量,火力楠林却拥有较高的土壤全氮、全磷、全钾、有效氮和速效钾含量,红锥林的土壤全钾、有效氮和速效钾含量最低,而米老排林具有最高的土壤含水量。
表 1 5种人工林土壤理化性质比较分析(n = 3)
Table 1. Comparative analysis of soil physicochemical properties among five different planted forests(n = 3).
参数
Parameters马尾松林
Pinus massoniana
plantation红锥林
Castanopsis hystrix
plantation米老排林
Mytilaria laosensis
plantation火力楠林
Michelia macclurei
plantation尾巨桉林
Eucalyptus urophylla ×
E.grandis plantation含水量
Moisture content/%29.68 ± 2.81 a 30.94 ± 2.98 ab 32.35 ± 2.31 ab 30.07 ± 3.79 ab 35.38 ± 0.82 b pH值
pH value4.30 ± 0.05 a 4.59 ± 0.09 b 4.37 ± 0.04 a 4.34 ± 0.02 a 5.02 ± 0.19 c 总碳
Total carbon/(g·kg−1)17.56 ± 9.59 a 20.19 ± 6.41 a 16.20 ± 3.32 a 17.74 ± 2.68 a 15.94 ± 1.24 a 全氮
Total nitrogen/(g·kg−1)0.67 ± 0.08 a 0.81 ± 0.22 ab 0.76 ± 0.30 a 1.18 ± 0.27 b 0.68 ± 0.05 a 全磷
Total phosphorus/(g·kg−1)0.23 ± 0.03 a 0.22 ± 0.02 a 0.20 ± 0.04 a 0.30 ± 0.03 b 0.12 ± 0.02 c 全钾
Total potassium/(g·kg−1)0.74 ± 0.29 a 0.64 ± 0.04 a 0.74 ± 0.13 a 1.13 ± 0.46 ab 1.46 ± 0.13 b 有效氮
Available nitrogen/(mg·kg−1)24.71 ± 9.15 a 10.36 ± 1.14 b 21.63 ± 4.90 ab 29.07 ± 6.27 a 19.73 ± 6.79 ab 有效磷
Available phosphorus/(mg·kg−1)1.36 ± 0.31 a 1.71 ± 0.38 a 1.69 ± 0.39 a 1.69 ± 0.43 a 0.60 ± 0.13 b 速效钾
Available potassium/(mg·kg−1)27.07 ± 10.08 bc 15.27 ± 2.85 a 17.83 ± 1.33 ab 27.83 ± 5.13 bc 30.93 ± 4.50 c 注:同行不同小写字母表示同一土壤参数不同林分类型间差异显著(p < 0.05)。
Note: Different lowercase letters in the same row indicate significant difference among different stand typesin the same soil parameter at 0.05 level. -
从5种人工林土壤样品提取的微生物基因组总DNA中各取3 μL用1%琼脂糖凝胶电泳检测,其结果(图1a)显示:DNA Marker条带亮度较好,且无明显拖带现象,可用于后续实验。从土壤细菌16S rRNA的V3可变区第2次PCR扩增产物各取4 μL于1%琼脂糖凝胶电泳检测结果(图1b)可知:PCR扩增后的DNA片段长度在250 bp左右,且无杂带,说明提取的DNA方法适合PCR扩增,可以直接进行后续实验。
-
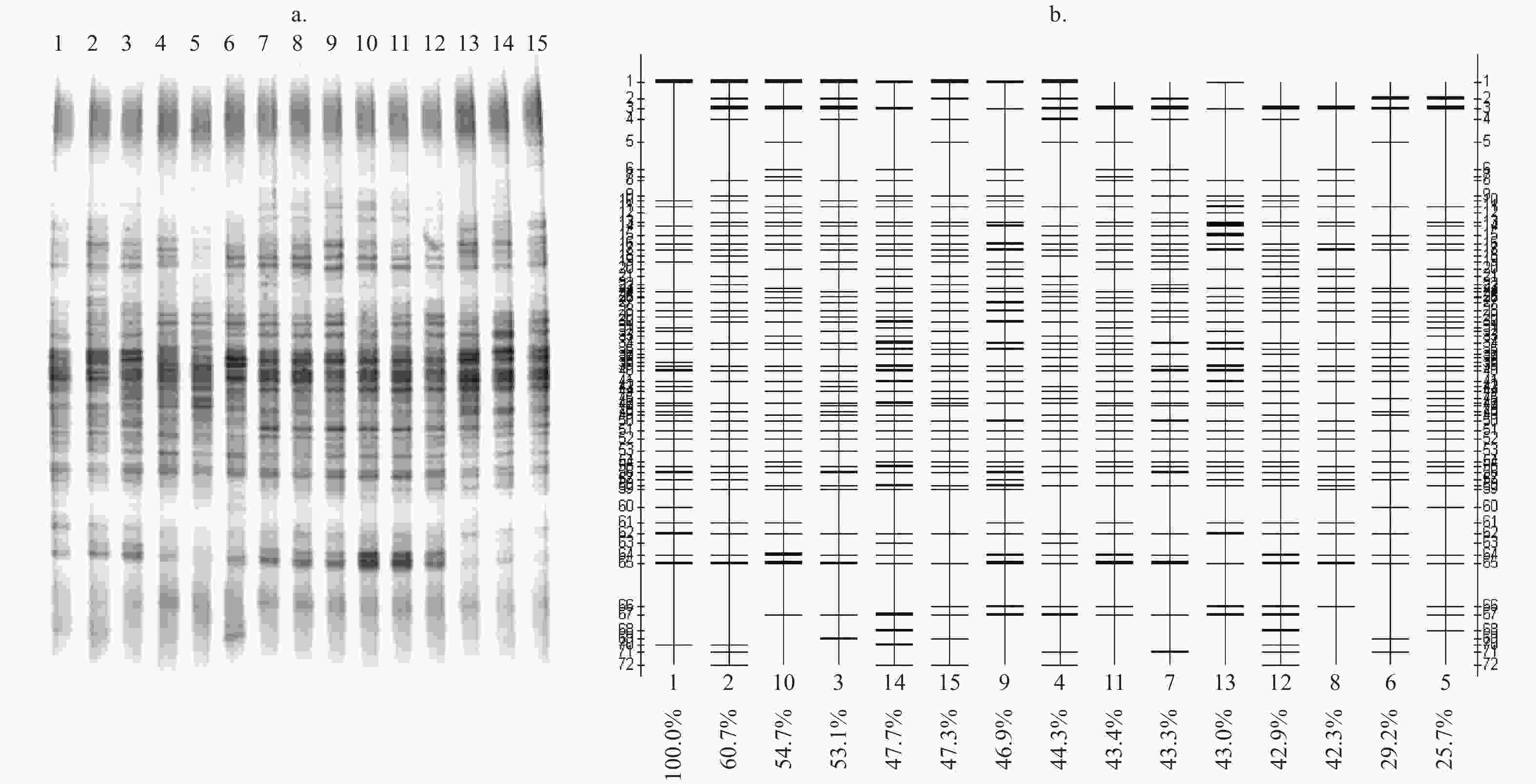
运用DGGE技术将各土壤样品中细菌的16S rRNA基因V3片段PCR产物分离出数目不等的电泳条带(图2a),经过Quantity One软件将原DGGE胶图转换成直观的条带分布图(图2b)。在图2b中,位于同一水平线的为相同物种,而左右两侧的数字为经分析后该板胶共有的条带数(也可认为是该板胶上所有样本包含的物种数),最下面一行的百分数是以第1个样本为基准的前提下,其余样本与第1样本的相似性。根据DGGE技术可以将长度相同而序列不同的DNA分离的原理,DGGE胶中条带数量越多,说明微生物种类丰富度越高[22]。5种林分土壤细菌DGGE图谱的条带数量顺序为:米老排林(45.67) > 红锥林(45.33) > 马尾松林(43.00) > 火力楠林(40.67) > 尾巨桉林(40.00)(表2)。
-
根据16S rRNA的PCR-DGGE图谱中条带的位置和亮度的数值化结果,计算各林分土壤细菌群落的丰富度、Shannon指数、Simpson指数和均匀度(表2)。由表2可知:各多样性指数在5种林分间的差异不显著(p > 0.05),但尾巨桉林土壤细菌群落的各多样性指数均略低于4种乡土树种人工林。
表 2 不同林分土壤细菌群落多样性比较(n = 3)
Table 2. Comparison of soil bacterial community diversity for different studied plantations(n = 3)
林分类型 Stand types 丰富度 Richness Shannon指数 Shannon index Simpson指数 Simpson index 均匀度 Evenness 马尾松林 Pinus massoniana plantation 43.00 ± 2.65 3.28 ± 0.04 0.94 ± 0.01 0.87 ± 0.02 红锥林 Castanopsis hystrix plantation 45.33 ± 4.51 3.34 ± 0.26 0.94 ± 0.03 0.88 ± 0.07 米老排林 Mytilaria laosensis plantation 45.67 ± 2.08 3.28 ± 0.17 0.94 ± 0.02 0.86 ± 0.04 火力楠林 Michelia macclurei plantation 40.67 ± 3.21 3.32 ± 0.18 0.94 ± 0.02 0.90 ± 0.04 尾巨桉林 Eucalyptus urophylla × E.grandis plantation 40.00 ± 3.97 3.03 ± 0.17 0.91 ± 0.03 0.82 ± 0.02 -
土壤样品的细菌群落多样性指标与土壤理化性质参数的Pearson相关分析(表3)表明:5种林分土壤细菌群落的Shannon指数、Simpson指数和均匀度与土壤全氮显著正相关(p < 0.05),而其Simpson指数和均匀度与土壤全磷显著正相关(p < 0.05)。
表 3 土壤细菌群落多样性指数与土壤理化性质的Pearson相关系数
Table 3. Pearson correlation coefficient between diversity indices of soil bacterial community and soil physicochemical properties
参数 Parameters 丰富度 Richness Shannon指数 Shannon index Simpson指数 Simpson index 均匀度 Evenness 含水量 Moisture content 0.003 −0.259 −0.275 −0.325 pH值 pH value −0.135 −0.467 −0.506 −0.510 总碳 Total carbon −0.061 0.265 0.298 0.365 全氮 Total nitrogen 0.019 0.539* 0.525* 0.662* 全磷 Total phosphorus −0.059 0.481 0.536* 0.631* 全钾 Total potassium −0.486 −0.455 −0.378 −0.313 有效氮 Available nitrogen −0.008 0.147 0.215 0.175 有效磷 Available phosphorus 0.242 0.400 0.445 0.370 速效钾 Available potassium −0.480 −0.384 −0.231 −0.119 注Note:* p < 0.05. -
在我国南亚热带地区,将针叶或外来速生树种人工林转变为乡土阔叶树种后其人工林生态系统功能的变化已引起生态学者关注[4, 23]。本文利用PCR-DGGE技术,探讨马尾松、红锥、米老排和火力楠等4种乡土树种人工林及外来树种尾巨桉人工林对林地土壤(0~20 cm)细菌群落多样性的影响,结果表明,尾巨桉林土壤细菌群落的丰富度、Shannon指数、Simpson指数和均匀度与4种乡土树种人工林之间的差异不显著(p > 0.05),这与谭宏伟等[16]关于广西红壤区桉树人工林土壤细菌丰富度、多样性指数以及均匀度皆与乡土树种马尾松人工林之间无显著差异的结论基本一致。
不同的植物凋落物数量和质量以及根系分泌物化学特性的不同必然引起土壤理化性质的变化,进而引起土壤微生物群落结构及多样性的改变[24-25]。土壤氮素是土壤细菌的重要营养来源,而土壤中的全氮是衡量土壤氮素供应状况的重要指标[26]。白晓旭等[27]研究认为,全氮是影响河南宝天曼自然保护区不同林龄锐齿栎(Quercus aliena Bl. var. acuteserrata Maxim. ex Wenz)及不同林分类型(短柄枹(Quercus glandulifera var. brevipetiolata Nakai)林、栓皮栎(Quercus variabilis Bl.)林、锐齿栎/华山松(Pinus armandii Franch.)混交林和80年生锐齿栎林)土壤细菌群结构变化的重要因子,且随全氮含量的增加,土壤菌群物种多样性呈增加趋势;朱平等[28]发现,祁连山不同植被类型(垫状植被、高寒草甸、沼泽化草甸和高寒灌丛)土壤微生物群落多样性与全氮显著正相关(p < 0.05)。本研究中,5种人工林土壤细菌多样性与土壤全氮显著正相关(p < 0.05),与上述研究结果基本一致。此外,土壤中磷素也是土壤细菌的重要营养来源,但是土壤中的磷素大部分以迟效性状态存在,全磷含量高并不意味着磷素供给充足,而全磷含量低于某一水平时却可能意味着磷素供应不足[29]。我国土壤全磷含量为0.2~1.1 g·kg−1,若全磷含量低于0.4 g·kg−1则有可能磷供应不足[20]。本研究中,5种人工林土壤全磷含量(0.12~0.30 g·kg−1)低于0.4 g·kg−1,导致土壤全磷成为细菌在土壤中生存和繁殖的影响因子,这可能是5种林分土壤细菌群落多样性与土壤全磷显著正相关的缘故。
在森林生态系统中,由于水分、养分、通气、温度、pH值等因子在土壤剖面上存在差异,导致土壤细菌多样性也存在某种程度上的差别[30-31]。张社奇等[32]在研究黄土高原刺槐(Robinia pseudoacacia Linn.)林地土壤微生物垂直分布时发现,土壤深度对细菌数量的分布具有显著影响;杜璨等[33]探讨了红桦(Betula albosinensis Burk.)林4个土壤层(0~10、10~20、20~40、40~60 cm)细菌群落丰富度、多样性指数和细菌群落组成及丰度变化;彭雯等[6]指出,不同土层(0~20、20~40 cm)在门、纲、目分类水平上均表现出桉树林土壤细菌群落组成与其他5种乡土树种(红锥、米老排、火力楠、山白兰和马尾松)人工林存在明显差异。然而,本文仅讨论了南亚热带5种不同树种人工林对0~20 cm土层细菌群落的丰富度、Shannon指数、Simpson指数和均匀度的影响,那么这5种人工林之间土壤细菌群落多样性的差异是否依土层不同而不同?还有待进一步研究。另外,我国南亚热带地区气候干湿季分明(4—9月为湿季,10月至翌年3月为干季),而不同季节会对植被土壤微生物群落多样性产生影响[28, 34-35]。因此,本文研究的5种人工林对土壤细菌群落多样性的影响是否会因季节而异,还需深入探究。
-
南亚热带地区的马尾松、红锥、米老排、火力楠和尾巨桉等人工林在0~20 cm土层间土壤细菌群落多样性无显著差异,5种人工林土壤细菌群落多样性与土壤全氮和全磷显著正相关。说明乡土阔叶树种(红锥、米老排和火力楠)人工林对表层土壤细菌群落多样性的影响效果与乡土针叶马尾松人工林及外来尾巨桉人工林相似。因此,在该地区营建乡土树种人工林与外来按树人工林对土壤细菌群落多样性的影响效果无明显差异。
南亚热带不同树种人工林对土壤细菌群落多样性的影响
Effects of Different Tree Species Plantations on Soil Bacterial Community Diversity in South Subtropical China
-
摘要:
目的 探讨我国南亚热带地区不同树种人工林对土壤细菌群落多样性的影响,为该地区实施人工林生态系统适应性经营策略的树种选择提供土壤微生物生态学方面的科学依据。 方法 采用PCR-DGGE技术,比较分析位于广西凭祥市中国林业科学研究院热带林业实验中心的4个乡土树种(马尾松、红锥、米老排和火力楠)人工林和外来树种尾巨桉人工林土壤(0~20 cm)细菌群落的丰富度、多样性和均匀度,并探讨了土壤细菌群落多样性与土壤理化性质因子之间的相互关系。 结果 5种不同树种人工林土壤细菌群落多样性之间无显著差异(p > 0.05),其土壤细菌群落多样性与土壤全氮和全磷呈显著正相关(p < 0.05)。 结论 从土壤细菌群落多样性看,在该地区营建乡土树种人工林与外来桉树人工林的效果无明显差异。 -
关键词:
- 土壤细菌群落
- / PCR-DGGE技术
- / 人工林
- / 南亚热带
Abstract:Objective To examine the effects of plantations composed of different tree species on soil bacterial community diversity in south subtropical China, and to provide reference for the selection of tree species for the adaptive management strategy of plantation ecosystem in this region. Method The richness, Shannon index, Simpson index and evenness of soil (0-20 cm) bacterial communities under four indigenous tree species (Pinus massoniana Lamb., Castanopsis hystrix (Lamb.) Hook., Mytilaria laosensis Lec. and Michelia macclurei Dandy) plantations and the plantation of exotic tree species Eucalyptus urophylla × E.grandis were studied by using PCR-DGGE technology in the Experimental Center of Tropical Forestry of Chinese Academy of Forestry in Pingxiang, Guangxi. Moreover, the relationship between soil bacterial community diversity and soil physichemical properties was discussed. Result No significant difference in diversity of soil bacterial communities was observed among the five types of plantations (p > 0.05). The bacterial community diversity of the five plantations was significantly and positively correlated with total nitrogen and total phosphorus (p < 0.05). Conclusion There is no significant difference between the native tree species plantation and the exotic eucalyptus plantation in this area in view of soil bacterial community diversity. -
Key words:
- soil bacterial community
- / PCR-DGGE technology
- / planted forest
- / south subtropical China
-
表 1 5种人工林土壤理化性质比较分析(n = 3)
Table 1. Comparative analysis of soil physicochemical properties among five different planted forests(n = 3).
参数
Parameters马尾松林
Pinus massoniana
plantation红锥林
Castanopsis hystrix
plantation米老排林
Mytilaria laosensis
plantation火力楠林
Michelia macclurei
plantation尾巨桉林
Eucalyptus urophylla ×
E.grandis plantation含水量
Moisture content/%29.68 ± 2.81 a 30.94 ± 2.98 ab 32.35 ± 2.31 ab 30.07 ± 3.79 ab 35.38 ± 0.82 b pH值
pH value4.30 ± 0.05 a 4.59 ± 0.09 b 4.37 ± 0.04 a 4.34 ± 0.02 a 5.02 ± 0.19 c 总碳
Total carbon/(g·kg−1)17.56 ± 9.59 a 20.19 ± 6.41 a 16.20 ± 3.32 a 17.74 ± 2.68 a 15.94 ± 1.24 a 全氮
Total nitrogen/(g·kg−1)0.67 ± 0.08 a 0.81 ± 0.22 ab 0.76 ± 0.30 a 1.18 ± 0.27 b 0.68 ± 0.05 a 全磷
Total phosphorus/(g·kg−1)0.23 ± 0.03 a 0.22 ± 0.02 a 0.20 ± 0.04 a 0.30 ± 0.03 b 0.12 ± 0.02 c 全钾
Total potassium/(g·kg−1)0.74 ± 0.29 a 0.64 ± 0.04 a 0.74 ± 0.13 a 1.13 ± 0.46 ab 1.46 ± 0.13 b 有效氮
Available nitrogen/(mg·kg−1)24.71 ± 9.15 a 10.36 ± 1.14 b 21.63 ± 4.90 ab 29.07 ± 6.27 a 19.73 ± 6.79 ab 有效磷
Available phosphorus/(mg·kg−1)1.36 ± 0.31 a 1.71 ± 0.38 a 1.69 ± 0.39 a 1.69 ± 0.43 a 0.60 ± 0.13 b 速效钾
Available potassium/(mg·kg−1)27.07 ± 10.08 bc 15.27 ± 2.85 a 17.83 ± 1.33 ab 27.83 ± 5.13 bc 30.93 ± 4.50 c 注:同行不同小写字母表示同一土壤参数不同林分类型间差异显著(p < 0.05)。
Note: Different lowercase letters in the same row indicate significant difference among different stand typesin the same soil parameter at 0.05 level.表 2 不同林分土壤细菌群落多样性比较(n = 3)
Table 2. Comparison of soil bacterial community diversity for different studied plantations(n = 3)
林分类型 Stand types 丰富度 Richness Shannon指数 Shannon index Simpson指数 Simpson index 均匀度 Evenness 马尾松林 Pinus massoniana plantation 43.00 ± 2.65 3.28 ± 0.04 0.94 ± 0.01 0.87 ± 0.02 红锥林 Castanopsis hystrix plantation 45.33 ± 4.51 3.34 ± 0.26 0.94 ± 0.03 0.88 ± 0.07 米老排林 Mytilaria laosensis plantation 45.67 ± 2.08 3.28 ± 0.17 0.94 ± 0.02 0.86 ± 0.04 火力楠林 Michelia macclurei plantation 40.67 ± 3.21 3.32 ± 0.18 0.94 ± 0.02 0.90 ± 0.04 尾巨桉林 Eucalyptus urophylla × E.grandis plantation 40.00 ± 3.97 3.03 ± 0.17 0.91 ± 0.03 0.82 ± 0.02 表 3 土壤细菌群落多样性指数与土壤理化性质的Pearson相关系数
Table 3. Pearson correlation coefficient between diversity indices of soil bacterial community and soil physicochemical properties
参数 Parameters 丰富度 Richness Shannon指数 Shannon index Simpson指数 Simpson index 均匀度 Evenness 含水量 Moisture content 0.003 −0.259 −0.275 −0.325 pH值 pH value −0.135 −0.467 −0.506 −0.510 总碳 Total carbon −0.061 0.265 0.298 0.365 全氮 Total nitrogen 0.019 0.539* 0.525* 0.662* 全磷 Total phosphorus −0.059 0.481 0.536* 0.631* 全钾 Total potassium −0.486 −0.455 −0.378 −0.313 有效氮 Available nitrogen −0.008 0.147 0.215 0.175 有效磷 Available phosphorus 0.242 0.400 0.445 0.370 速效钾 Available potassium −0.480 −0.384 −0.231 −0.119 注Note:* p < 0.05. -
[1] 刘世荣, 杨予静, 王 晖. 中国人工林经营发展战略与对策: 从追求木材产量的单一目标经营转向提升生态系统服务质量和效益的多目标经营[J]. 生态学报, 2018, 38(1):1-10. [2] 郑 路, 蔡道雄, 卢立华, 等. 南亚热带不同树种人工林生物量及其分配格局[J]. 林业科学研究, 2014, 27(4):454-458. [3] He Y, Qin L, Li Z, et al. Carbon storage capacity of monoculture and mixed-species plantations in subtropical China[J]. Forest Ecology and Management, 2013, 295: 193-198. doi: 10.1016/j.foreco.2013.01.020 [4] Wang H, Liu S R, Mo J M, et al. Soil organic carbon stock and chemical composition in four plantations of indigenous tree Species in subtropical China[J]. Ecological Research, 2010, 25(6): 1071-1079. doi: 10.1007/s11284-010-0730-2 [5] 徐伟强, 周 璋, 赵厚本, 等. 南亚热带3种常绿阔叶次生林的生物量结构和固碳现状[J]. 生态环境学报, 2015, 24(12):1938-1943. [6] 彭 雯, 谭 玲, 明安刚, 等. 南亚热带典型人工纯林土壤剖面细菌群落组成差异分析[J]. 土壤通报, 2018, 49(6):1361-1369. [7] Nannipieri P, Ascher-Jenull J, Ceccherini M T, et al. Microbial diversity and soil functions[J]. European Journal of Soil Science, 2003, 54(4): 655-670. doi: 10.1046/j.1351-0754.2003.0556.x [8] Zhou J, Xia B, Treves D S, et al. Spatial and resource factors influencing high microbial diversity in soil[J]. Applied and Environmental Microbiology, 2002, 68(1): 326-334. doi: 10.1128/AEM.68.1.326-334.2002 [9] Zechmeister-Boltenstern S, Keibliinger K M, Mooshammer M, et al. The application of ecological stoichiometry to plant–microbial–soil organic matter transformations[J]. Ecological Monographs, 2015, 85(2): 133-155. doi: 10.1890/14-0777.1 [10] Zhang C, Liu G, Xue S, et al. Soil bacterial community dynamics reflect changes in plant community and soil properties during the secondary succession of abandoned farmland in the Loess Plateau[J]. Soil Biology and Biochemistry, 2016, 97: 40-49. doi: 10.1016/j.soilbio.2016.02.013 [11] Atushi O, Motomu M, Shuichi S. Impacts of root symbiotic associations on interspecific variation in sugar exudation rates and rhizosphere microbial communities: a comparison among four plant families[J]. Plant and Soil, 2016, 399(1-2): 345-356. doi: 10.1007/s11104-015-2703-2 [12] Ushio M, Balser T C, KitayamaK. Effects of condensed tannins in conifer leaves on the composition and activity of the soil microbial community in a tropical montane forest[J]. Plant and Soil, 2013, 365(1-2): 157-170. doi: 10.1007/s11104-012-1365-6 [13] 郝 建, 莫慧华, 黄弼昌, 等. 西南桦和尾巨桉凋落叶分解及其与土壤性质的相关性[J]. 林业科学研究, 2016, 29(2):202-208. doi: 10.3969/j.issn.1001-1498.2016.02.008 [14] Lladós S, Lóéópez-Mondóéjar R E N, Baldrian P. Forest soil bacteria: diversity, involvement in ecosystem processes, and response to global change[J]. Microbiology and Molecular Biology Reviews, 2017, 81: e00063-16. [15] Nakayma M, Imamuea S, Taniguchi T, et al. Does conversion from natural forest to plantation affect fungal and bacterial biodiversity, community structure, and co-occurrence networks in the organic horizon and mineral soil?[J]. Forest Ecology and Management, 2019, 446: 238-250. doi: 10.1016/j.foreco.2019.05.042 [16] 谭宏伟, 杨尚东, 吴 俊, 等. 红壤区桉树人工林与不同林分土壤微生物活性及细菌多样性的比较[J]. 土壤学报, 2014, 51(3):575-584. [17] 罗 达, 史作民, 唐敬超, 等. 南亚热带乡土树种人工纯林及混交林土壤微生物群落结构[J]. 应用生态学报, 2014, 25(9):2543-2550. [18] 黄雪蔓, 刘世荣, 尤业明. 固氮树种对第二代桉树人工林土壤微生物生物量和结构的影响[J]. 林业科学研究, 2014, 27(5):612-620. [19] 覃 林, 何友均, 李智勇, 等. 南亚热带红椎马尾松纯林及其混交林生物量和生产力分配格局[J]. 林业科学, 2011, 47(12):17-21. doi: 10.11707/j.1001-7488.20111203 [20] 鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 1999: 169-195. [21] 罗海峰, 齐鸿雁, 张洪勋. 乙草胺对农田土壤细菌多样性的影响[J]. 微生物学报, 2004, 44(4):519-522. doi: 10.3321/j.issn:0001-6209.2004.04.025 [22] Krsek M, Wellington E M H. Comparison of different methods for the isolation and purification of total community DNA from soil[J]. Journal of Microbiological Methods, 1999, 39(1): 1-16. doi: 10.1016/S0167-7012(99)00093-7 [23] 覃 林, 马雪珍, 吴水荣, 等. 南亚热带典型乡土阔叶人工林与桉树人工林土壤微生物量氮及可溶性氮特征[J]. 应用与环境生物学报, 2017, 23(4):678-684. [24] Hooper D U, Bignell D E, Brown V K, et al. Interactions between aboveground and belowground biodiversity in terrestrial ecosystems: patterns, mechanisms, and feedbacks[J]. BioScience, 2000, 50(12): 1049-1061. doi: 10.1641/0006-3568(2000)050[1049:IBAABB]2.0.CO;2 [25] Fierer N, Jackson R B. The diversity and biogeography of soil bacterial communities[J]. Proceedings of the National Academy of Sciences of the United States of America, 2006, 103(3): 626-631. doi: 10.1073/pnas.0507535103 [26] 杨 菁, 周国英, 田媛媛, 等. 降香黄檀不同混交林土壤细菌多样性差异分析[J]. 生态学报, 2015, 35(24):8117-8127. [27] 白晓旭, 史荣久, 尤业明, 等. 河南宝天曼不同林龄与林型森林土壤的细菌群落结构与多样性[J]. 应用生态学报, 2015, 26(8):2273-2281. [28] 朱 平, 陈仁升, 宋耀选, 等. 祁连山不同植被类型土壤微生物群落多样性差异[J]. 草业学报, 2015, 24(6):75-84. doi: 10.11686/cyxb2014272 [29] 李亚娟, 曹广民, 龙瑞军. 不同草地利用方式对土壤有机碳、全氮和全磷的影响[J]. 草原与草坪, 2012, 32(5):26-29,35. doi: 10.3969/j.issn.1009-5500.2012.05.006 [30] 李钧敏, 金则新, 张崇邦. 不同土层土壤细菌的遗传多样性及其与环境因子的相关性[J]. 浙江大学学报: 理学版, 2006, 33(6):695-701. [31] López-Mondéjar R, Voříšková J, Větrovský T, et al. The bacterial community inhabiting temperate deciduous forests is vertically stratified and undergoes seasonal dynamics[J]. Soil Biology and Biochemistry, 2015, 87: 43-50. doi: 10.1016/j.soilbio.2015.04.008 [32] 张社奇, 王国栋, 田 鹏, 等. 黄土高原刺槐林地土壤微生物的分布特征[J]. 水土保持学报, 2004, 18(6):128-131. doi: 10.3321/j.issn:1009-2242.2004.06.031 [33] 杜 璨, 许晨阳, 王 强, 等. 秦岭红桦林土壤细菌群落剖面分布特征及其影响因素[J]. 环境科学, 2017, 38(7):3010-3019. [34] 吴则焰, 林文雄, 陈志芳, 等. 武夷山国家自然保护区不同植被类型土壤微生物群落特征[J]. 应用生态学报, 2013, 24(8):2301-2309. [35] 赵永鑫, 徐天梅, 郑亚强, 等. 西双版纳自然保护区干热季不同植被土壤微生物群落多样性[J]. 西部林业科学, 2020, 49(3):132-140. -





 下载:
下载: